
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
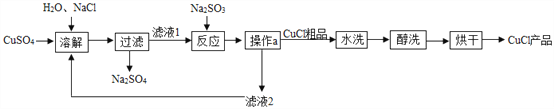
(1)“滤液1”中除了Na+、SO42-外,还存在较多的离子是_______(写离子符号)。
(2)“反应”中发生的化学变化是2CuCl2+2Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为_______________。
(3)“操作a”的名称是______。“醇洗”的目的是____________。
(4)本流程中可以循环利用的物质(水除外)是_________(写化学式)。
(5)320 g CuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是____________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘( I2)而泛黄变质。化学兴趣小组查得以下资料:
Ⅰ.对于碘化钾变质的原理,有两种不同的反应:
甲:4 KI+O2 +2CO2= 2K2CO3 +2I2 乙:4KI+ O2 +2H2O=4KOH +2I2
Ⅱ. KOH与NaOH两者的化学性质相似。为探究碘化钾变质原理的合理性,进行以下实验。
【实验过程】
[实验1]取适量碘化钾固体暴露于空气中一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
(1)石灰水变浑浊的原因是_______________(用化学方程式表示)。
(2)化学兴趣小组的同学认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。理由是_____________________。
[实验2]按甲图所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
(3)据此现象,可得出的结论是_________________。
[实验3]按乙图所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
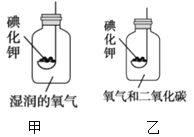
查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行。化学兴趣小组据此改进实验,很快观察到固体泛黄的现象。
(4)简述化学兴趣小组改进实验的具体措施:________________。
【实验结论】
(5)根据上述实验,化学兴趣小组得出结论:碘化钾固体泛黄变质是碘化钾与________共同作用的结果。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组进行CO2气体的制取、并验证CO2能与NaOH发生化学反应的实验。
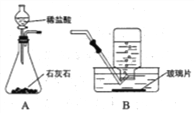
(1)用上图装置制取CO2气体。
①写出反应的化学方程式: ____________。
②A装置用分液漏斗加液,与用长颈漏斗加液比较,其优点是_______________。
③从B装置中取出收集满CO2气体集气瓶的操作是_____________。
(2)通过C装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量溶质质量分数为20%的NaOH溶液,振荡集气瓶后打开止水夹。
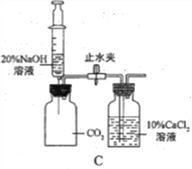
①打开止水夹后观察到的现象是______。
②反应后将集气瓶中混合物过滤,所得溶液中除CaCl2外,还存在的溶质有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)实验室用高锰酸钾制取氧气:__________________________。
(2)铁丝在氧气中燃烧:__________________________。
(3)熟石灰中和含硫酸的废水:__________________________。
(4)碳酸氢铵受热分解:__________________________。
(5)镁在二氧化碳中燃烧生成氧化镁和碳单质:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
选项 | 甲 | 乙 | 丙 |
A | C | CO2 | CO |
B | H2O2 | O2 | H2O |
C | CuO | Cu | CuSO4 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100 g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。则下列说法正确的是
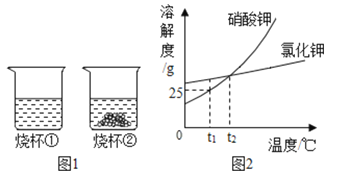
A. 烧杯①的溶液一定是不饱和溶液
B. 烧杯①的溶液是硝酸钾溶液
C. t1℃时烧杯②的溶液的溶质质量分数为25 %
D. 若烧杯①和烧杯②的溶液都升温到t2℃时,两种溶液的溶质质量分数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于复分解反应的是
A. CaO+2H2O=Ca(OH)2 B. CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
C. 2H2O![]() 2H2O+O2↑ D. Zn+H2SO4=ZnSO4+H2↑
2H2O+O2↑ D. Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某黄铜(铜锌合金)中锌的质量分数,某校研究小组取10 g样品置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中物质的总质量与加入稀硫酸的质量关系如图所示。
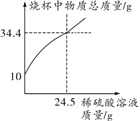
请计算:
(1)该黄铜样品中锌的质量分数为___________。
(2)所用稀硫酸的溶质质量分数为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀H2SO4,加入到盛有NaOH溶液的小烧杯中。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是________。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有________。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | ___________ | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【实验结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出【实验结论】(2)中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
(1)实验操作中的错误是________________________。
(2)实验方案中也有一个是错误的,错误的原因是___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组的同学利用下图装置制取并收集一瓶二氧化碳气体,请和他们一起完成以下实验探究。
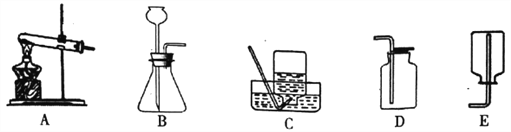
(1)实验室制取一瓶二氧化碳气体,应选用的发生装置为______________(填序号),反应的化学方程式为___________________。
(2)一氧化氮是一种密度比空气略大,难溶于水的无色气体,易与空气中的氧气反应生成红棕色的二氧化氮气体,则收集一氧化氮气体应选择________装置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com