
科目: 来源: 题型:
【题目】某实验小组设计了下图所示的实验装置。
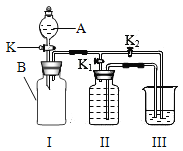
(1)甲同学认为若II装置中装有水,可用于制取并收集氧气,请写出K1、K2的开关顺序________。
(2)乙同学认为可以利用I、III装置验证二氧化碳的性质。若广口瓶B中盛放二氧化碳,A中盛放氢氧化钠溶液,烧杯中盛放稀盐酸,验证二氧化碳能与氢氧化钠发生反应,他的操作为________________,最终他看到了III中稀盐酸倒流入I中有气泡产生。
(3)丁同学认为将III的烧杯换成量简,Ⅱ中的广口瓶装满水,则可以利用I、Ⅱ、III装置测定氢氧化钠样品中含碳酸钠杂质的质量分数,丁同学测定方法利用的化学反应的化学方程式是____________,你认为此方案是否可行,并简述理由_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学在探究Mg、Cu、Fe三种金属的性质时进行了如图所示实验。
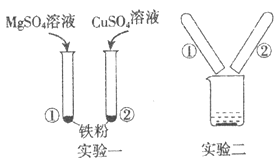
(1)实验一中的现象是________________。
(2)将实验一反应后的所有物质倒入烧杯中,充分反应后过滤,滤液中可能含有的溶质的组合有:_____________。
A. FeSO4 B. CuSO4、FeSO4 C. MgSO4、Fe2(SO4)3
D. MgSO4、FeSO4 E. MgSO4、CuSO4 F. MgSO4、CuSO4、FeSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】品吸潮和吸氧后容易变质,为了延长食品保质期,可采取以下不同的方法。
(1)泡沫铁粉是一种新型的食品干燥剂和保鲜剂,当它露置于空气中,一段时间后会变成铁锈,为检验某泡沫铁粉是否还有效,可向其中滴加盐酸,若看到________现象,说明还有效。
(2)硅胶也是一种干燥剂,其主要成分是SiO2·nH2O,其中Si元素的化合价为_______。
(3)山梨酸钾(C6H7KO2)是国际粮农组织和卫生组织推荐的高效安全的防腐保鲜剂。山梨酸钾中钾质量分数的计算式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用能源、节约能源、保护环境是我们大家共同关注的社会问题。
(1)海底埋藏着大量的“可燃冰”,可成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为_________________。
(2)人们常利用煤燃烧反应产生的能量来做饭、取暖。下列有关说法正确的是_________。
A. 化学反应过程中都会发生放热现象
B. 在化学反应中只有燃烧反应才能放出热量
C. 在当今社会,人类需要的大部分能量都是由化学反应产生的
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中蕴藏着许多化学知识。
(1)下列用品所使用的主要材料,属于有机合成材料的是_______。(填序号)。

(2)山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的________来止痒。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图像中,能正确反映对应变化关系的是
|
|
|
|
A. 向一定量的稀盐酸中加入氧化铁 | B. 向一定量的氢氧化钠溶液中滴加稀盐酸 | C. 向一定量的硫酸铜溶液中加入铁粉 | D. 向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为氯化铵和氯化钠在不同温度时的溶解度。下列说法正确的是( )
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl 溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
A. 20 ℃,氯化钠饱和溶液的溶质质量分数为36%
B. 由表中数据可知,溶解度受温度变化影响较大的物质是氯化钠
C. 氯化钠与氯化铵溶解度相等的温度在10 ℃~20 ℃之间
D. 50 ℃时,100 g水中加入50.0 g氯化铵配成溶液,再冷却到20 ℃,能够析出13.2 g固体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,不属于复分解反应的是
A. MgCl2+2NaOH=Mg(OH)2↓+2NaCl
B. Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
C. 2CuO+C![]() 2Cu+CO2↑
2Cu+CO2↑
D. CaO+2HCl=CaCl2+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】某化工厂的废水中含有亚硫酸钠(Na2SO3),若直接排放会造成污染。化学兴趣小组对该厂的废水处理设计了下图所示的实验方案:

(提示:Na2SO3 + CaC12 = CaSO3↓ + 2NaCl;CaC12不与废水中的其它杂质反应)
(1)氯化钙的相对分子质量是_________。
(2)反应生成亚硫酸钙沉淀的质量为_________g。
(3)求废水中亚硫酸钠的质量分数为_________(写出计算过程,结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】早在1754年,英国化学家布莱克就发现了一种重要的气体。他曾这样记载:
①灼烧白垩后质量减轻44%,说明有气体从中放出;该气体固定在白垩中,所以它是“固定空气”。②“固定空气”能被熟石灰吸收,生成不溶于水的白垩。③蜡烛在“固定空气”中不燃烧。④麻雀在“固定空气”中会窒息而死。请回答下列问题:
(1)布莱克发现的“固定空气”是_________。
(2)白垩、石灰石、大理石与_________(填生活中的一种物质)等,主要成分相同。
(3)写出资料①、②中有关反应的化学方程式:________、_________。
(4)从资料④可知,进入久未开启的地窖、干涸的深井时,首先要_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com