
科目: 来源: 题型:
【题目】自动充气气球因使用方便,无需其它充气器材而逐渐得以推广。某化学兴趣小组对自动充气气球进行了如下探究。

(查阅资料)①自动充气气球的结构如图所示,气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
②氯化银是一种白色沉淀且不溶于稀硝酸。
(1)探究液体包的成分:
取液体包中的少量溶液分别放于两只于试管中,在其中一只试管中加入锌粒产生气泡,另一只试管中滴加硝酸银溶液,产生白色沉淀,继续滴加稀硝酸沉淀不溶,则小组同学证明液体包中装的是________,写出该液体与锌粒反应的化学方程式____________。
(2)探究白色粉末成分:
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠。
(设计并进行实验)实验一:完成下表
操作步骤 | 现象 | 结论 |
甲同学的猜想不正确 |
实验二:按下图的实验装置,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的烧瓶中注入等体积、足量的稀盐酸,并测量生成二氧化碳的体积,记录如下表:

实验编号 | 锥形瓶内物质 | 最终得到CO2 体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 0.8 | V1 |
② | 碳酸钠 | 0.8 | V2 |
③ | 白色粉末 | a | V1 |
(3)实验装置中植物油的作用是___;表中a= ___;V1____V2(填“>”、“<”或“=”)。
(分析并得出结论)(4)分析上表中数据得出结论:白色粉末的成分是__________,依据是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学把干燥、纯净的氯酸钾和二氧化锰的混合物31.5g装入大试管中,加热制取氧气,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 28.9 | 26.3 | 23.7 | 21.9 | 21.9 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为___________g;
(2)把剩余固体加入足量的水溶解过滤得到滤液55g(二氧化锰难溶于水),计算滤液中溶质的质量分数是多少?(精确到0.1%) ___________
查看答案和解析>>
科目: 来源: 题型:
【题目】“五一”长假,小明和化学兴趣小组的同学去实验室做实验,请你根据下图所示的实验过程,回答问题:
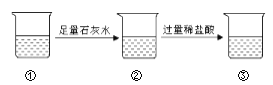
(1)烧杯①加入石灰水后发生反应的化学方程式为_______________________________。
(2)烧杯②中滴加稀盐酸至过量会看到沉淀消失有气泡冒出,产生气泡的化学方程式为_____________,最终烧杯③中的溶质是____________________(写化学式)。
(3)烧杯③的废液直接倒入下水道会造成水质污染。请你帮助小明选择下列物质中的一种加入烧杯③的废液中,完全反应后再倒掉废液就不再对水质存在污染。你选择的是_____(填字母序号)。
A.石蕊溶液 B.过量的氢氧化钠溶液 C.适量的氢氧化铜 D.过量的大理石
查看答案和解析>>
科目: 来源: 题型:
【题目】国际上提倡向中国人学习用铁锅炒菜。工业上常用赤铁矿(主要成分氧化铁)和一氧化碳冶炼生铁,该反应的化学方程式为_____。用铁锅炒菜时,油锅中的油不慎起火,只需一个简单的操作,火就熄灭了,该操作是____,其灭火的原理是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图象能正确反映其对应的实验操作的是
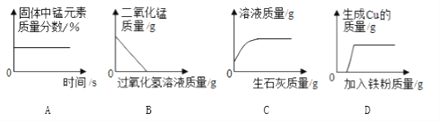
A. 加热一定量的高锰酸钾固体
B. 向一定量的MnO2中加入H2O2溶液
C. 向一定质量的饱和石灰水中加入生石灰
D. 向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是

A. 升高温度,可使甲的饱和溶液变为不饱和溶液
B. 50℃时,可以配制溶质质量分数是20%的乙溶液
C. 50℃时分别在100 g水中加入20 g甲、乙充分搅拌,再同时降温至20℃,甲、乙溶液均变为饱和溶液
D. 20℃时乙溶液的溶质质量分数一定大于甲
查看答案和解析>>
科目: 来源: 题型:
【题目】无水溴化钙可用作阻燃剂、制冷剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:完成下列填空:
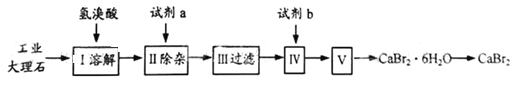
⑴上述使用的氢溴酸的质量分数为26%,若用47%的氢溴酸配置26%的氢溴酸,所需的玻璃仪器有玻璃棒、烧杯、_________ 和________ ;步骤I溶解中发生的化学反应方程式为___________。
⑵已知步骤Ⅲ的滤液中不含NH4+。步骤Ⅱ加入的试剂a是 _______,控制溶液的pH约为8.0,将Al3+、Fe3+分别转化成沉淀而除去,写出沉淀的化学式________、 __________。
⑶试剂b是_________ ,步骤Ⅳ的目的是 _______________________ 。
⑷步骤Ⅴ所含的操作依次是 _______________ 、____________ 、过滤。
⑸制得的溴化钙可以通过如下步骤测定其纯度:
①称取4.00g无水溴化钙样品;②溶解;③滴入过量Na2CO3溶液,充分反应后过滤;④洗涤、________;⑤称量得到1.88g碳酸钙。
a.请将上述步骤④补充完整,检验碳酸钙沉淀已经洗涤干净的方法是:取最后一次洗涤液,滴加__________溶液,若无白色沉淀产生,则已洗干净。
b.依据测定数据,请计算出样品中溴化钙的质量分数为________。(写出计算过程)。
c.若上述测定溴化钙纯度的实验操作规范,但测定结果偏低,其原因可能是 ________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】以冶铜工厂预处理过的污泥渣(主要成分为CuO和Cu)为原料制备CuSO4晶体的流程如下:
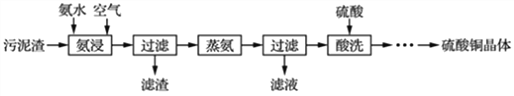
(1) 氨浸过程中加入氨水后,持续通入空气,将铜转化成Cu(NH3)4(OH)2,写出发生反应的化学方程式: _____________________;通入的空气除了参与反应外,还有另一个作用是___________________。
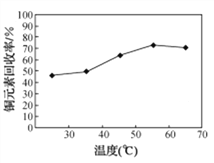
(2) 氨浸过程中,铜元素回收率随温度变化如图所示。则氨浸过程中,反应温度最好控制在______ ℃,温度过高铜元素回收率降低的原因是____________________________。
(3) 蒸氨过程的生成物均是两种元素组成的化合物,则除氨和水外,另一产物的化学式为________。
(4) 该流程中可循环利用的物质是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了验证一氧化碳的性质,某实验探究小组通过查阅资料得知:固体草酸(H2C2O42H2O)受热可分解,其化学方程式是:H2C2O42H2O=3H2O↑+CO2↑+CO↑,可制得一氧化碳气体。根据下图进行实验:
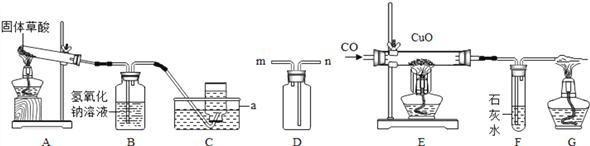
(1)写出仪器a的名称 _________。
(2)若在装置A的试管口添加一团棉花用来制取氧气,写出反应的化学方程式___________,若用D装置收集氧气,氧气应从______(填m或n)端进入,检验氧气已经收集满的方法:_________。
(3)若要验证草酸分解产物中有二氧化碳和水蒸气生成,将生成的混合气体依次通过 ______和__________(填试剂名称),即可验证。
(4)在上述验证CO性质的实验中,应先点燃 _______处酒精灯(选填“E”或“G”),实验中观察到装置E中的现象: _____________。
(5)上述CO的制备与性质实验中,说明CO具有的性质有: ________ 。
A.还原性 B.可燃性 C.毒性 D.难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。
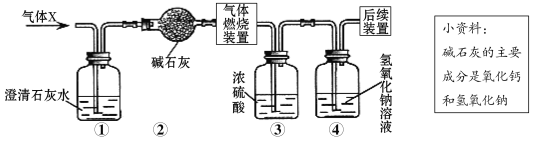
下列关于气体X成分的分析中,错误的是( )
A.一定没有二氧化碳 B.可能含有甲烷和氢气
C.可能只有甲烷 D.可能含有氢气和一氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com