
科目: 来源: 题型:
【题目】根据下列表格中的信息回答问题。
A.过氧化氢溶液和二氧化锰混合 | B.加热高锰酸钾 | C.硫燃烧 |
|
|
|
(1)A、B实验中数据变化关系与对应图像相符的是____(填字母序号)。
(2)A中反应的文字表达式是____。
(3)C中可观察到硫在氧气中燃烧,发出____火焰,生成______气味的无色气体,此反应的文字表达式___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中的①和②是氟元素和钙元素在元素周期表中的信息,A、B、C、D是4种粒子的结构示意图。请完成下列空白。

(1)钙元素的相对原子质量为_______,氟元素的原子序数为_______;D中的x为_______。
(2)①和②是不同种元素,它们的最本质的区别是_______________________________。
(3)A、B、C、D结构示意图中,属于同种元素的粒子是_______(填字母)。
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_______(填字母)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学语言是学习化学的重要工具。
(1) 完成下列化学反应的符号表达式:
化学反应 | 符号表达式 |
红磷在氧气中燃烧 | ①__________________ |
木炭在氧气中燃烧 | ②_____________ |
(2)填写化学符号或化学符号表示的含义:
内容 | ③ | ④ | ⑤ | |
化学符号 | 2Fe | ____ | ______ |
|
表示含义 | ______ | 1个钠离子 | 1个氯离子 | 最外层电子数为____,属于____元素(填“金属”或“非金属”)。 |
查看答案和解析>>
科目: 来源: 题型:
【题目】1911年卢瑟福为探索原子的内部结构进行了“α粒子散射实验” 用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔。实验时发现(示意图如下):
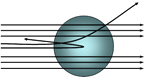
![]()
(1)大多数α粒子能穿透金箔而不改变原来的运动方向;
(2)一小部分α粒子改变了原来的运动方向;
(3)有极少部分α粒子被弹了回来。
下列由该实验分析得出的认识中,正确的是
A. 原子核不带电 B. 原子是实心的球体
C. 原子质量主要集中在原子核 D. 原子核由质子和中子构成
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钴(Co)在国防工业中有重要应用。某矿石中含钻的氧化物(CoO、Co2O3)研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件。
(1)写出下列化合物中Co元素的化合价:CoO_________,Co2O3______________。
(2)酸浸时钴的氧化物发生如下反应:
反应I CoO+H2SO4===CoSO4+H2O
反应Ⅱ 2Co2O3+4H2SO4===4CoSO4+O2↑+4H2O
反应Ⅲ Co2O3+2H2SO4+Na2SO3===2CoSO4+2H2O+Na2SO4
①反应后溶液中含钴元素的微粒是_________ (填化学符号)
②已知反应前矿石中CoO的质量为ag,Co2O3的质量为bg,则理论上可以生成CoSO4____g(用含a、b的式子表示)
(3)为探究最佳提取条件,将矿石在一定条件下酸浸4小时,测量钴元素的浸出率部分数据如下:
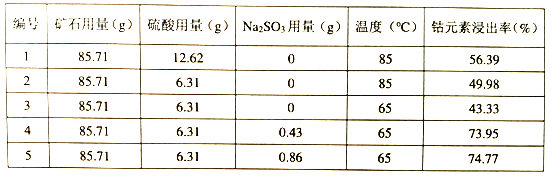
①本实验研究了哪些因素对钴元素浸出率的影响__________________________________;
②根据上表数据,其他条件不变,温度升高,钴元素的浸出率___________________________;
③工业生产中采用实验______________(填编号)的提取条件更合理。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温为25℃时,某小组用无水氯化铜粉末制备氯化铜大晶体,制备过程如下:
步骤I:查阅资料,得到氯化铜溶解度数据如下
温度(℃) | 0 | 20 | 25 | 40 | 50 | 60 | 80 |
溶解度(g) | 69.2 | 74.5 | 76.4 | 81.8 | 85.5 | 89.4 | 98.0 |
步骤Ⅱ:配制少量CuCl2热饱和溶液,冷却结晶,得到晶种。
步骤Ⅲ:把晶种悬挂在新配制的CuCl2热饱和溶液中,室温下静置数天,形成大晶体。
步骤Ⅳ:取出大晶体,处理剩余的溶液(母液)。
根据以上信息,回答下列问题:
(1)用20mL蒸馏水(密度约为1g/mL)配制50℃的氯化铜饱和溶液。
①计算需称取CuCl2的质量是_______g。
②将称取的CuCl2固体和20mL水倒入烧杯中,_______________(填操作名称),直至固体完全溶解。
(2)母液中Cu2+属于重金属离子,随意排放将导致环境污染。下列方法可用于母液处理的是__________。
A.收集母液于敞口容器中,用报纸包住容器口,待水分自然蒸干后保存所得固体
B.向母液中加入适量AgNO3,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
C.向母液中加入适量NaOH,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
(3)若用铁粉置换出母液中的铜,100g母液需要铁粉的质量至少是_____________ g(只列计算式,已知CuCl2的相对分子质量为135)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下:
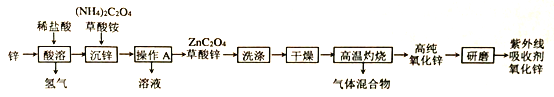
(1)推测草酸的化学式是____________;
(2)“沉锌”过程中发生复分解反应,反应的化学方程式是_______________________________
(3) “操作A”的名称是______________ 实验室常用的研磨仪器是_____________;
(4)“高温灼烧”时草酸锌分解,反应的化学方程式是______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室制备气体的部分装置:
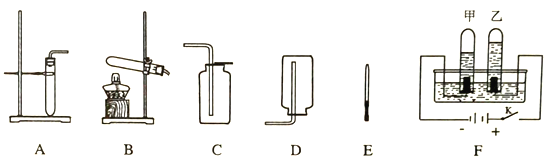
(1)加热混有二氧化锰的氯酸钾制备一瓶氧气用于性质实验。
①该方法制得O2的化学方程式是______________________________________。
②可选用_____和________(填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后_____________________,观察到有气泡冒出,说明装置气密性良好。
(2)氢气被认为是理想的清洁、高能燃料。
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用_______(填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器——>检查装置气密性——>装入药品制备氢气——>_____________——>点燃。
②电解水也可制得H2。装置如图F,_________管中产生的是氢气。
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_________。
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是几项基本实验操作的示意图
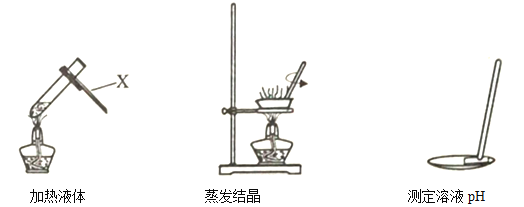
(1)仪器X的名称是____________;加热液体时,液体体积不能超过试管容积的_______;
(2)蒸发结晶时,用玻璃棒搅拌,当_______________________,停止加热;
(3)测定溶液pH时,用玻璃棒蘸取待测液滴到pH试纸上,______________,读出pH。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案,不能达到相应实验目的的是
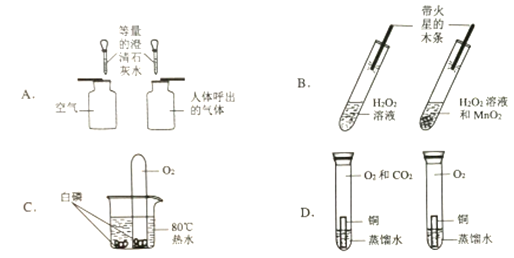
A. 比较空气与人体呼出的气体中CO2含量 B. 探究MnO2能否加快H2O2分解
C. 验证燃烧需要温度达到着火点 D. 探究CO2对铜生锈是否有影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com