
科目: 来源: 题型:
【题目】紫薯因富含硒元素被誉为“抗癌大王”.硒元素的部分信息如图所示.下列做法不正确的是( )

A.硒是一种非金属元素
B.硒元素的质子数为34
C.硒的原子结构示意图中x=18
D.在化学反应中,硒原子容易失去2个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是一些微观粒子结构示意图,有关叙述正确的是( )
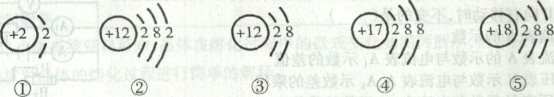
A.②⑤为同一周期元素的原子 B.①②的元素在周期表的同一.族
C.①③④⑤是具有相对稳定结构的原子 D.②③属于同种元素的同种粒子
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据如图所示的实验装置图填空。
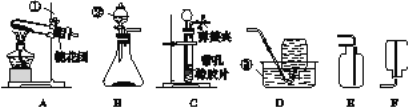
(1)指出图中标有数字的仪器的名称:①__________,②____________,③____________。
(2)在实验室用高锰酸钾制氧气时,试管口的棉花团的作用是___________________,
写出反应的文字表达式:________________。
(3)当实验室中用B装置制取氧气时,仪器②的作用是___________、___________,该反应的文字表达式为________________。
(4)在实验室制取并收集二氧化碳可选用______________(填序号)装置,写出实验室制取二氧化碳的文字表达式:____________。
(5)检查装置B气密性的方法是_________,装置C相对于装置B在操作方面的优势为_______。
(6)某位同学设计了如图所示五套制取二氧化碳的装置,其中能达到装置C操作优势的是________(填序号)。
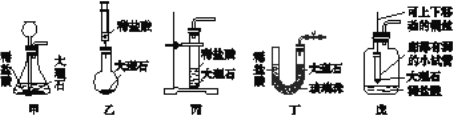
(7)在实验室中常用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体。甲烷是一种无色无味、密度比空气小、极难溶于水的气体, 则制取并收集甲烷,应该从图A~F中选择的发生装置是________(填序号),收集装置是______________(填序号)。
(8)若用如图所示装置进行向上排空气法收集氧气的实验,气体应从_____(填“a”或“b”)端导入。
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下列实验图回答问题。

(1)仪器a的名称是__________。
(2)上述三个实验中,水对实验仪器起到安全保护作用的是________(填字母)。
(3)C实验中发生反应的文字表达式是______________________。
(4)对于B实验,小李同学进行了改进与创新,实验过程如图所示:

上图改进实验与B实验相比,明显的优点是_____________________ (写一条即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在括号内填入物质名称。
(1)(_____)+(_____)![]() 二氧化硫
二氧化硫
(2)(_____)+(_____)![]() 五氧化二磷
五氧化二磷
(3)高锰酸钾![]() (______)+(______)+(_____)
(______)+(______)+(_____)
(4)过氧化氢![]() (_____)+(_____)
(_____)+(_____)
(5)二氧化碳+水―→(_____)
以上反应属于化合反应的是______________(填序号,下同),属于分解反应的是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人们为了揭示原子结构的秘密,经历了漫长的探究过程。自1897年汤姆逊发现电子并提出类似“西瓜”的原子模型,1911年物理学家卢瑟福等人探索原子的内部结构时又进行了下面的实验。他们在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现:①大多数α粒子能穿透金箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运动方向;③有极少数α粒子被弹了回来。

请你根据对原子结构的认识,分析出现上述现象的原因。
(1)现象①:_______________________________。
(2)现象②:______________________________。
(3)现象③:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】原子的电子层最多可达到7层,以n代表电子层数,每层的电子排布是有一定原则的:①每层最多容纳的电子数为2n2个;②最外层不超过8个(第一层为最外层时不超过2个);③次外层不超过18个,倒数第三层不超过32个。
依据此规律,画出的硒原子(![]() Se)和碘原子(
Se)和碘原子(![]() I)的结构示意图如图所示。
I)的结构示意图如图所示。
硒原子: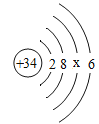 碘原子:
碘原子: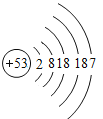
(1)硒原子的结构示意图中x=________。
(2)碘原子的化学性质与下列________(填字母)的化学性质相似。
A.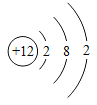 B.
B. C.
C.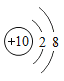 D.
D.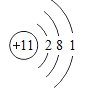
查看答案和解析>>
科目: 来源: 题型:
【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。可以说镍行业发展蕴藏着巨大的潜力。
Ⅰ制备草酸镍
工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍(NiC2O4)。
根据下列工艺流程图回答问题:
(资料卡片1)
(1)过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢具有强氧化性,所以常作为氧化剂、漂白剂和消毒剂。
(2)氧化反应可以从元素化合价升降的角度进行物质所含元素化合价升高的反应就是氧化反应。
(3)金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。

(1)“酸溶”之后的滤渣中含有的金属是_______________。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式_________________________。
(3)加H2O2时,温度不能太高,其原因是_______________________。若H2O2在“酸溶”步骤即与盐酸同时加入,则与原方案相比滤液中会增加的金属离子是Cu2+和_______(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式____________。
Ⅱ制备镍粉
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3yNi(OH)2zH2O,并利用其制备镍粉,过程如下:

(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O ![]() NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体已洗涤干净的试剂是____________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是_________(填名称)。
Ⅲ 测定碱式碳酸镍晶体的组成
为测定碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)组成,某小组设计了如下实验方案及装置:

(资料卡片2)
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3
(3)碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理)
8)实验过程中步骤⑤鼓入空气的目的是__________________。
(9)计算3.77g碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)中镍元素的质量_________(写出计算过程,计算结果准确到小数点后两位)。
(实验反思)
(10)另一小组同学在实验中发现,实验结束后,称得装置B中残留固体质量明显偏大,老师带领全组同学经过仔细分析后发现,这是由于该组同学加热时在酒精灯上加了铁丝网罩,温度过高所导致。请问该组同学称得的残留固体中镍元素的质量分数可能是__________。
A.70.08% B.75.88% C.78.67% D.79.58%
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室中则以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O,工艺流程如下:
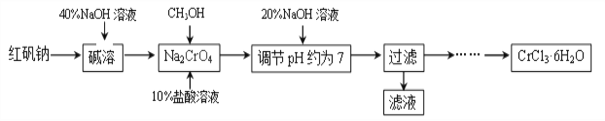
已知:a.CH3OH+10HCl+2Na2CrO4 2CrCl3+4NaCl+CO2 ![]() +7H2O;
+7H2O;
b.Cr(OH)3是一种难溶于水的碱;
c.CrCl3·6H2O不溶于乙醚,易溶于水、乙醇。
(1)在“调节pH约为7”的步骤中,测定溶液的pH可使用____________。请写出该步骤的反应原理_____________(用化学反应方程式表示)。
(2)“碱溶”步骤中所加40%NaOH溶液不宜过量太多的原因是_________________。
(3)请你补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得固体溶解于盐酸,通过蒸发浓缩、________、过滤、洗涤、低温干燥,得到CrCl3·6H2O。下列物质中可以用来洗涤CrCl3·6H2O的是_________(填序号)。
A.水 B.盐酸 C.乙醇 D.乙醚
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置回答问题。

(1)请写标号仪器的名称:a______________。
(2)用高锰酸钾为原料制取较纯净的氧气可选用的装置组合为__________(填字母,下同),发生装置应作的改进是_____________,反应的化学方程式为_________________。
(3)实验室用锌粒和稀硫酸制取氢气,反应的化学方程式为__________________,可选用的发生装置是_______,若用F装置收集氢气,气体应从________端通入(填“b”或“C”)。
(4)已知:氨气极易溶与水,且与水反应生成氨水,氨气难溶于氢氧化钠溶液。
①碳酸氢铵是一种常用的氮肥,受热易分解,生成氨气、水、二氧化碳,该反应的化学方程式为__________。
②检验碳酸氢铵分解后的气体中含有二氧化碳,下列方案可行的是___________(填序号)。
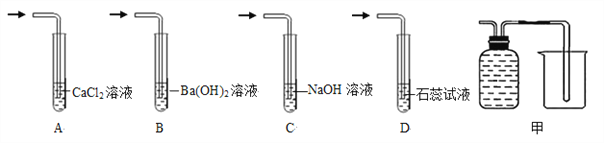
③甲图可用于分离碳酸氢铵分解产生的气体并回收氨气,广口瓶中应盛放的液体是_________,装置需要作怎样的改进才能达到实验目的?请用铅笔在答题卡相应位置画出。 _________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com