
科目: 来源: 题型:
【题目】下列表达错误的是
A.硫酸铵的化学式:(NH4)2SO4
B.氧原子的结构示意图: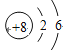
C.铁和盐酸反应的化学方程式:2Fe+6HCl=2FeCl3+3H2↑
D.锰酸钾中锰元素的化合价为+6价:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种石灰石样品的成分是CaCO3和SiO2。课外小组同学将88.8 g盐酸加入到35 g石灰石样品中(已知SiO2不与盐酸反应),盐酸与碳酸钙恰好完全反应,收集的气体质量为8.8g,(以下计算均需写出计算过程,假设实验过程中溶液损失忽略不计)
(1)写出盐酸与碳酸钙反应的化学方程式:_______
(2)计算35g样品中CaCO3的质量_________。(写出计算过程)
(3)反应后过滤,得到CaCl2溶液,将此溶液配成10%的CaCl2溶液,①计算:这时还需要向滤液中加入水多少克?②量取:量取一定量体积的水,倒入氯化钙溶液的烧杯中。③混匀:用玻璃棒搅拌,使___。
查看答案和解析>>
科目: 来源: 题型:
【题目】生命的孕育和维系需要水,科学研究离不开水.请你完成下列探究。
(1)探究一:用水作溶剂.在盛有5mL水和5mL汽油的两只试管中分别加入1~2小粒高锰酸钾,可观察到的现象是______,结论:同一种物质在不同溶剂中的溶解性不同。该实验量取5ml液体需要用到的仪器是_______和________
(2)探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容。
两种白色固体 | 主要操作、现象和结论 |
_______ | ____ |
(3)探究三:溶质在水中的溶解与结晶。
(查阅资料)熟石灰与碳酸氢铵、氯化铵混合研磨,生成有刺激性气味的气体;碳酸氢铵、碳酸氢钠与稀盐酸反应生成无色无味的气体;20℃时,五种物质的溶解度如下表。
物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 | Na2CO3 |
溶解度/g | 36.0 | 21.0 | 37.2 | 9.6 | 21.5 |
相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变。
(提出问题)20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃)。析出的晶体是什么?
(设计实验)设计方案,并进行实验。
①取少量晶体与熟石灰粉末混合、研磨,无明显现象,说明该晶体不可能是_______。
②取少量晶体于试管中,加入_______,现象为生成无色无味的气体。
③(实验结论)析出的晶体是_______。
④(实验拓展)析出晶体的原因是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制取氧气时,发现制得的气体有刺激性气味,于是在老师的指导下对该气体成分进行探究。
(提出问题) 氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
(查阅资料)
①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
(1)(猜想与假设)
猜想一:该气体为O2;猜想二:该气体为Cl2;猜想三:该气体为________。
(2)(实验探究)
序号 | 实验操作 | 实验现象 | 实验结论 |
① | 小丽用排水集气法收集A、B两瓶气体,将带火星木条伸入A中;湿润的淀粉碘化钾试纸伸入B中 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色 | 猜想___成立 |
② | 小岚用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中 | C中带火星木条复燃,D中淀粉碘化钾试纸_______ | 猜想三成立 |
(3)(反思与评价)①小涛认为小丽的结论不正确,原因是_____。
②还可用蓝色石蕊试纸检验Cl2的存在。
(4)(拓展应用) MnO2不仅能作催化剂还可以作反应物,实验室通常用MnO2与浓盐酸共热制取Cl2,同时生成+2价的锰的氯化物和另一种常见的化合物,请写出该反应的化学方程式:___________。
(5)实验室除了用氯酸钾制取氧气,还可用高锰酸钾或过氧化氢溶液制取氧气,请分别写出实验室用高锰酸钾、过氧化氢溶液制取氧气的化学方程式: ___________、______________;
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)如图为铁元素在元素周期表中的信息,亚铁离子(写出离子符号____)的核外电子数为___。
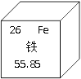
(2)健康人体内,总量4~5g的铁元素主要以____(选填“单质”、“化合物”)形式存在,缺铁会患上___(填字母)。
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
(3)(实验一)
兴趣小组通过下图实验研究铁的冶炼
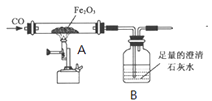
(资料1)已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
![]()
(资料2)实验研究表明:该实验得到的是四氧化三铁与铁粉的混合物
①试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式_______;
②实验一段时间后,观察到A处现象是___; B处反应的方程式____;小明将所得的黑色固体物质放入足量的稀硫酸中,发现有少量气泡。写出产生气泡反应的化学方程式___,说明黑色固体物质____(填字母)。
a.不含铁 b.一定全部是铁 c.含有铁
(4)(实验二)兴趣小组用下图实验研究实验一所得黑色粉末中单质铁的质量分数
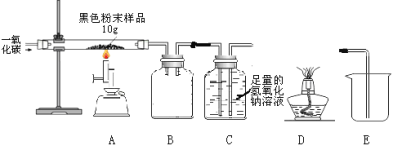
(资料3)氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,且吸收能力比石灰水强。
①从安全与规范的角度考虑,装置C后面应连接____(选填装置序号D或E),B装置的作用是_____。
②铁与四氧化三铁的混合物10 g充分反应后,玻璃管中剩余固体(单质铁)的质量为8.4g。请计算10 g黑色粉末中单质铁的质量分数______。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学就在我们身边,与我们的生活有着密切的联系。
(1)改善居民生活环境,提高居民生活质量,从环保角度看,你认为下列行为不利于空气质量改善的是___(填序号)。
①居民燃煤取暖 ②退耕还林 ③燃放烟花爆竹 ④焚烧秸秆
(2)某同学洗衣服,手抓洗衣粉放到水中时,有发热的感觉,说明洗衣粉溶于水____(填“放出”或“吸收”)热量。
(3)在生煤火炉时,可点燃木材来引燃煤,是因为______。
(4)根据如图某抗酸药的包装示意图,回答下列问题。

①图中标示的物质中,属于有机合成材料的是_____;
②淀粉属于______(填字母序号)
A.蛋白质 B.糖类 C.油脂 D.维生素
③图中塑料包装废弃后可用于微型化学实验,其优点是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,下列说法错误的是( )
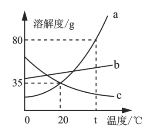
A. t℃时,将50g a物质加入到50g水中充分搅拌,可得到90g a的饱和溶液;
B. 将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c;
C. a中含有少量b,可用冷却a的热饱和溶液的方法提纯a;
D. a、b、c三种物质均属于易溶物质。
查看答案和解析>>
科目: 来源: 题型:
【题目】锌是人体健康所必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫力功能低下。市售的葡萄糖酸锌口服液对治疗锌缺乏症具有较好的疗效。如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:

请计算
(1)葡萄糖酸锌的相对分子质量为___;
(2)葡萄糖酸锌中碳、氧元素的质量比为___;
(3)葡萄糖酸锌中锌元素的质量分数为___.(精确到0.01%)
(4)某患者除正常饮食吸收锌元素外,还需服用该品牌葡萄糖酸锌口服液。若治疗一个疗程还需要补充104mg锌元素,而这些锌有75%来自于该口服液,则患者共需要服用___支葡萄糖酸锌口服液?
查看答案和解析>>
科目: 来源: 题型:
【题目】在老师的指导下,同学们进行了有趣的化学实验探究:
一、测定空气中氧气含量
图1所示的是小亮同学用红磷在空气中燃烧的测定方法.过程是:
第1步:将集气瓶容积划分为五等份,并做好标记.
第2步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第3步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.请回答下列问题:
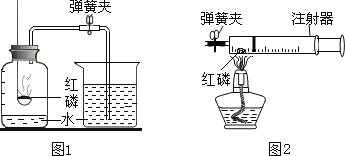
①第2步红磷燃烧时的现象_______________,化学反应表达式____________
②实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是_________.
A、集气瓶底部的水占了一部分体积
B、红磷过少
C、红磷没有燃烧完就急着打开了止水夹
③小博同学对实验进行反思后,提出了改进方法(如图2所示),小博在正式开始实验前,夹紧弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处.该操作的主要目的是_________,你认为改进后的优点是_________
二、小余阅读课外资料得知:双氧水分解除了用二氧化锰(MnO2)还可用氧化铜(CuO)等物质作催化剂,于是他对氧化铜产生了探究兴趣.
(提出问题)氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
(设计实验)小余以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)
实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
① | 1.2g | / | |
② | 1.2g | CuO 0.5g | |
③ | 1.2g | MnO20.5g |
①上述实验应测 量的“待测数据”是时间__________.
②若实验②比实验①的“待测数据”_________(填“大”或“小”),说明氧化铜能加快氯酸钾的分解.
③将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g黑色粉末,这样做的目的是________,小余同学认为氧化铜肯定是氯酸钾分解的催化剂,但小淳同学对此提出了异议,小淳同学设计了如下实验:将第二次精确称量得到的0.5g黑色粉末和1.2g氯酸钾混合放入试管中,加热,伸入带火星木条,发现木条很快复燃.小淳同学这样做目的是________,
(预期结论)氧化铜也能作氯酸钾的催化剂.
(评价设计)你认为小余设计实验③和实验②对比的目的是__________; 写出实验②反应的表达式______
查看答案和解析>>
科目: 来源: 题型:
【题目】图Ⅰ是小红进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ。

实验操作:
a:向B、C、E三支试管中分别加入5 mL的蒸馏水,各滴入1滴~2滴无色酚酞溶液,振荡,观察溶液颜色。
b:在A、D试管中分别加入2 mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
分析讨论:
(1)E试管中放有酚酞溶液的目的是 __________________。
(2)进行操作b时观察到的现象是 ___________________。
(3)由此可以得到的实验结论是①________________;②_________________。
(4)对比改进前的实验,改进后的实验的优点是 ___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com