
科目: 来源: 题型:
【题目】机动车排放的尾气是空气的重要污染源,其成分之一是 NO。某化学兴趣小组的同学在查阅资料后得知:①NO常温下是一种无色、难溶于水的气体,它的密度比空气略大;②NO常温下能与氧气迅速反应,生成红棕色的NO2气体:2N0+ O2 =2 NO2;③实验室常用铜与稀硝酸反应制取NO: 3Cu+ 8HN03(稀)=3Cu(N03) 2+2N0↑+4X.
请根据以上信息完成下列问题:
(1)物质x的化学式为____________
(2)若选择合适的装置来制取并收集NO气体,你选择的发生装置是____________(填字母代号,下同),收集装置是__________。
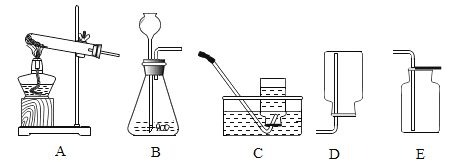
(3)某化工厂准备生产Cu(N03)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HN03(稀)=3Cu(N03)2 +2N0↑+4X
方案二:2Cu+ O2![]() 2CuO; CuO+2HN03= Cu(N03) 2+H20
2CuO; CuO+2HN03= Cu(N03) 2+H20
从经济效益的角度考虑,你选择的方案及理由是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用如图所示装置测定空气中氧气含量,实验步骤如下:
①在集气瓶内加入少量水,将水面上方空间分为5等份,并作好标记;
②在带橡皮塞和导管的燃烧匙内装入过量的红磷,将导管上的止水夹夹紧,在酒精上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞;
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
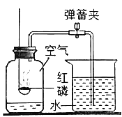
(1)该实验中红磷需稍过量,目的是_____,该反应的符号表达式(或化学方程式)为_________;
(2)步骤②中点燃红磷后,立即伸入集气瓶内并塞紧橡皮塞的目的是__________;
(3)步骤③中打开止水夹后观察到的现象是____________;
(4)若将红磷换成炭粉,该实验不能成功,原因是____________;
(5)该实验完毕,若进入集气瓶的水不到瓶内空气体积的五分之一,你认为原因是:____________(答一点即可);
(6)该实验得出氮气的化学性质是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
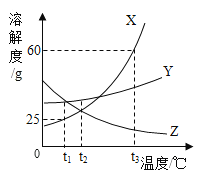
(1)X中含有少量Y,应采用____________的方法提纯X。
(2)t2℃时,三种物质的溶解度的大小关系是__________
(3)t3℃时,溶质质量分数为25%的x溶液降温到t1℃,所得溶液中溶质质量分数是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制取气体的装置。回答下列问题:
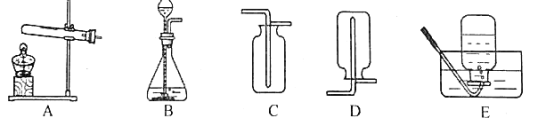
(1)用高锰酸钾制氧气导管口要放____,目的是_____,此反应的符号表达式(化学方程式)为__________。
(2)可用C装置收集氧气,因为_____,此时导管要接近瓶底的原因是____,判断C中集满氧气的方法是______.
(3)可用E装置收集氧气,因为氧气_______,用此收集方法判断氧气集满的现象是____,若收集的氧气不纯,可能的原因是______。实验后,要先把导管移出水面,目的是______。
(4)已知颗粒状的锌和稀硫酸在常温下反应即可制得氢气,可为其选择的发生装置是(填序号)_______,收集装置是______。(已知氢气是种密度最小的气体,难溶于水)
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。请回答:
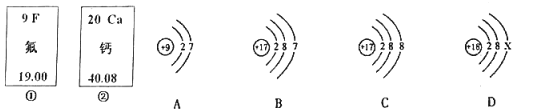
(1)氟原子的相对原子质量为________,钙元素的原子序数为___________;
(2)X= ____________
(3)A、B、C、D属于同种元素的粒子是(填序号)______________;
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号)__________.
查看答案和解析>>
科目: 来源: 题型:
【题目】用适当的化学符号填空:
(1)①2个氮分子__________;
②氧化铁中氧元素的化合价为-2价____________;
③相对分子质量最小的氧化物____________;
④构成食盐的微粒有_____________.
(2)在给定的符号:![]() 中数字“2”表示分子个数的是_____(填序号,下同),表示分子中原子个数的是_____,表示离子所带电荷数的是_____.
中数字“2”表示分子个数的是_____(填序号,下同),表示分子中原子个数的是_____,表示离子所带电荷数的是_____.
(3)从给定化合价的![]() 四种元素中,选择适当的元素按要求写出有关物质的化学式:单质___;氧化物______;化合物________(不属于氧化物).
四种元素中,选择适当的元素按要求写出有关物质的化学式:单质___;氧化物______;化合物________(不属于氧化物).
查看答案和解析>>
科目: 来源: 题型:
【题目】水是重要的自然资源,也是生命之源。
(1)水分子中氧原子的结构示意图为____________
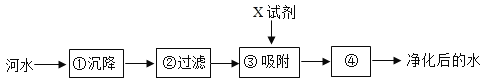
(2)自来水厂净化水的主要步骤如上图所示,下列有关说法错误的是_______(填字母代号)。
A.步骤①②可以除去难溶性杂质
B.X试剂可以是活性炭
C.步骤④可用硫酸铜杀菌、消毒
D.步骤①中可加人明矾作絮凝剂
查看答案和解析>>
科目: 来源: 题型:
【题目】“配制一定质量分数的溶液”和“粗盐中难溶性杂质的去除”是初中化学的基础实验,请回答下列问题:
(1)“粗盐中难溶性杂质的去除”实验步骤:
①溶解称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。
②过滤。
③蒸发,请从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是________。
④计算产率得到精盐3.2g,则精盐的产率为__________(计算结果保留一位小数)。
(2)整个实验中至少要进行__________次称量。
(3)从海水中获胜得的粗盐,经过上述实验得到精盐属于__________(填“混合物”或“纯净物”)。
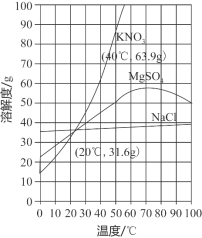
(4)根据如图所示溶解度曲线,40℃时,向装有50g水的烧杯中加入25gKNO3固体,充分搅拌后,所得溶液的溶质质量分数为_____%(精确到0.1%),将该溶液降温至20℃时,析出KNO3晶体的质量为____g。
(5)若用溶质质量分数为16%的KNO3溶液和蒸馏水配制100g溶质质量分数为10%的KNO3溶液,则需要取蒸馏水的体积为__________ml。
查看答案和解析>>
科目: 来源: 题型:
【题目】六水合硫酸镍(NiSO4·6H2O)是一种重要的工业原料。该物质为绿色易溶于水的晶体,在280℃时失去结晶水生成黄绿色无水物,当温度更高开始分解,释放出三氧化硫,变成氧化镍。该晶体可有含镍、铜、铁的电镀废渣为原料获得,主要流程如下:
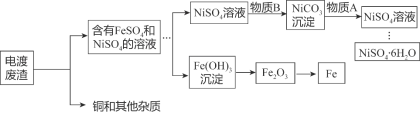
(1)由NiSO4溶液得到六水合硫酸镍晶体最好用加热浓缩,然后再降温结晶而不是蒸发结晶的原因____。
(2)电镀废渣中Fe与物质A发生反应的化学方程式为______________________________,该反应属于__________反应(填基本反应类型)。
(3)NiCO3沉淀转化为NiSO4溶液发生反应的化学方程式为____________________。
(4)该工艺流程还可制得Fe,214gFe(OH)3理论上能得Fe的质量为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人类每时每刻都离不开空气,没有空气就没有生命,也没有生机勃勃的地球。
(1)空气主要由__________(填物质名称)和氧气组成,此外,还含有少量的稀有气体等。
(2)空气中的各种成分广泛应用于多个领域,其中氧气可用于_________(填字母序号,下同),稀有气体可用于_________。
A.制造霓虹灯 B.医疗急救
(3)如图所示的装置可用于测定空气中氧气的含量。
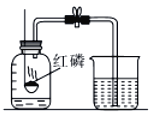
①请补全下列实验步骤。
a.按图示连接好装置;
b.________________;
c.在集气瓶内加入少量水,并将水面上方空间分为五等份,用弹簧夹夹紧胶皮管;
d.取足量红磷放入燃烧匙中,点燃后立即伸入瓶中,并把塞子塞紧;
e.待红磷熄灭并冷却至室温后,打开弹簧夹。
②红磷燃烧的现象是_____________,反应的文字表达式为________。
③冷却至室温后打开弹簧夹,水能进入集气瓶中的原因是_________________。
④若某同学在实验后得出结论:空气中氧气的体积约占1/5。能得出此结论的实验现象为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com