
科目: 来源: 题型:
【题目】今年3月22~28日是第28届“中国水周”,其主题为“节约水资源,保障水安全。”
(1)下列关于水的说法中,不正确的有________(填序号)。
①水是由氢元素和氧元素组成的化合物 ②清澈、透明的泉水是纯净物
③合理施用农药、化肥,以减少水体污染 ④将活性炭放入硬水中可使其软化
⑤洗菜、洗衣后的水用来浇花、冲洗厕所
(2)自然界中的水一般要净化后才能使用。吸附、过滤、蒸馏等三种净化水的操作中,单一操作相对净化程度最高的是________。
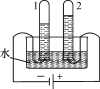
(3)电解水实验揭示了水的组成。如图实验中得到氧气的试管是________(填“1”或“2”)。
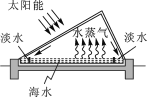
(4)海水淡化可缓解淡水资源匮乏的问题。如图为太阳能海水淡化装置示意图。
①水变成水蒸气的过程中,不发生变化的是________(填字母序号)。
A.分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会________(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如果用“”、“”分别表示两种不同的原子,如图所示的是某些气体粒子的示意图,根据其组成特点用字母回答:
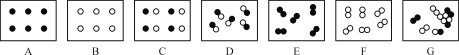
(1)属于纯净物的有________;其中属于单质的有________,属于化合物的有________;
(2)属于混合物的有________;
(3)由原子直接构成的纯净物有________;
(4)由分子构成的纯净物有________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)下表是元素周期表的一部分,请你根据下表回答问题:
3 Li 锂 6.941 | 4Be[来铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟[来 19.00 | 10 Ne 氖 20.18 |
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 29.95 |
(1)根据上表回答问题
①钠的相对原子质量是 。
②上表中,金属元素有 种。
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图。
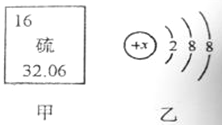
①该元素的原子的核电荷数为 ,该原子的最外层电子数为 。
②图乙所示粒子的符号为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
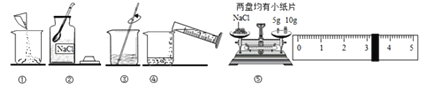
(1)用图中序号表示配制溶液的正确操作顺序 ;
(2)图②中用来取用NaCl的仪器是 ;
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为 g;
(4)NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数 (填“大于”、“小于”或“等于”)10%。
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列计算:
(1)向200g30%的A物质的水溶液中加入100g60%的A物质的水溶液,充分混合,所得溶液的溶质质量分数为_______。
(2)欲配制密度为1.31g/mL、溶质质量分数为20%的KNO3溶液1000g,需要水_______g
查看答案和解析>>
科目: 来源: 题型:
【题目】仔细阅读下面的探究实验信息,回答相关问题。
Ⅰ.(实验目的)探究固体物质溶于水时的热现象。
Ⅱ.(查阅资料)
(1)物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
(2)通常状况下,水的凝固点为0℃、沸点为100℃。
Ⅲ.(提出猜想)物质固体物质溶于水时,有可能出现放热、_____、既不放热也不吸热等三种可能性。
Ⅳ.(实验探究)某探究小组的同学设计了如下图所示的实验方案。试剂瓶a、b、c中分别盛装有A、B、C三种干燥的粉末状固体药品。操作:用a、b、c三个烧杯,分别盛装相同体积的水,将烧杯中的水加热至沸腾,撤去酒精灯,见沸腾刚止即迅速向a、b、c烧杯中对应加入一药匙的A、B、C。现象:a烧杯中的水立即沸腾,b、c烧杯中的水未见沸腾现象。
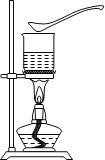
![]()
![]()
![]()
Ⅴ.(实验结论)
(1)物质A溶于水时,其热现象为_____,说明Q吸_______(填“>”或“<”或“=”)Q放。
(2)物质B或C溶于水时,其热现象为_______。
Ⅵ.(反思交流)不能准确断定物质B或C溶于水时的热现象的原因是_______。
Ⅶ.(拓展实验)小张同学对物质A溶于水的实验现象很感兴趣,继续向沸腾刚止的热水中加入相同质量的物质A,又看到沸腾现象,继续如此重复实验,至烧杯中出现固体物质后,再继续加入相同质量的物质A,却看不到沸腾现象。请解释不再产生沸腾现象的原因_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请你根据表中信息回答下列问题:
① | He | ||||||||||||||||
② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | Ne | ||||||||||
⑨ | ⑩ | Ar | |||||||||||||||
Kr | |||||||||||||||||
(1)表中②号与⑥号元素在元素周期表中处于同一_______(填“周期”或“族”)。
(2)表中⑤号元素的元素名称为_____,表中⑥号元素的质子数为_______,⑨号元素的原子结构示意图为_____。
(3)表中⑩号元素在化学反应中容易_______(填“得到”或“失去”电子),⑦号元素的1个原子获得2个电子后所形成的微粒符号为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列计算题:
(1)某元素R的原子能够形成核外有10个电子的Rn- 离子,则元素R的原子序数为_______。
(2)已知:十个C-12原子的质量为m克,一个氧原子的质量为n克,则该氧原子的相对原子质量为_______(用m、n表示)。
(3)已知某温度下,200g水中最多可溶解50gNaCl固体,则该温度下NaCl饱和溶液的溶质质量分数为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列实验题
(实验一)结合净化黄泥水的活动经验和加工自来水的原理,指出下列杂质的除去方法(填方法名称)
水中杂质种类 | 除去杂质的方法名称 |
颗粒较大的不溶性杂质 | ____ |
颗粒较小的不溶性杂质 | ____ |
可溶性杂质 | ____ |
(实验二)实验室欲配制一定质量分数的食盐溶液。请完成下列问题:
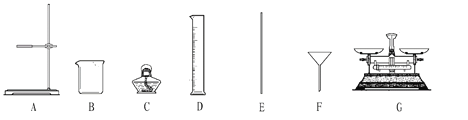
(1)B仪器的名称是_______,D仪器的名称是_____。
(2)完成本实验,所需仪器除B、E外,还必须选用上述仪器中的_______(填仪器编号),仪器E的作用是_______。
(3)配制的步骤可以概括为计算、称量和量取、_______、装瓶。
(4)如果量取水的体积时,操作者的视线是仰视,则所配溶液的质量分数将_______(填“偏大”或“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对氧气的制取进行了进一步探究。
(1)用高锰酸钾制氧气,对比用向上排空气法和排水法收集到的氧气的纯度。
(进行实验)
①用向上排空气法收集氧气:将带火星的木条放在集气瓶口,当_________时证明氧气集满,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
②用排水法收集氧气:氧气能用排水法收集的原因是____,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
氧气的收集方法 | 向上排空气法 | 排水法 | ||||
氧气的体积分数/% | 79.7 | 79.6 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数/% | 79.7 | 89.7 | ||||
(实验分析)不考虑操作失误的因素,用排水法也收集不到纯净的氧气,其主要原因是__________。
(2)用过氧化氢溶液制氧气,探究不同催化剂催化过氧化氢分解的效果。
(查阅资料)
①MnO2、Cr2O3、Fe2O3、CuO、S对过氧化氢的分解均具有催化作用。
②海藻酸钠可以作为催化剂的载体支架,形成负载不同催化剂的海藻酸钠微球。
(进行实验)
①制备五种负载不同催化剂(MnO2、Cr2O3、Fe2O3、CuO、S)的海藻酸钠微球,每个微球大小相同,且负载催化剂的质量相等。
②取30粒负载某种催化剂的海藻酸钠微球与20mL质量分数为5%的过氧化氢溶液,在锥形瓶中迅速混合发生反应,实验装置如图1,采集200s内压强数据,绘制曲线如图2。

(实验分析)
①每次实验时,海藻酸钠微球数应相同的原因是_________。
②本实验中,通过一段时间内______来反映生成氧气的快慢。
③本实验中,负载MnO2的微球显示了良好的催化效果,60s时竟将橡皮塞弹飞,在图2中对应的曲线是_______(填“a”或“b”);负载_______的微球催化效果较好,反应温和;负载Fe2O3、Cr2O3的微球催化效果一般;负载_______的微球催化能力最弱。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com