
科目: 来源: 题型:
【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。我校兴趣小组的同学为此开展了以下探究活动:
【提出问题1】鸡蛋白中主要的营养成分是______ ;
【查阅资料】
a、CaCO3灼烧分解生成氧化钙和一种无毒的氧化物。
b、蛋壳中的其它成分不参加反应。
c、NaHCO3+HCl= NaCl + H2O +CO2↑,Ba(OH)2+CO2=BaCO3↓+H2O,
d、已知仪器a装有10%的稀盐酸,其他成分均不与HCl反应,装置内试剂均足量。
【提出问题2】蛋壳中的CaCO3含量是多少呢?小华拟将该蛋壳放在空气中充分灼烧完成测定;小明拟通过蛋壳与稀盐酸反应完成测定。请你参与他们的探究。
【设计方案】他们分别称取12.0g蛋壳设计了以下不同的实验方案:
小华的方案:
称取12.0g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g。则:减少的质量是______ (填化学式)的质量,经计算得蛋壳中的CaCO3的质量分数为______ 。
(3)小明的方案:小明设计了如下图所示的实验装置。
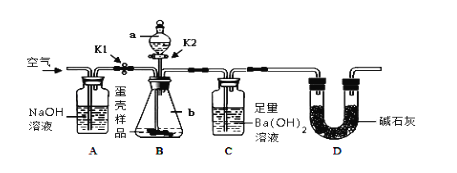
【实验步骤】
①按上图连接好装置后,并______ ;
②向B装置中加入蛋壳样品后,先通入空气一会儿;
③接下来的实验操作是______ ,直到______ 为止(填实验现象);
④再通入空气一会儿,至装置C中不再产生沉淀为止;
⑤将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
⑥重复上述实验。
【实验数据】重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量(g) | 19.68 | 19.75 | 19.67 |
【实验分析及数据处理】
①上述数据能否用托盘天平称量______ 。(填“能”或“不能”)
②若无A装置,直接通入空气,则测定结果将______ 。(填“偏大”、“偏小”或“不变”)D装置的作用是___
③实验重复3次的目的是______ 。
④请利用3次实验数据的平均值,计算该蛋壳中的CaCO3质量分数______ 。
【实验反思】
下列各项措施中,能提高小明测定准确度的是______ (填序号)。
Ⅰ.在装置A、B之间增加盛有浓硫酸的洗气瓶
Ⅱ.缓缓滴加稀盐酸
Ⅲ.在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
IV.直接称量装置C反应前后的质量
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组利用下列装置进行气体的制取实验,请回答下列问题.
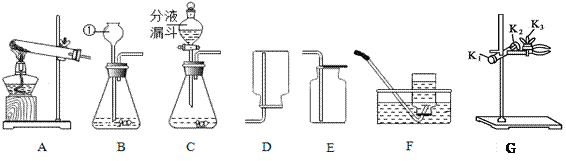
(1)写出标号①仪器的名称___________.
(2)用高锰酸钾制取和收集较纯净的氧气,选择的装置组合是___(填字母)写出反应的化学方程式______________________________,实验后发现制得的氧气不纯,可能的原因是_________________________.(答一点即可)
(3)如图G,要调节夹持试管的铁夹的松紧,应调节旋钮___(填“K1”“K2”或“K3”)。
(4)实验室制取二氧化碳的化学方程式______________________,与B相比,C作为制取二氧化碳的发生装置,优点是_______________,验证二氧化碳收集满的方法是______________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】现有碳酸钠和氯化钠的固体混合样品。由下图实验过程和提供的数据可计算样品中碳酸钠的质量分数约为

A. 47.5% B. 21.2% C. 70.7% D. 85.6%
查看答案和解析>>
科目: 来源: 题型:
【题目】金属是人类生活中的常用的材料。
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是________。(填“符号”)
(2)铁钉在初中化学实验中多次出现,下图展示了光亮铁钉的一系列变化。
![]()
(ⅰ)变化②中,铁钉主要与空气中的________________发生反应。
(ⅱ)变化③中除去铁锈的化学方程式为______________________。
(ⅲ)如果用a、b分别代表光亮的铁钉和无锈铁钉,则它们的质量关系________
A、a<b B、a>b C、a=b D、无法比较
(3)为探究锌、铁、铜三种金属的活动性,以及他们和氢元素的位置关系,小明设计了如下实验,你认为不需要进行的实验是__________________ (填字母序号)。
A.将铁粉放入硫酸锌溶液中 B.将铁粉放入稀硫酸中
C.将铁粉放入硫酸铜溶液中 D.将铜片放入稀硫酸中
(4)该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】,他以铜锈为原料设计并完成如下实验(杂质不与稀硫酸反应,且不含铜元素。图中部分物质略去)。

①无色气体A是________,溶液C中所含的阳离子是________,固体D中含有的物质是_____________。
②在蓝色溶液B中加入铁粉时,发生反应的化学方程式为_____________。
③已知铜锈样品的质量是10g,固体F的质量是3.2g,则铜锈中含Cu2(OH)2CO3的质量分数是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】大气中CO2含量不断升高,使全球气候问题日趋严重。科学家们正在努力尝试通过下列途径减少CO2的排放:利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,流程如图。
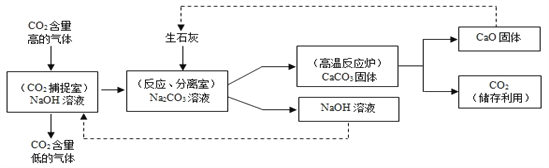
下列有关该过程的叙述正确的是 ( )
该过程可实现CO2零排放
该过程中只有1种物质可以循环利用
C.分离室中分离物质的操作是蒸发
D.该过程至少发生了4个化学反应
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是

A. 将丙的饱和溶液变为不饱和溶液,可采用升温的方法
B. t1℃时,可以制得溶质质量分数为8%的丙溶液
C. t2℃时,甲、乙两种物质的饱和溶液降温至20℃,析出甲的质量比析出乙的质量大
D. t1℃时甲、乙、丙三种物质的饱和溶液升高到t2℃时,溶质质量分数为甲>乙>丙
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组对人体吸入的空气和呼出气体进行了如下实验探究。
(提出问题)人体吸入的空气与呼出气体组成有什么不同?
(资料)①白磷着火点约40℃;②通常条件下,氢氧化钠溶液与白磷不反应,氢氧化钠溶液可以吸收二氧化碳气体。
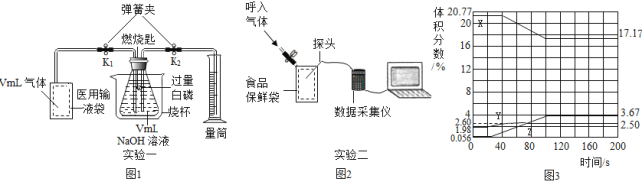
(实验操作)实验一:(如图1)
(1)检查好装置气密性后装入试剂,医用输液袋中收集VmL空气。
(2)打开弹簧夹_______,缓慢将袋中空气全部排入锥形瓶中,读出量筒内收集到液体V1mL.由此测得空气中_____的体积为______mL。
(3)关闭弹簧夹K1、K2,再用_____方法(填具体操作),使燃烧匙内的白磷迅速燃烧,反应的化学方程式为________。充分反应后,冷却至室温,打开K2,量筒内剩余液体为V2mL。由此测得氧气在空气中所占的体积分数可表示为_____。
实验二:(如图2)
(4)把测定氧气、二氧化碳、水蒸气的传感器放入食品保鲜袋,然后向袋内呼出气体。采集的数据经处理如图3所示,表示氧气体积分数变化的_____。(填“X”、“Y”或“Z”)。Y的体积分数在60s之后逐渐减小的原因是_________。
(数据处理)(5)实验二中,200s时没有被采集数据的其他所有气体的总体积分数为____%。
(评价与反思)(6)由实验二分析,人体呼出气体与空气相比,组成上的差异是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组利用以下装置探究气体的制取及性质。
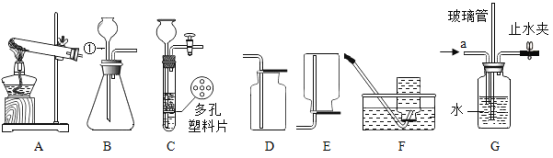
(1)①用高锰酸钾制取氧气,应选择____(填序号)为气体发生装置,反应化学方程式为___,充分反应后,高锰酸钾中的氧元素转化为氧气的最大转化率为________(填序号);
a.25% b.33.3% c.50% d.100%
②为防止高锰酸钾粉末进入导管,应采取的措施是_____(填序号)。
a.润湿玻璃管 b.检查气密性 c.均匀预热 d.在试管口附近放一团棉花
(2)①用装置C制取二氧化碳,多孔塑料片上常放置的药品为______,此装置与B装置相比,最大的优点是_____。
②实验室制取二氧化碳气体的化学反应方程式为_____;收集二氧化碳的装置是_____(填序号),其中仪器①的名称为_____。
(3)①用锌粒与稀硫酸制取氢气,用装置______(填序号)可以收集较纯净氢气;
②点燃不纯的氢气可能发生爆炸。图G是某同学的改进装置:若将氢气的发生装置与导管a连接,松开止水夹,在导管口点燃气体,发生装置不会爆炸。此装置的作用是___(填序号)。
a.提高了气体纯度 b.阻止气体在发生装置内燃烧 c.改变了氢气的化学性质
(4)某兴趣小组设计出了一种有趣的喷泉(如图一)。已知氨气(NH3)是一种无色有刺激性气味的气体,密度比空气小且极易溶于水。

①玻璃套管中的固体可能是_________;
②为了保证实验安全和环保,若选用图二甲、乙装置组合收集氨气,气体应从_____(填a或b)端通入,另一端接乙装置中的c,装置中漏斗的两个作用是______,______。
查看答案和解析>>
科目: 来源: 题型:
【题目】质量守恒定律的发现对化学的发展作出了重要贡献。
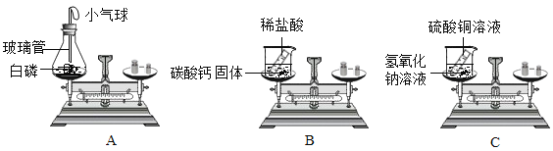
(1)用如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是______(填序号),理由是_________。
(2)从微观角度分析有助于我们理解质量守恒定律,在一密闭容器内有4种物质A、B、C、D,它们在一定条件下发生燃烧的反应,经过一段时间后停止反应,其中A、B、C、D的微观示意图和反应前后各物质的质量如表所示。
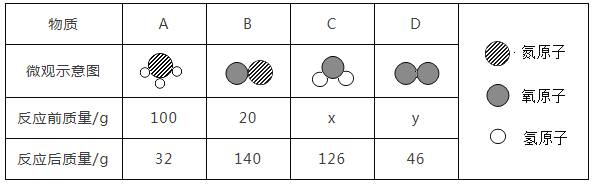
①从微观角度分析,化学反应中质量守恒的原因是______。
②该反应中B和C的质量比为_____。
③表中x的值是______。
(3)1756年,俄国化学家罗蒙诺索夫曾开展的实验:先用天平称取质量为m1的金属锡粉(Sn)。将锡粉放在密闭容器里进行完全燃烧生成了白色固体物质,称量容器的总质量为m2。打开容器,听到了空气进入容器发出的“丝丝的声响”,待容器中空气恢复到初始状态,重新称量容器的总质量为m3。
①锡的常见化合价为+4,则锡的燃烧化学方程式是_________。
②罗蒙诺索夫分析数据后发现,生成白色物质的质量________(用含m1m2m3代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。

探究一:该气体的成分。
(猜想与假设)小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_______。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)(1)由实验①可知,该气体中肯定含有___,该反应的化学方程式__。
(2)由实验②__(填“能”或“不能”)确定该气体中不含氧气,理由是_____。
探究二:泡腾片中碳酸氢钠的含量。
经测定维C泡腾片中钠元素的质量分数是6.9%,则该泡腾片中碳酸氢钠的质量分数是___%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com