
科目: 来源: 题型:
【题目】工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
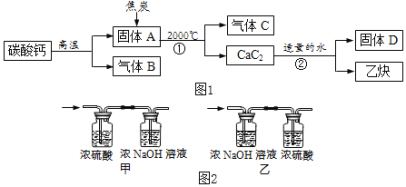
(资料)
(1)碳酸钙高温分解可得两种氧化物。
(2)浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
(讨论)(1)C、B组成元素相同,C有毒,反应①化学方程式为_________。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_________。
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_________。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g
(6)乙炔的化学式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染.于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
(1)操作①的名称是_____.需要的玻璃仪器有烧杯、________ 、玻璃棒。
(2)步骤①中加入过量M的化学式_________.请写出工业上用赤铁矿(主要成分为Fe2O3)炼铁的化学方程式____________.
(3)若加入一定量M(不考虑上述实验过程中后续实验现象和结论),则滤液A中一定含有的溶质的化学式是_________
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6g克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是
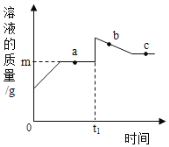
A. 取a点时溶液,加入锌粉,有气体放出
B. b点时,溶液中溶解的物质有两种
C. c点时,烧杯中固体一定是铜
D. 加入铁粉充分反应后的残留固体中有2.8克铁
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下图回答问题:
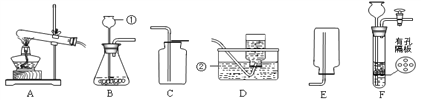
(1)写出有标号的仪器名称:①________,②________ .
(2)实验室用高锰酸钾制取O2的化学方程式为 ________ ,用A、D装置制取O2时,为防止高锰酸钾进入导管,采取的措施是________ .使用该组合制取O2的另一化学反应方程式为________.
(3)实验室用B、C装置制取CO2的化学方程式为 ___,若将发生装置由B改为F,其优点是_____.
(4)某兴趣小组将新制得的CO2通入澄清的石灰水中,未见浑浊.分析原因可能有下列两种情况:
①可能是错用了较浓的盐酸,CO2中混入了较多的氯化氢气体,为验证此想法甲同学查阅资料知:氯化氢气体的水溶液能使紫色石蕊试液变红,于是将气体通入紫色石蕊试液.你认为此方案________(填“是”或“否”)可行.
②可能是生成的CaCO3又与CO2反应生成了可溶性的Ca(HCO3)2,反应的化学方程式为 __________.
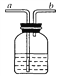
(5)下图是一种有洗气、贮气等用途的装置.用该装置收集氢气时,瓶内先装满水,气体从_____(填“a”或“b”,下同)处导管通入.
查看答案和解析>>
科目: 来源: 题型:
【题目】)下图是利用缺铁性氧化物[Fe(1-y)O]进行CO2再资源化研究的示意图。下列说法正确的是( )
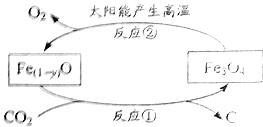
A.如该研究成熟并广泛应用,能缓解温室效应
B.反应①为置换反应,反应②为分解反应
C.反应①提高了铁的氧化物中铁的质量分数
D.整个转化反应的化学方程式可表示为:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验得出的结论或说法不合理的是
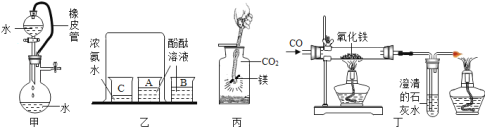
A. 甲装置中水不断下滴,说明此装置一定漏气
B. 乙实验可以说明微粒是不停运动的
C. 丙实验中镁在二氧化碳中剧烈燃烧,说明燃烧不一定需要氧气
D. 丁实验既可以说明一氧化碳能与氧化铁反应,又可以说明一氧化碳具有可燃性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的化学方程式正确的是
A. 铁丝在氧气中燃烧:4Fe+3O2![]() 2Fe2O3
2Fe2O3
B. 铝片溶于稀硫酸:Al+H2SO4═AlSO4+H2↑
C. 古代湿法炼铜:2Fe+3CuSO4═Fe2(SO4)3+3Cu
D. 过氧化钠与二氧化碳常温下反应生成碳酸钠和氧气:2Na2O2+2CO2═2Na2CO3+O2
查看答案和解析>>
科目: 来源: 题型:
【题目】在“宏观一微观”之间建立联系,是学习化学学科必备的思维方式。如图是某反应的微观示意图,下列说法正确的是( )
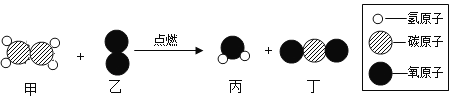
A. 该反应中甲、乙、丙、丁都属于化合物
B. 反应生成甲、乙分子个数比为1:1
C. 参加反应的甲、乙的质量比为15:56
D. 该反应属于置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组欲验证草酸晶体(H2C2O4·2H2O)的热分解产物,请你参与过程分析。探究过程如下:
(查阅资料)
(1)已知草酸晶体(H2C2O4·2H2O)是一种无色晶体,100℃开始失水,101.5℃左右分解产生H2O、CO和CO2,反应方程式为:H2C2O4·2H2O![]() CO↑+ CO2↑+3H2O。
CO↑+ CO2↑+3H2O。
(2)浓硫酸具有吸水性,常用作气体干燥剂。
(3)白色的无水硫酸铜遇水蒸气变蓝色。
(实验设计)用下图所示装置进行实验(装置C、F中澄清石灰水足量)
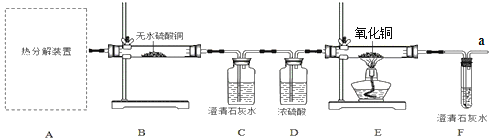
(问题讨论)
(1)下列可用作A中草酸晶体热分解装置的是________(填“甲”或“乙”或“丙”)。
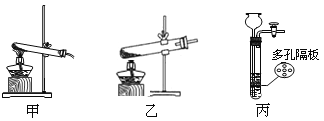
(2)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是________。
(3)实验过程中观察到:B中白色无水CuSO4变成蓝色,C和F中澄清石灰水均变浑浊,E中____(填实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O、CO2、CO ,E中反应方程式是___。
(4)若通过F装置中澄清石灰水变浑浊来证明草酸晶体热分解的气体产物中有CO,则需在C和D装置之间增加盛有澄清石灰水的洗气瓶,其作用是__________。
(5)从环保角度考虑,该套实验装置有明显缺陷,其改进方式为________。
(继续探究)
(6)兰兰把E中生成的铜与稀硫酸混合加热,发现加热沸腾一段时间后,溶液开始变成淡蓝色,同时产生较多的气泡,生成的是什么气体呢?她猜想①可能是H2 ;②可能是NO2 ;③可能是SO2 ,亚亚认为猜想_________(填序号)一定是错误的,理由是_______。
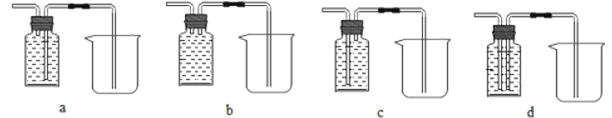
(7)该小组同学认为a导管尾气中的一氧化碳可以利用,于是将a导管与下列装置连接,除去尾气中的二氧化碳并收集一氧化碳,准备进行后续地探究,其中最合理的装置是______。(填“a、b、c、d”,瓶内为氢氧化钠溶液,能吸收尾气中的CO2)。
(定量分析)
(8)如果有1.4克一氧化碳与E中足量的氧化铜完全反应,生成的气体完全被F中足量的石灰水充分吸收,可得到沉淀多少克______?(请写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组的同学从实验收集到一桶含有FeSO4、CuSO4的废液, 他们想从中回收金属铜和硫酸亚铁晶体,设计了如下操作方案, 结合方案回答下列问题:
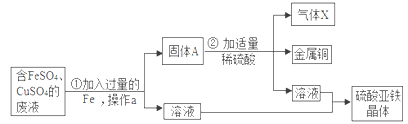
(1)固体A中含有_______(填化学式),无色气体X为_______(填化学式)。
(2)步骤①中反应的化学方程式为____________,该反应的基本类型为_________反应。
(3)操作a的名称为__________,在该操作中用到了玻璃棒其作用为_________。
(4)步骤②中加入适量稀硫酸的目的是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com