
科目: 来源: 题型:
【题目】很多家庭开始使用“扫地机器人”,它不仅可以帮助我们扫地,而且简单实用。请回答下列问题:

(1)“扫地机器人”机身外壳材料的主要成分是铝合金,它属于___ (填“纯净物”或“混合物”)
(2)该款机器人的电池可以利用太阳能充电,则在充电过程中是将太阳能转化为_____能;太阳电池板的主要材料是硅,硅单质与金刚石结构相似,则构成硅单质的粒子是____
(3)请用化学方程式表示金属铜、铝的活动性顺序_____________
(4)根据扫地机器人的制造、使用情况,谈一谈化学与生活的关系______________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为某化工企业生产流程示意图,有关说法正确的是

A. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
B. 钛酸亚铁(FeTiO3)中钛元素为+3价
C. 中氩气(Ar)作反应物
D. 中反应为:2FeTiO3+6C+6Cl2![]() 2X+2TiCl4+6CO,则X为FeCl3
2X+2TiCl4+6CO,则X为FeCl3
查看答案和解析>>
科目: 来源: 题型:
【题目】在点燃条件下,M和N反应生成X和Y。反应前后分子变化的微观示意图如下所示(其中“![]() ”代表氢原子,“
”代表氢原子,“![]() ”代表碳原子,“
”代表碳原子,“![]() ”代表氧原子)。下列叙述中,不正确的是
”代表氧原子)。下列叙述中,不正确的是
物质 | M | N | X | Y |
微观示意图 |
|
|
|
|
A.生成物均为氧化物
B.在该反应中,生成X和Y的质量比为9:22
C.M中碳、氢、氧三种元素的质量比为12:3:8
D.在该反应中,M和N两种物质的分子个数比为1:3
查看答案和解析>>
科目: 来源: 题型:
【题目】小明同学利用以下材料自制酸甜可口的汽水。
材料:1瓶(500 mL)纯净水、5g蔗糖(C12H22O11)、1. 5 g小苏打(NaHCO3)、1.5 g柠檬酸(C6H8O7)。
制备过程如下图所示:
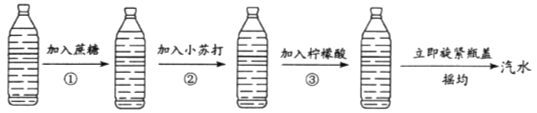
已知:小苏打与柠檬酸发生的反应为3NaHCO3 +C6H8O7=C6H5O7Na3+3H2O+3CO2↑
(1)NaHCO3由___________种元素组成,其相对分子质量为_________。
(2)蔗糖中各元素的质量比为____________________。
(3)柠檬酸中碳元素的质量分数为________________。
(4)加入柠檬酸后,立即旋紧瓶盖的原因是______________。
(5)自制汽水的溶质有C6H5O7Na3、CO2、C12H22O11和_______________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化氢在生产生活中有着广泛的应用。化学实验小组对过氧化氢的某些性质进行了研究。
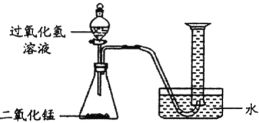
Ⅰ.不稳定性
(1)如图所示进行实验(还测量收集的氧气体积),过氧化氢分解的化学方程式为_________________。
(2)能用排水法收集氧气的原因是 _________________________。
(3)已知:常温常压下,氧气的密度为1. 33 g·L–1。实验小组称量了10 g溶质质量分数为 6%的过氧化氢溶液进行实验,如果将该过氧化氢溶液一次性全部放入锥形瓶中,则选择规格为________mL(选填“50”、“200”或“250"”)的量筒收集氧气较为合适。
(4)实验小组同学还探究了温度对过氧化氢分解速率的影响,相关实验数据如下表:
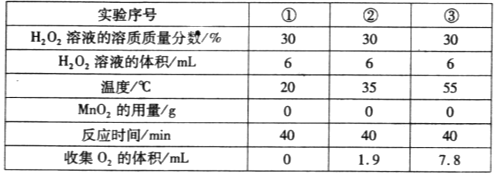
由此得出的结论是_________________________。
Ⅱ.腐蚀性
(查阅资料)H2O2溶液有一定的腐蚀性。
(进行实验)将铜片分别浸泡在以下3种溶液中进行实验,实验现象如下表:
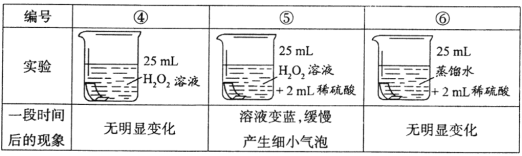
(解释与结论)
(5)实验④的作用是________________。
(6)实验⑤中铜片被腐蚀的反应为Cu + H2O2+ H2SO4=CuSO4+□________,请补全该反应的化学方程式。
(反思交流)
(7)小红同学提出,实验⑤中除发生(6)所给的反应外,还发生了另一个反应导致有细小的气泡产生,该反应的反应物是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某些铜制品在空气中久置,表面会生成绿色的铜锈(又称铜绿)。某化学兴趣小组设计并进行如下实验,以探究铜锈的组成和铜生锈的条件。
Ⅰ.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
(进行实验)兴趣小组同学从铜器上取下适量的干燥铜锈,按下图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
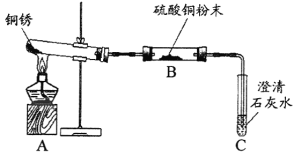
(解释与结论)
(1)C中反应的化学方程式为_________________。
(2)依据以上现象分析,铜锈中一定含有的元素为铜和________(填元素名称)。
Ⅱ.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)兴趣小组同学取直径、长度均相同的铜丝,打磨光亮,并设计了如下图所示的5个实验,一周后观察到的实验现象如下表:
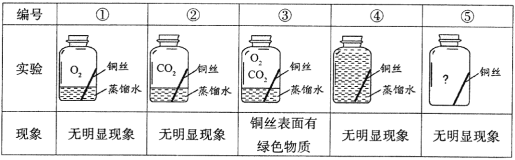
(解释与结论)
(3)实验中都使用了经煮沸并迅速冷却的蒸馏水,“煮沸并迅速冷却”的目的是_____________。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是___________(填编号)。
(5)对比实验②和③,得出的结论是_____________。
(6)为验证猜想,请在图中将实验⑤补充完整_____________。
(7)由上述实验可推知,铜生锈的条件是_____________。
(反思与应用)
(8)结合上述实验,你对日常生活中保存铜制品的建议是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用空气制取氮肥的主要流程如图:
![]()
(1)过程Ⅰ是利用空气中各成分的沸点不同,分离得到氮气,该过程发生的是_____变化(选填“物理”或“化学”)。
(2)过程Ⅱ中,氮气和氢气反应生成氨气,该反应为_____反应(填基本反应类型名称)。
(3)过程Ⅳ发生反应的微观示意图如图:
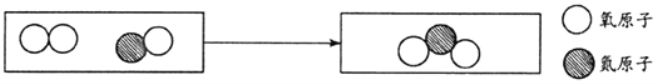
过程Ⅳ发生反应的化学方程式为_____。
(4)过程Ⅲ中发生的反应为氨气和氧气在催化剂、加热条件下反应生成一氧化氮气体和另一种氧化物W,该反应的化学方程式为_____,并列式计算当有20.4t氨气参加反应时理论上生成的一氧化氮的质量。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是配制180g溶质质量分数为10%的NaCl溶液的实验操作示意图。
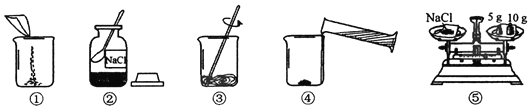
(1)正确的操作顺序是_____(填图中的数字序号)。
(2)请在图中画出即将向天平左侧托盘上加氯化钠固体进行称量时游码(用“![]() ”表示)的位置。
”表示)的位置。
![]()
(3)在称取氯化钠的过程中,观察到指针轻微的偏向分度盘的右侧,则接下来的操作应该是_____。
(4)实验中需要量取水的体积为_____mL,应选择规格为_____mL(选填“50”、“100”、“200”或“250”)的量筒来量取水。
(5)溶解时,用玻璃棒搅拌的作用是_____。
(6)下列操作会导致所配溶液的溶质质量分数偏大的是_____。
A.氯化钠固体不纯
B.配制溶液的烧杯事先用少量蒸馏水润洗
C.用量筒量取水时俯视读数
D.把配制好的溶液装入细口瓶时有少量液体洒出
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图所示装置探究可燃物燃烧的条件。
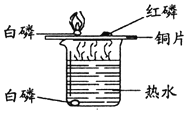
(1)白磷( P4)在空气中的燃烧产物与红磷的燃烧产物相同,写出白磷燃烧的化学方程式:_____。
(2)对比铜片上白磷燃烧和红磷不燃烧的现象,说明可燃物燃烧的条件之一是_____。
(3)能说明可燃物燃烧需要与氧气接触的现象是_____。
(4)烧杯中80℃的热水所起的作用是_____。
(5)实验完毕将烧杯中的热水慢慢倒出,当白磷刚露出水面便剧烈燃烧起来,其原因_____。
(6)从以上实验可得到的启示:实验室保存少量白磷的方法是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效多功能净水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为: 3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)次氯酸钠(NaClO)的相对分子质量为__;其中氯元素的化合价为__;
(2)高铁酸钠(Na2FeO4)中铁元素和氧元素的质量比为____(填最简比);
(3)现要制得830kg含杂质20%的高铁酸钠,至少需要次氯酸钠的质量是多少__________?(列式计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com