
科目: 来源: 题型:
【题目】(本题共12分)某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如下图所示。
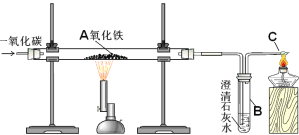
(1)A处发生反应的化学方程式是 。
(2)B中发生反应的化学方程式是_____________________。
C处点燃酒精灯的目的是_______________________。
(3)实验结束后,小李看到红色固体全部变黑了,认为产物就是单质铁,但小王提出了质疑:还有可能生成其它物质。为了进一步验证其固体成分,小王查到下列资料:
铁的氧化物有氧化铁、氧化亚铁、四氧化三铁(该化合物中铁有+2、+3两种化合价),其中氧化铁为红棕色,其余都为黑色;并且只有四氧化三铁能被磁铁吸引。②铁的氧化物都能与酸发生反应而溶解。
根据上述信息,小王又设计了两个实验。
①将黑色固体研磨后,取少量加入_______溶液中,观察到有气泡出现,溶液未变黄色,据此得出的结论是______________________________。
再用磁铁吸引余下黑色固体,实验后即可对黑色固体成分进行判断_______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如图所示(不含结晶水),请回答:
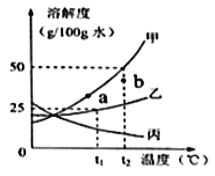
(1)t2℃时,将30g甲固体加入到50g水中,充分搅拌后的所得溶液是_____(填“饱和”“不饱和”)。
(2)若甲中含有少量乙,应用________法提纯甲。
(3)等质量的甲、乙、丙三种饱和溶液从t2℃降温至0℃后,溶液的质量分数由大到小的顺序是 _________。
(4)若使甲溶液的状态从a点转化为b点,可采取的措施是 ______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为解决环境污染问题,我区已全面禁止燃煤取暖,大力推行天然气取暖。
(1)煤、石油、天然气被称为化石燃料。天然气是比较清洁的化石燃料,其主要成分完全燃烧的化学方程式是______。
(2)氢气被认为是理想、清洁的燃料,氢气燃烧的化学方程式是______。请再举出2种清洁能源:______、______。
查看答案和解析>>
科目: 来源: 题型:
【题目】水是生命之源,请回答有关水的下列问题:

(1)电解水实验如图所示。①中所得气体是______,①与②中所得气体的体积比约为______。该反应的微观示意图如下,请在方框内补全相应微粒的示意图。_____

(2)“生命吸管”是一种便携式户外净水器。其净水原理如下图:
![]()
①抗菌活性复合滤料中有活性炭、离子交换树脂等。活性炭的主要作用是______。
②离子交换树脂能去除原水中的钙离子,钙离子的符号是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组探究盐酸和氢氧化钠反应过程中溶液![]() 的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
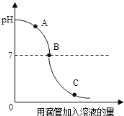
A. 该实验是将氢氧化钠溶液滴入盐酸中
B. ![]() 点时的溶液能使石蕊试液变红
点时的溶液能使石蕊试液变红
C. ![]() 点表示盐酸和氢氧化钠恰好完全反应
点表示盐酸和氢氧化钠恰好完全反应
D. ![]() 点时,溶液中的溶质只有氯化钠
点时,溶液中的溶质只有氯化钠
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是
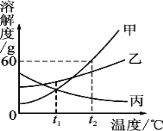
A. t2℃100 g甲物质饱和溶液中含有60 g甲
B. t2℃时,三种固体物质的溶解度关系为甲>乙>丙
C. 将丙物质不饱和溶液变为饱和溶液,可采用升温的方法
D. t2℃时,分别用100 g水配制甲、乙的饱和溶液,再降温到t1℃,析出固体的质量:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠广泛用于造纸、纺织、玻璃、洗涤剂、肥皂、制革等工业,是一种重要的化工原料。吕布兰、索尔维和侯德榜为碳酸钠的工业化生产作出了巨大贡献。
I、吕布兰法
1789年,法国医生吕布兰 (N.Leblanc,1742﹣1806)以食盐、浓硫酸、木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如图:
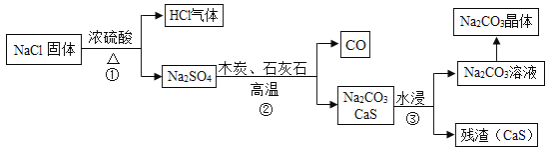
(1)碳酸钠俗称_____。
(2)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为 ___________。
(3)③中“水浸”时通常需要搅拌,其目的是________。
(4)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处______。
Ⅱ、索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
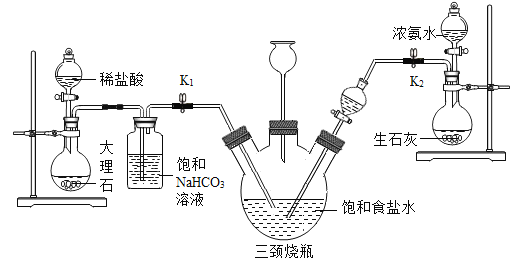
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
请回答下列问题:
(5)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为_____;
(6)三颈烧瓶上连接的长颈漏斗的主要作用是_____
(7)①根据实验记录,计算t2时 NaHCO3固体的分解率 (已分解的 NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_________。
②若加热前NaHCO3固体中还存在少量NaCl,上述计算结果将_____ (填“偏大”、“偏小或“无影响”)。
(8)制碱技术在很长一段时间内把持在英、法等西方国家手中,我国化学工程专家侯德榜先生独立摸索出索尔维法并公布与众,又于1943年创造性地将制碱与制氨两种工艺联合起来,基本消除废弃物的排放,同时生产出碳酸钠和氯化铵两种产品,这就是著名的侯氏制碱法。下列认识或理解正确的是_____
①科学认识是在曲折的、艰辛的积累过程中不断进步的;
②“科技兴邦、实业救国”是侯德榜先生回国研究的巨大动力;
③侯氏制碱法大大提高了原料的利用率,它符合当今“绿色化学”的理念。
查看答案和解析>>
科目: 来源: 题型:
【题目】在粗盐的提纯实验中
(1)其主要操作步骤顺序是______。
①过滤 ②溶解 ③蒸发 ④计算产率
(2)蒸发时,蒸发皿内出现____时应停止加热。
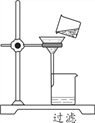
(3)如图是某同学过滤的操作图,指出图中明显错误______;过滤后,如果滤液仍然浑浊,其原因可能是____。(填一种)
(4)通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质MgCl2、CaCl2得到纯净的NaCl,可采用如下图所示流程:
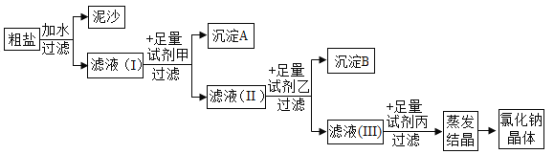
①上图中所用甲、乙、丙三种试剂依次是____。
A NaOH溶液、Na2CO3溶液、稀盐酸
B Na2CO3溶液、KOH溶液、稀盐酸
C NaOH溶液、Na2CO3溶液、稀硫酸
步骤I和步骤II能否互换 (填“能”或“否”)___;加入足量试剂丙的作用是___。
②反思交流:通过以上规范操作,制得氯化钠的质量比原粗盐样品中含氯化钠的质量___(填“增多”、“减少”、“不变”)。
(5)实验室用氯化钠固体配制50g15%的氯化钠溶液
①在溶解过程中,玻璃棒的作用是____。
②下列操作中,可能导致配制氯化钠溶液的溶质质量分数偏大的是____(填序号)。
a.称取时,将氯化钠置于托盘天平的右盘 b.量取水时俯视读数
c.用已有少量水的烧杯溶解氯化钠 d.转移时,有少量溶液溅出
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制取气体的常用装置
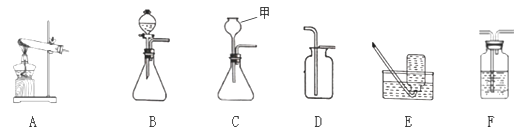
(1)上图C装置中,仪器甲的名称为_______
(2)实验室欲选用A装置制取氧气,其反应方程式为______;若用D装置收集氧气,如何验证氧气已集满______。
(3)实验室若用碳酸钠粉末和稀盐酸制取并收集二氧化碳,可选用_______装置组合进行 (选填字母)。
①为了得到纯净、干燥的二氧化碳气体,除杂装置 (如图)的导管按气流方向连接顺序是 (_______)(选填字母)。

A a→b→c→d B b→a→c→d
C c→d→a→b D d→c→b→a
②常用澄清石灰水检验二氧化碳的存在,该反应的化学方程式为____;若二氧化碳过量,二氧化碳又会与碳酸钙、水反应生成易溶的碳酸氢钙[Ca (HCO3)2],该反应的化学方程式为_____。向含有氢氧化钙14.8g的石灰水里缓缓通入一定量二氧化碳,充分反应后若生成10g沉淀,则通入二氧化碳的质量可能为_____ (选填字母).
A 4.4g B 8.8g C 13.2g D 17.6g
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
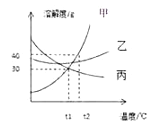
A. 降温可使丙物质的不饱和溶液变成饱和溶液
B. t2℃时,等质量甲、乙、丙的饱和溶液中溶剂的质量:甲>乙>丙
C. t2℃时,将15g甲物质加入到50g水中,再降温到t1℃,所得溶液溶质的质量分数不变
D. 分别将甲、乙、丙三种物质t2℃的饱和溶液降温到t1℃,所得溶液溶质的质量分数乙>甲=丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com