
科目: 来源: 题型:
【题目】下列图象是对应变化在反应前后,固体质量随反应时间变化的关系图,其中正确的是( )
A. 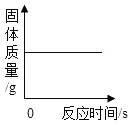 在密闭容器中,镁带燃烧前后固体质量的变化
在密闭容器中,镁带燃烧前后固体质量的变化
B. 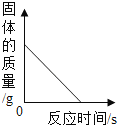 木炭还原一定质量的氧化铜
木炭还原一定质量的氧化铜
C.  向一定质量二氧化锰中加入过氧化氢溶液
向一定质量二氧化锰中加入过氧化氢溶液
D. 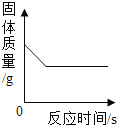 加热一定质量的高锰酸钾制氧气
加热一定质量的高锰酸钾制氧气
查看答案和解析>>
科目: 来源: 题型:
【题目】如图的反应中,甲、乙、丙三种分子的个数比为1︰3︰2,则从图示中获得的信息正确的是
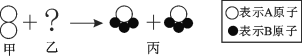
A.生成物一定属于氧化物 B.原子种类在化学反应中发生了变化
C.该反应不可能是分解反应 D.乙分子中A与B的原子个数比为1∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成。为了确定该粉末的成分,同学们进行如下探究:
请回答下列问题:
(猜想假设)
(1)黑色粉末是铁粉
(2)黑色粉末是氧化铜粉末
(3)黑色粉末是铁粉和氧化铜粉末的混合物
(设计方案)取少量黑色粉末,放入硬质玻璃管中,
通入一氧化碳气体,片刻后加热充分反应(实验装置如图所示)
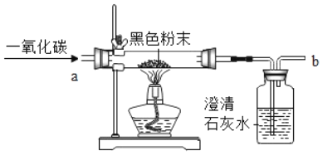
请填写如表空白:(实验中铁粉和氧化铜粉末两物质间不发生反应)
实验中可能出现的现象 | 结论 |
_____ | 猜想(1)成立 |
黑色粉末全部变红,澄清的石灰水变浑浊 | 写出石灰水变浑浊的化学方程式____。 |
_____ | 猜想(3)成立 |
(反思评价)
(1)实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温。继续通入一氧化碳的目的是_____。
(2)从环保角度上看,上述装置有不足之处,改进的方法是_____。
(3)经过实际实验,确认猜想(2)成立。继续实验,直到玻璃管中的固体质量不再减少时,测得澄清石灰水吸收了4.4克的二氧化碳,求黑色粉末的质量______。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制取气体的有关装置图,据图回答下列问题:

(1)写出图中标号仪器的名称:m_____。
(2)实验室制取CO2的化学方程式为_____,收集装置为_____(填装置序号,下同),验满的方法是_____。
(3)若用氯酸钾制取氧气,选用的发生装置为_____,反应的化学方程式为_____。若用E装置收集氧气,氧气应从_____(填“a”或“b”)端通入。
(4)若要F中的两个气球悬浮在空气中,则甲可能是_____(填序号)。
a 空气 b 氧气 c 氢气
(5)兴趣小组探究了影响大理石与稀盐酸反应剧烈程度的因素。
(查阅资料)反应物的浓度越大,反应速率越快。
(实验过程)(注:盐酸足量)
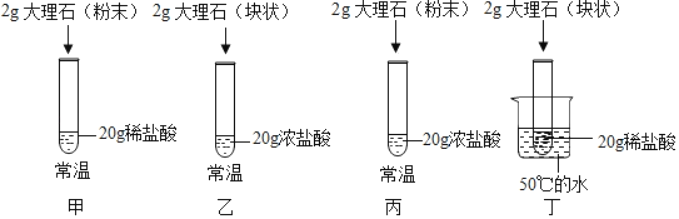
(实验分析)
①若要探究盐酸浓度大小对反应的影响,可选择实验甲与_____对照(选填实验编号)。
②除盐酸浓度大小外,上述实验研究的另两个影响反应的因素是_____和_____。
(交流讨论)与甲相比较,下列对丙的分析,错误的是_____ (选填编号)。
A 反应更为剧烈 B 产生的二氧化碳速度更快 C 产生的二氧化碳的质量更大
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示初中化学常见物质间的转化关系,A、B 为组成元素相同的两种固体,E、F 常温下均为液体且组成元素相同,H、I为无色气体且组成元素相同;D、G和J都是黑色固体,K是一种亮红色金属单质,请回答下列问题:(部分反应条件和生成物略去)
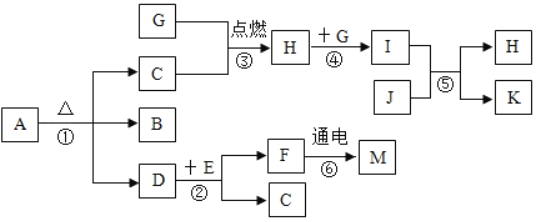
(1)I的化学式_____。
(2)写出反应①、②的化学方程式:①_____;②_____。
(3)图中①﹣⑥反应中属于分解反应的是_____(填序号)。
(4)写出反应⑤的实验现象:_____。
(5)写出H的一种用途_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属是工业的脊梁,结合课本知识回答下列问题。
(1)常温下大多数金属都是固体,但体温计中的金属却是液体,该金属是_____(填元素符号)。
(2)氧化铝的熔点(2050℃)高于铝的熔点(660℃)。硬铝(含铝、铜、镁、硅)是用途广泛的铝合金,硬铝比铝的硬度_____(填“大”或“小”)。
(3)氧化铝可用于制造耐火砖等耐高温材料,这是因为_____。
(4)从活泼金属的化合物中提炼单质比较困难。人类3000多年前就使用铜,1500多年前就使用铁,推测人类使用铝比使用铁的年代_____(“早”或“晚”)。
(5)探究铝与酸的反应前、用砂纸打磨铝条是为了除去_____(填化学式)。
(6)如图为铝原子的原子结构示意图及铝元素在元素周期表中的相关信息,根据图示下列说法错误的是_____
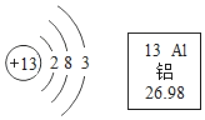
A 铝的原子序数是13 B 铝原子在反应中易得到电子,形成阳离子
C 铝的相对原子质量是26.98g D 铝元素属于金属元素
(7)赤铁矿主要含氧化铁,写出工业上用一氧化碳冶炼该矿石的化学方程式_____。
(8)某合金中含有金属钪(Se)。相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性Se_____Zn(填“>”或“<”)。已知Se与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】21世纪是钛的世纪。利用钛白粉(TiO2)生产海绵钛(Ti)的工艺流程如下:下列说法不正确的是( )
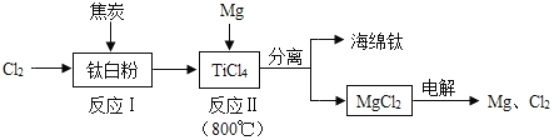
A. 该工艺流程所使用的原料中,TiO2属于氧化物
B. 反应Ⅱ可获得海绵钛,化学方程式为TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
C. 该工艺流程中,氯气和镁可以循环使用
D. 分解MgCl2的过程中,化学能转化为电能
查看答案和解析>>
科目: 来源: 题型:
【题目】小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成份。
(提出问题)该淡黄色固体的化学成份是什么?
(查阅资料)
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
(设计实验方案)
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是_____(填“方案一”或“方案二”),理由是_____。
(实验验证并得出结论)
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH),确定该淡黄色粉末为过氧化钠(Na2O2)。
小明还想对生成的气体成分进行判断,他提出了以下三种假设:
A 该气体是CO2 B 该气体是O2 C 该气体是H2
①同学们首先一致认为上述假设中的_____(填“A”或“B”或“C”)肯定不合理,理由是_____。
②通过查阅资料,同学们又得知:在化学反应中,有元素化合价升高,就必然有元素化合价降低。于是通过小组讨论,大家一致认为上述假设中的_____(填“A”或“B”或“C”)肯定也不合理。
③同学们用图1装置(装置气密性良好)进行实验检验,验证了上述分析的合理性:
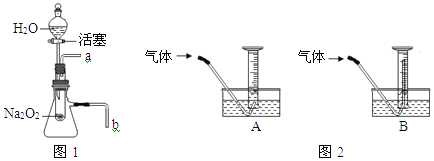
他们的方法是:打开活塞使水流入试管,将带火星的木条放在导管_____(填“a”或“b”)处,发现木条复燃,说明生成的气体是氧气。
④小佳同学待试管内固体完全溶解且不再有气泡产生后,往试管内加入少量二氧化锰,又立即产生大量气泡,由此可知过氧化钠与水反应后的溶液中含有过氧化氢,写出过氧化氢在二氧化锰催化下分解的化学方程式:_____。
⑤小王同学用图2装置,测量生成氧气的体积:测量气体体积读数时,必须待试管和量筒内的气体都冷却至室温时才能进行,因此应选用图2装置中的_____(填“A”或“B”),否则测量结果会_____(填“偏大”或“偏小”)。
(交流与反思)
下列关于Na2O2说法不正确的是_____(填字母序号)。
a.Na2O2中氧元素的化合价是﹣2价
b.Na2O2必须密封保存
c.Na2O2着火后可用水扑灭
(定量计算)
通过进一步查阅资料可知:过氧化钠 (Na2O2)与水反应时,先生成氢氧化钠和过氧化氢,然后过氧化氢再分解产生氧气。总反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.小李同学将20g某过氧化钠样品放入足量水中,充分反应后共产生气体3.2g(杂质不与水反应)。求该样品中过氧化钠的质量分数_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】空气是宝贵的自然资源,其组成如下表。
空气组成 | N2 | O2 | X | CO2 | 其它 |
体积分数 | 78% | 21% | 0.934% | 0.034% | 0.02% |
如图是以空气、煤等为原料合成尿素[CO(NH2)2]的流程(部分产物已略去)。请按要求回答相关问题:
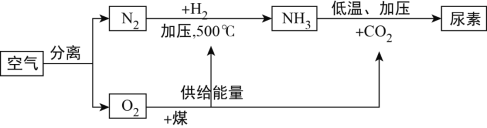
(1)上表中X的名称是________。
(2)氮气和氢气合成氨气属于________反应.(填基本反应类型)。
(3)分离空气的常用方法有以下两种。
Ⅰ.将空气液化后再气化,液态空气气化时首先分离出氮气。则沸点:N2________O2(选填“高于”、“等于”、“低于”)
Ⅱ.用分子筛分离.分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N2________O2(选填“大于”、“等于”、“小于”)。
(4)结合流程推测:化学反应中发生物质变化的同时一定还伴随有________变化。(选填“状态”、“能量”、“原子”、“压强”)。
(5)写出NH3合成尿素的符号表达式:________________。
(6)已知:相同条件下气体的体积之比等于其分子个数之比。则空气中氮分子与氧分子总质量之比等于________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com