
科目: 来源: 题型:
【题目】不同温度下,碳酸钠和碳酸氢钠的溶解度如下表所示
温度/℃ 溶解度/g | 0 | 20 | 40 | 60 |
碳酸钠 | 7.0 | 21.8 | 48.8 | 46.4 |
碳酸氢钠 | 6.9 | 9.6 | 12.7 | 16.4 |
⑴ 服用碳酸氢钠治疗胃酸过多时,胃液的pH________(填“增大”、“减小”或“不变”),发生反应的化学方程式是____________________。
⑵为区分碳酸钠和碳酸氢钠两种白色固体。在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示。

甲烧杯中加入的物质是________(填化学式),加入的质量m的范围为:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效、安全的消毒剂。
⑴ ClO2中氯元素的化合价是______。SO2和ClO2一样都属于氧化物,SO2中氧元素的质量分数为_______。
⑵ 在一定条件下,ClO2与氰化氢(HCN)反应的微观示意图如下:

“![]() ”表示的物质的化学式为____,反应生成的N2与CO2的质量比为____。
”表示的物质的化学式为____,反应生成的N2与CO2的质量比为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如右图所示,“”表示相连的两种物质能发生反应,“![]() ”表示一种物质能转化成另一种物质,部分反应物、生成物及反应条件未标出。下列说法错误的是
”表示一种物质能转化成另一种物质,部分反应物、生成物及反应条件未标出。下列说法错误的是
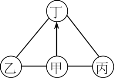
A. 甲的物质类别只能是单质或酸
B. 甲是镁,乙和丙可以是酸
C. 甲是酸,乙和丙可以是金属
D. 甲、乙、丙、丁可分属不同类别的物质
查看答案和解析>>
科目: 来源: 题型:
【题目】电视节目《荒野求生》中的生命吸管(如图所示)是一种将污水净化为饮用水的吸管装置,可以除去 99.3% 的细菌和病毒,但难以除去汞等金属离子。回答下列问题:

(1)汞等金属离子危害人体健康的原因是 。
(2)生命吸管 (“能”或“不能”)使硬水软化。家庭中使硬水软化一般采取 方法。
(3) 吸管中活性炭主要用来除去 。碘主要起到杀菌消毒作用,生活中消毒还可采用84消毒液,有效成分是次氯酸钠(NaClO),杀菌原理是与空气中的二氧化碳和水反应生成碳酸氢钠和次氯酸(HClO),试写出反应方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
I.定性探究
(提出问题)烧碱样品中含有哪些杂质?
(猜想)猜想一:可能含有Na2CO3;
猜想二:可能含有NaCl,作出此猜想的依据______(用简洁的文字表述)。
(设计实验)
实验步骤 | 实验现象 | 解释或结论 |
①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。 | 试管外壁发热 | 原因是 ______ |
②向①所得的溶液中加入稀硝酸至过量,将产生的气体通入澄清石灰水 | 有气体产生,澄清石灰水浑浊 | 样品中含有的杂质是 ______ |
③向②所得的溶液中滴加几滴硝酸银溶液。 | 无现象 | 猜想二 ______ (填“正确”或“错误”) |
(交流与讨论)小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”,你同意他的观点吗?若不同意,写出理由______。
Ⅱ.定量探究
(提出问题)烧碱样品中氢氧化钠的质量分数是多少呢?
(设计实验)小丽同学设计探究方案①、②进行实验并测得数据如下:
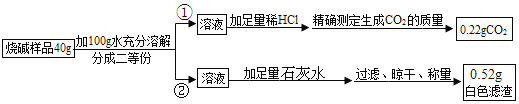
(交流与反思)
(1)小强同学认为方案②因缺少______(填操作名称),导致测得的氢氧化钠的质量分数偏小。
(2)请你利用方案①测得的数据计算烧碱样品中氢氧化钠的质量分数______(请在答题纸上写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】注射器的运用对某些化学实验现象的观察或实验过程的改进常常起到了意想不到的效果。
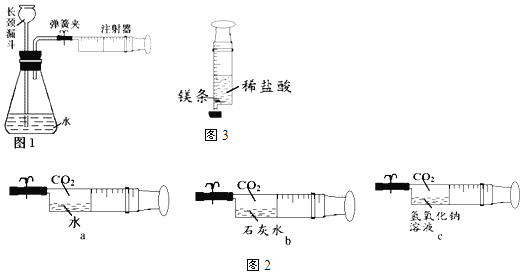
(1)检查装置的气密性(如图1)
连接好装置(注射器内留有一半体积的空气),打开弹簧夹,向长颈漏斗中注入水,使其下端管口形成液封,然后慢慢推注射器的活塞,看到______现象,则说明装置的气密性良好。
(2)探究CO2的性质(如图2)
用注射器吸收液体和CO2(体积比均为1:5),然后夹紧弹簧夹,用力振荡。
①依据______(填“a、b或c”)现象的对比,可认为氢氧化钠和二氧化碳发生反应,写出该反应的化学方程式______。
②若要证明a中也发生了化学反应,你的实验方案是(写出操作、现象)______。
(3)探究镁与盐酸的反应(如图3)
将一小块镁条放在注射器中,再吸取10mL的稀盐酸,迅速封住注射器的尖嘴部分。完毕后注射器中镁条有剩余,向试液中滴入两滴酚酞溶液,溶液变红。
(查阅资料)氢氧化镁微溶于热水,且溶解度随温度升高而增大。
(提出猜想)猜想Ⅰ:氯化镁溶液呈碱性使酚酞变成红色;
猜想Ⅱ:镁与热水反应后生成碱使酚酞变红色。
(实验与思考)
①为验证猜想Ⅰ,需测定______溶液的酸碱性,实验表明该溶液显弱酸性。
②为验证猜想Ⅱ,在滴有两滴酚酞的热水中放入一段镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气泡产生,收集并点燃该气体,发现气体能燃烧。请根据以上现象写出镁与热水反应的化学方程式______。
③在进行上述猜想Ⅱ的探究时,发现实验一段时间后,酚酞的红色总是会逐渐消失。
甲同学猜想:可能是镁与热水反应后生成的碱逐渐被空气中的______反应掉了;
乙同学猜想:可能是水温逐渐降低,导致氢氧化镁的溶解度变小。
请你设计一个简单的实验方案验证乙同学的猜想(写出相应的操作、现象和结论)______。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国著名化学家侯德榜发明的“联合制碱法”主要原理是:
Ⅰ.向浓氨水中通入足量的CO2,使氨气、水和CO2发生化合反应而生成NH4HCO3溶液;
Ⅱ.向所得溶液中加入食盐细粒,充分搅拌,会析出溶解度较小的小苏打固体并得到化肥溶液;
Ⅲ.加热析出的固体制取纯碱。
此法经过调整并应用于化工产业,某化工企业的工艺流程示意图如下,请完成下列填空:
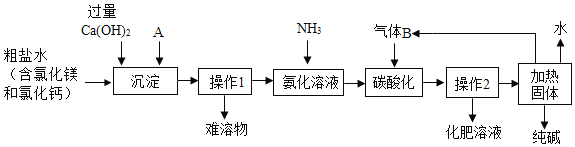
(1)“联合制碱法”原理Ⅱ中发生反应的化学方程式为______,该反应能够发生的原因是______。
(2)在如图所示的流程中,先加过量的Ca(OH)2溶液是为了除去______离子(写符号),再加入A溶液的化学式是______,两种溶液加入的先后顺序能否颠倒?说明理由______。
(3)“操作1”需用的玻璃仪器有______,“氨化溶液”后,溶液的pH______7(填“大于”、“小于”或“等于”),从而有利于吸收“气体B”。
(4)该工艺流程中可循环利用的物质为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是密闭容器中某反应的微观示意图,“![]() ”、“
”、“![]() ”表示不同种元素的原子.
”表示不同种元素的原子.
![]()
(1)反应前的方框内应再填入1个______微粒(填序号),判断依据是______.
A.![]() B.
B.![]() C.
C.![]()
(2)该反应属于______反应(填:“分解”、“化合”或“置换”).
(3)“![]() ”和“
”和“![]() ”两种原子的本质区别是______不同.
”两种原子的本质区别是______不同.
(4)若“![]() ”表示水分子,则MnO2催化“
”表示水分子,则MnO2催化“![]() ”分解的化学方程式为______.
”分解的化学方程式为______.
(5)若“![]() ”表示二氧化碳分子,写出“
”表示二氧化碳分子,写出“![]() ”与氧化铁反应的化学方程式______,“
”与氧化铁反应的化学方程式______,“![]() ”在此反应中体现______性.
”在此反应中体现______性.
查看答案和解析>>
科目: 来源: 题型:
【题目】请你根据自己所学化学知识回答下列问题:
(1)合成橡胶、棉花、聚乙烯塑料、蚕丝等都是人们生活和生产中常见的有机材料,其中属于天然有机高分子材料的是______。废旧塑料造成的污染被称为“______”。
(2)车用乙醇汽油是将乙醇和汽油以一定的比例混合而成的一种汽车燃料,乙醇完全燃烧的化学反应方程式为______。
(3)过量排放CO2会导致“______”。研究表明:CO2可用来合成多种有机物,在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水,在该反应中CO2和NH3的质量比为______(填最简整数比)。人体排泄的尿液中也含有尿素,它通常是由______(填:“糖类”或“油脂”或“氨基酸”或“维生素”)氧化而成的。
(4)SO2、CO2、O3、NO2几种气体中会导致酸雨的是______,用pH试纸测定雨水酸碱度的具体操作是______。酸雨会造成土壤酸化,人们常用熟石灰来改良酸性土壤,其利用的原理是______;长期使用化肥K2SO4也会导致土壤酸化,用BaCl2溶液可以区分K2SO4和KCl两种钾肥,试写出其对应的化学方程式______。
查看答案和解析>>
科目: 来源: 题型:
【题目】CaO2在渔业有广泛的应用,它与水反应的原理为:aCaO2+bH2O=cCa(OH)2+dX.向14.4gCaO2中慢慢滴加水,反应过程中CaO2、Ca(OH)2的质量随加入水的质量变化如图所示,下列说法不正确的是

A. 由反应可知,![]() 可以用作鱼塘增氧剂B. 化学计量数
可以用作鱼塘增氧剂B. 化学计量数![]()
C. 完全反应后,生成X的质量为![]() D. 化学方程式中a和b的比为1:2
D. 化学方程式中a和b的比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com