
科目: 来源: 题型:
【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
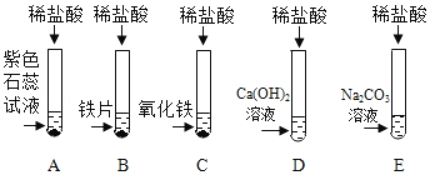
(1)A试管中的实验现象为_____,C试管中所发生反应的化学方程式为_____。
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
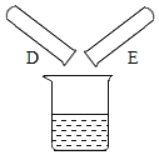
(提出问题)滤液中溶质的成分是什么?
(作出猜想)猜想:NaCl
猜想二:NaCl和CaCl2
猜想三:_____
猜想四:NaCl、Ca(OH)2和HCl
(进行讨论)经过讨论,同学们一致认为猜想_____是错误的。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液。 | _____ | 猜想二不成立 |
取少量滤液于试管中,滴加_____(填名称)。 | _____ | 猜想三成立 |
(迁移拓展)稀盐酸、稀硫酸有一些相似的化学性质,是因为在不同的酸溶液中都含有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学符号或者化学式填写:
(1)2个氢原子______。
(2)硫酸钠溶液中的阴离子______。
(3)波尔多液中的盐______。
(4)三氧化硫中硫元素的化合价______。
查看答案和解析>>
科目: 来源: 题型:
【题目】为粗略测定某石灰石中碳酸钙的含量进行如下实验。(装置气密性良好,杂质不参与反应)
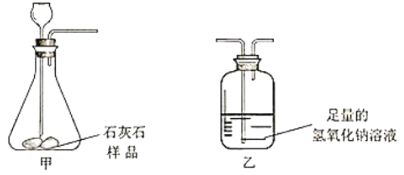
步骤I:称量装置甲和盛放的石灰石样品的总质量;装置乙和盛放的氢氧化钠溶液的总质量。步骤II:连接装置甲和乙,盐酸由长颈漏斗加入到锥形瓶中至气泡不再产生为止。
步骤III:二氧化碳被完全吸收后,测得装置甲及其盛放的药品增重了37.8克;装置乙及其盛放的药品增重了2.2克。
(1)盐酸中的溶质是______(填写名称)。
(2)二氧化碳与氢氧化钠溶液反应的化学方程式是______。装置乙吸收的二氧化碳为______摩尔。
(3)该石灰石样品中碳酸钙物质的量_____。(根据化学方程式列式计算)
(4)实验中所加的盐酸溶质质量分数可能为______(选填编号)。
a 5% b 7% c 10%
(5)如所用的盐酸溶质质量分数过大,对碳酸钙含量测定结果的影响是______(选填“偏大”“偏小”或“无”),理由是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某废液中含硫酸铜、硫酸锌、硫酸亚铁,为回收硫酸锌及有关金属,设计如下流程。
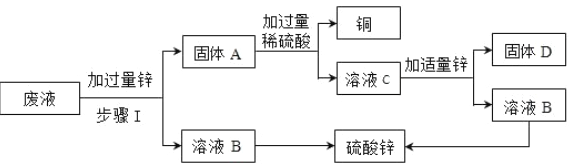
①硫酸锌属于______(选填“酸”“碱”或“盐”)。
②分离得到固体A和溶液B的操作名称是______。
③步骤I中反应的化学方程式是______。
④加入稀硫酸的目的是______。判断稀硫酸过量的方法是______。
⑤除废液外,上述流程中含铁元素的物质有______(选填编号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图装置可用于氯酸钾与二氧化锰混合制备氧气。
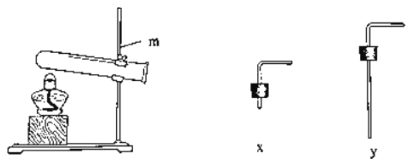
(1)仪器m的名称是______。试管与______(选填“x”“y”)连接,搭建氧气发生装置。
(2)氯酸钾与二氧化锰制备氧气的化学方程式是______,二氧化锰的作用是______。
(3)双氧水与二氧化锰混合也能制备氧气,有关该反应说法正确的是______(选填编号)。
a.生成两种单质
b.反应后液体中氢元素的百分含量增加
c.液体减少的质量等于生成氧气的质量
(4)实验室制取氧气选择的反应物在物质组成上的共同点是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】KCl有着广泛的用途。
①农业生产中KCl可用作______(选填“钾”“氮”或“磷”)肥。
②对KCl溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈______色。
③固体物质的溶解度与溶解性的关系下表所示。
20℃时溶解度(g/100g水) | >10 | 1~10 | 0.01~1 | <0.01 |
溶解性 | 易溶 | 可溶 | 微溶 | 难溶 |
20℃时,KCl属于______溶物质。
④20℃时,向三个分别盛有100g水的烧杯中,加入不同质量的KCl固体配制溶液。

有关上述溶液说法正确的是______(选填编号)。
a.I中溶质质量分数为20% b.I升温至40℃,溶质质量不变
c.II和III中溶质质量相等 d.III降温至10℃,析出固体45g
⑤写出鉴别KCl溶液和K2SO4溶液的一种方法______。
查看答案和解析>>
科目: 来源: 题型:
【题目】现欲探究一种固体混合物A的成分,已知其中可能含有NH4NO3、MgO、BaCl2、Na2SO4四种物质中的两种或多种,按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
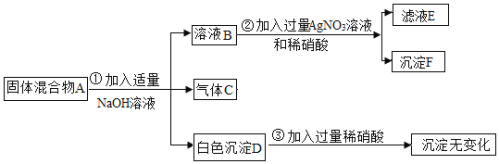
(1)气体C的气味为______,该气体溶于水,所得溶液______7(填“大于”“小于”“等于”之一)。
(2)滤液E中的溶质有______种,沉淀F的化学式为______。
(3)该固体混合物中一定存在的是______(写化学式)。
(4)溶液B中存在的酸根离子为______(写离子符号)。
(5)写出过程①中生成沉淀D的化学方程式______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
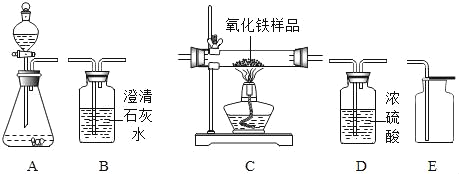
(1)以过氧化氢溶液和二氧化锰为原料制取并收集干燥的氧气,按照要求设计实验装置、连接仪器,并检验装置的气密性。
①所选仪器的连接顺序为_____(填写仪器序号字母)。
②制取氧气的化学方程式为_____。
(2)某化学兴趣小组的同学欲用CO气体(含有少量的CO2和水蒸气)测定氧化铁样品中Fe2O3的质量分数。现取2a g氧化铁样品进行相关测定,仪器的连接顺序为:CO气体→B1→D→C→B2→尾气处理(B1、B2为盛有澄清石灰水的洗气瓶)(假设杂质不发生反应,质量也不变化,各装置的作用都是充分的)。
①装置B1中观察到的实验现象为_____。
②反应结束后,若通过B2装置质量的变化进行测定,假设B2装置增重ag,则该样品中Fe2O3的质量分数为_____(结果精确到0.1%)。
③若不连接B1装置,通过测定反应前后C处大玻璃管的质量变化,来计算该样品中Fe2O3的质量分数。若其他操作正确,则计算结果将_____(填“偏大”“偏小”“不受影响之一)
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组的同学欲对石灰石样品进行探究,在烧杯中加入含CaCO3质量分数为80%的石灰石样品25g,然后逐滴加入稀盐酸,烧杯中石灰石样品的质量与滴入稀盐酸的质量关系曲线如图所示(假设石灰石中的杂质不反应,也不溶于水)。请根据题意回答下列问题。
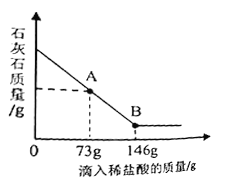
(1)人体缺钙会得骨质疏松症,CaCO3常作补钙剂,这里的“钙”是指钙______(填“元素”“单质”“原子”之一)该石灰石样品中CaCO3的质量为______。
(2)实验过程中观察到的一项明显现象为______。
(3)当滴入稀盐酸73g(即图中A点)时,烧杯中溶液里的溶质是______(写化学式)。
(4)当滴入稀盐酸146g(即图中B点)时,试通过计算求此时烧杯中所得不饱和溶液的质量____(计算结果精确到0.1g)。
查看答案和解析>>
科目: 来源: 题型:
【题目】生活在盐碱湖附近的人们习惯“夏天晒盐(NaCl)、冬天捞碱(Na2CO3)”。Na2CO3和NaCl两物质的溶解度曲线如图所示,据图回答下列问题:
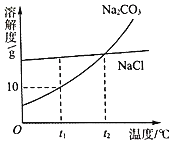
①t1℃时,将15g的Na2CO3加入100g水中可得到______(填“饱和溶液”“不饱和溶液”之一)。
②t2℃时,等质量的Na2CO3和NaCl两种物质的饱和溶液分别降温到t1℃,析出晶体后,此时得到______的溶液质量较大。
③检验“夏天晒盐”所得的NaCl样品中是否混有碳酸钠杂质的方法是______(请从稀盐酸、NaOH溶液、CaCl2溶液中选择一种试剂,并简述操作、现象及结论)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com