
科目: 来源: 题型:
【题目】用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的pH变化如图所示。
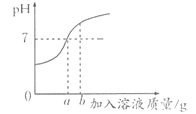
(1)写出该反应的化学方程式___________。
(2)该实验是将_____________________________滴加到另一种溶液中。
(3)当所加溶液的质量为bg时,写出此时溶液中溶质的化学式___________
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是初中化学中常见仪器装置,回答下列问题:
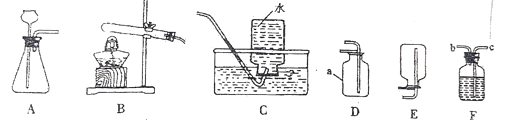
(1)D中仪器a的名称是______实验室用高锰酸钾制取氧气,可选用的发生装置为_____(选填装置编号,下同)。发生的化学反应方程式___________
(2)用大理石和稀盐酸制取并收集二氧化碳,可选用的发生装置是_______收集装置为_________,发生的化学反应方程式___________为防止气体从发生装置泄漏的必要措施是___________
(3)F装置有多种用途。用于气体干燥、除杂时,气体应从_______处进入(选填导管口编号)。干燥二氧化碳时,瓶中液体可以是___________(选填下列试剂编号,下同);除去一氧化碳中的二氧化碳时,瓶中液体可以是_______
①浓硫酸 ②烧碱溶液 ③稀硫酸 ④饱和碳酸氢钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确
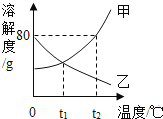
A. 甲的溶解度大
B. t1℃,甲、乙两种物质的饱和溶液质质量分数相等
C. t2℃时,向100g水中加入100g甲后形成溶液的质量为200g
D. 将t2℃甲、乙的饱和溶液分别降到t1℃时,两溶液的溶质质量分数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】今年三月五号,十三届人大二次会议在北京人民大会堂开幕。从李克强总理的政府报告中我们能深切体会到国家对于环境保护、环境治理的高度重视。在工业生产上规定空气中二氧化硫的允许排放量不得超过![]() ,否则将危害人类的健康,造成环境污染。某校学习小组欲利用“碘量法”测定扬州石化厂附近空气中的
,否则将危害人类的健康,造成环境污染。某校学习小组欲利用“碘量法”测定扬州石化厂附近空气中的![]() 的含量,请你参与并协助他们完成相关学习任务(部分装置图如下图所示)。
的含量,请你参与并协助他们完成相关学习任务(部分装置图如下图所示)。
(查阅资料)淀粉遇碘(![]() )变蓝,遇氢碘酸(
)变蓝,遇氢碘酸(![]() )不变色.氢碘酸为无色液体.
)不变色.氢碘酸为无色液体.
(测定原理)碘溶液吸收![]() 的化学反应原理是:
的化学反应原理是:![]()
(测定步骤)
①先准确称取1.27g粉末状碘(![]() ),并称取一定量的碘化钾(碘化钾可增大碘在水中的溶解度),加水使之完全溶解,配成1000mL碘水,准确称量取此溶液5.00mL并稀释10倍,再滴加2~3滴淀粉指示剂既得标准碘溶液。
),并称取一定量的碘化钾(碘化钾可增大碘在水中的溶解度),加水使之完全溶解,配成1000mL碘水,准确称量取此溶液5.00mL并稀释10倍,再滴加2~3滴淀粉指示剂既得标准碘溶液。
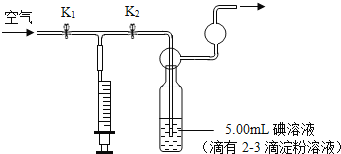
②准确量取标准碘溶液5.00mL倒入洗气瓶中待用(如上图)。则该标准碘溶液中所含碘的溶质质量分数为____________(本题中溶液的密度可看做1.0g/cm3)
③到指定的测试地点甲处抽气,抽气时应先关闭旋塞K2,打开旋塞K1,拉注射器活塞到100mL处,再_______________将气体缓缓全部推入标准碘溶液中,即完成一次抽气。每次抽气100mL,直到反应恰好完全反应为止,记录抽气次数(n)。
④在测试地点甲处,有三位同学分别做了实验,实验数据如下
测试地点甲处 | 小青 | 小白 | 小金 |
抽气次数n | 88 | 91 | 85 |
数据中__________(选填:小青、小白或小金)的最接近真实值,另两位同学不准确的原因为__________________。
⑤小组的其他同学再到不同地点再重复实验4次(每次所取碘溶液均为5.00mL)。这样做的目的是____________。5次实验的抽气次数记录见下表
测试地点 | 甲处 | 乙处 | 丙处 | 丁处 | 戊处 |
抽气次数 | 85 | 89 | 80 | 92 | 79 |
(交流与讨论)
(1)所配制的碘溶液显______色,实验中表明恰好完全反应的现象是__________。
(2)所配制的碘溶液浓度过浓,过稀都不合理,试分析浓度过浓不合理的原因是_________。
(3)通过计算,学习小组得出结论:扬州石化厂附近空气中![]() 的含量为____mg/l______(选填“超标”或“不超标”)
的含量为____mg/l______(选填“超标”或“不超标”)
(4)化工厂的含硫尾气处理后才能排放,下列物质中,能吸收![]() 的有______(选填字母)。
的有______(选填字母)。
A 氨水
B 酸性高锰酸钾溶液
C 熟石灰
查看答案和解析>>
科目: 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为![]() ,还含有硅、铝等杂质。制备流程如图所示:
,还含有硅、铝等杂质。制备流程如图所示:
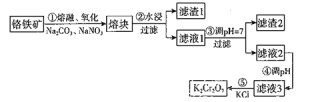
请回答下列问题:
步骤①的主要反应为:
![]()
(1)铬铁矿熔融氧化前要粉碎的目的是_______________________。
(2)滤渣1中含量最高的金属元素是_______,滤渣2的主要成分是氢氧化铝和含硅杂质。
(3)步骤④调节滤液2的PH使之变小,可以提高滤液中![]() 的浓度。
的浓度。
(4)有关物质的溶解度如下图所示。向“滤液3”中加入适量![]() ,蒸发浓缩、________、过滤得到
,蒸发浓缩、________、过滤得到![]() 固体。在温度为_________(填字母)时,得到的
固体。在温度为_________(填字母)时,得到的![]() 固体产品最多。
固体产品最多。
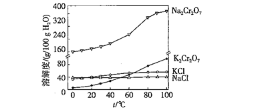
A 80℃ B 60℃ C 40℃ D 10℃
(5)步骤⑤主要反应的化学方程式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】感悟衣食住行中的化学魅力
Ⅰ.“慈母手中线,游子身上衣”
现在的衣服不仅仅有保暖作用,还有装饰美体的功能。

(1)这件大衣中的粘纤属于人造纤维,属于合成纤维的是__________(选填“羊毛”或“聚酯纤维”)。羊毛的主要成分是_________。
(2)如果衣服染上油渍,干洗店用干洗剂四氯乙烯除去油污的原理是________。(选填“乳化”或溶解”)
Ⅱ.“民以食为天”
扬州炒饭是我市特色美食。下表是每200g扬州炒饭所含主要营养成分
营养素 | 蛋白质 | 油脂 | 碳水化合物 | 维生素 | 铁 | 钙 |
含量 | 39.6g | 23.5g | 104.7 | 58.2mg | 25mg | 110mg |
(1)表中“钙 110mg”里的“钙”是指___(填字母编号)。
A 元素B 原子C 分子D 离子
(2)人如果缺乏维生素A容易引起________症。
(3)用化学符号表示:两个钙离子__________,一个水分子________。
(4)铁元素是人体必需的________元素。(选填“常量”或“微量”)
(5)碳水化合物是__________的俗称。
(6)植物光合作用的化学方程式是_____________________________。
(7)“自热米饭”的自加热原理:饭盒决层中的水与生右灰接触,反应放出大量热,该反应的化学方程式为____________________________________。吃不完的炒饭可以装进保鲜袋放入冰箱,这种保鲜袋是由________制成(选填字母:A. 聚乙烯 B.聚氯乙烯),它具有_______。(选填字母:A.热固性 B.热塑性)
Ⅲ.“安得广厦千万间”。
(1)钢筋混凝土保障我们的房子坚固、安全,它属于____材料(选填“无机”、“合成”、“复合”)
(2)合理的装修使我们的房子更温馨舒适,但是要预防甲醛污染;甲酵(CH2O)会使蛋白质_______引起中毒,在屋里放一些活性炭可以吸收甲醛,这是利用活性炭的______性,用酸性高锰酸钾溶液也可以吸收甲醛,请配平该化学方程式:
CH2O+___KMnO4+____H2SO4=_____CO2↑+____K2SO4+____MnSO4+____H2O
(3)厨房所用燃料---天然气的其要成分是______(填化学式),它完全燃烧的化学方程式是____________________。若观察到火焰呈黄色或橙色时,需孵灶具的空气进风口调____(大“或“小")。
Ⅳ.“门外迢适行路”
共享单车给我们的出行提供了极大的方便。单车的车架大多数是钢材质的,钢是铁和____的合金,铁在________的作用下容易生锈,若铁锈的成分用 ![]() 表示,请写出铁生锈的化学方程式_____________________________。
表示,请写出铁生锈的化学方程式_____________________________。
V.传承中华传统文化
下列是与化学有关的古代文献。其中理解错误的是___________。
A 《石灰吟》(明·于谦)中”...烈火焚烧若等闲....要留清白在人间”其中“清白”指氢氧化钙
B 《咏煤炭》(明·于谦)中“凿开混沌得乌金….不辞辛苦出山林”其中“乌金”主要成分是煤炭
C 《天工开物》(明·宋应星)中有记载:“以消石、硫磺为主。草木灰为辅。...魂散惊而魄齑粉”,文中提到的是火药
D 《淮南万毕术》(西汉刘安)中有描述:“曾青得铁则化为铜,文中的“曾青”指的是铜的化
合物
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们在学校一定做过这些实验,现提供下列装置:
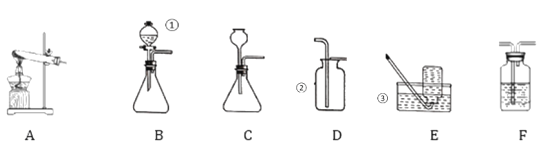
Ⅰ.实验室制备氧气
(1)请写出实验仪器的名称:①是________;②是_______;③是________。
(2)实验室用高锰酸钾制取氧气,发生装置A应做的改动是______,反应的化学方程式为______________________,若用E装置收集氧气,当有______时,开始收集气体。
Ⅱ.实验室制二氧化碳
(1)按照“C→F→F→真空气囊”的装置顺序制取纯净的CO2气体,C装置中发生反应的化学方程式为_____________,第一个F装置盛放试剂为______第二个F装置盛放的作用是__________________________________。
(2)若将C换成B装置,B的优点是_______________________。
Ⅲ.配制稀盐酸
(1)用市售浓盐酸(溶质质量分数为37%,密度为1.2g/ml)配制500g溶质质量分数为12%的稀盐酸,需要浓盐酸___ml(保留一位小数),量取水时应选用的量筒是____(选填字母)
A 100ml量筒 B 250ml量筒 C 500ml量筒
(2)下列操作中,可能导致配制稀盐酸的溶质质量分数偏大的是______(填字母)。
A 将浓盐酸导入量筒时,洒出少许
B 量取水时俯视读数
C 用不干燥的烧杯稀释盐酸
D 将配好的溶液转移到吸口瓶时,有少量溶液溅出
查看答案和解析>>
科目: 来源: 题型:
【题目】常温常压下,如下图所示的密闭容器中有一个理想活塞(滑动自如,且密封性好),处在容器体积的1/3处;其中,1/3的部分充的是空气,另2/3的部分充的是H2和O2的混合气体;当后者用电火花点燃引爆时,活塞先被冲到左边;而当容器内的气体逐渐恢复到原来的温度时,活塞渐渐向右边移动,最终停在容器容积的2/3处,则原来的氢气和氧气的体积比可能是(同温同压下)
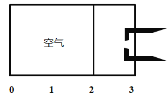
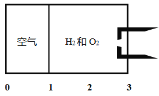
A. 3:1B. 7:2C. 4:5D. 1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某同学设计的“自过滤”器,能在无人在场的情况下实现顺利过滤,其中装置的关键是导管a和b的设计,下列设计能达到“自过滤”目的的是
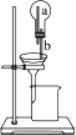
A. a的上端应该在圆底烧瓶中的液面以上,b的下端应在漏斗中的滤纸边缘以上
B. a的上端应该在圆底烧瓶中的液面以下,b的下端应在漏斗中的滤纸边缘以上
C. a的上端应该在圆底烧瓶中的液面以上,b的下端应在漏斗中的滤纸边缘以下
D. a的上端应该在圆底烧瓶中的液面以下,b的下端应在漏斗中的滤纸边缘以下
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com