
科目: 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图:
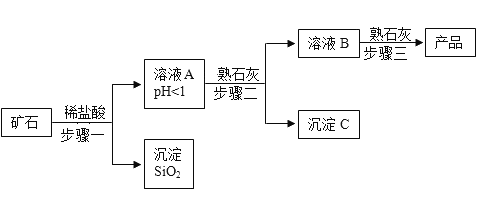
(注:在步骤二中,通过控制加入熟石灰的量,可使不同的金属离子先后生成沉淀)
(1)请写出步骤一中发生反应的化学方程式:_____(任写一个);
(2)溶液A中所含的非金属阳离子有_____(填离子符号);
(3)沉淀C的成分_____
(4)三个步骤中均用到的玻璃仪器是_____、_____、_____;
(5)步骤三中生成产品的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气是一种无色、有刺激性气味的气体密度比空气小,极易溶于水,溶液呈碱性。
氨气还原氧化铜的化学反应原理2NH3+3CuO![]() 3Cu+N2+3H2O。某研究性学习小组制取了氨气并验证氨气的某些性质(注:碱石灰是氢氧化钠和氧化钙的混合物,常用作某些气体的干燥剂),请回答
3Cu+N2+3H2O。某研究性学习小组制取了氨气并验证氨气的某些性质(注:碱石灰是氢氧化钠和氧化钙的混合物,常用作某些气体的干燥剂),请回答
I.制取氨气:
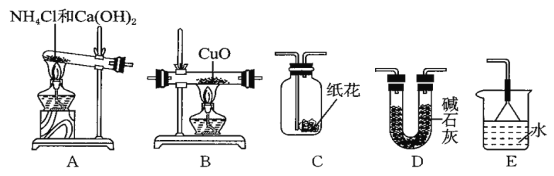
(1)A装置可制取氨气,同时生成水和一种盐,写出反应的化学方程式_____
(2)用A装置可制取氧气,试写出对应的化学方程式_____
Ⅱ.验证氨气的性质
请回答:
(3)为达成“氨气还原氧化铜”的实验目的装置A、B、D、E的正确连接顺序A、_____、_____、E;(填序号),为了保证试验成功,在装药品之前应该_____(填操作名称)
(4)装置B观察到的现象_____,装置E的作用_____;
(5)将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变蓝色,原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】最近,我国科学家成功合成新型催化剂,将CO2高效转化为甲醇(CH3OH)。这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如图所示。下列说法正确的是
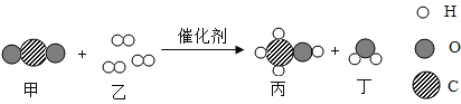
A. 丙的相对原子质量是32gB. 丙中C、H、O元素的质量比为3:1:4
C. 生成的丙和丁的分子个数为2:1D. 该反应为置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在“宏观一微观一符号”之间建立联系是化学学科特有的思维方式列图示信息的分析不正确的是对下
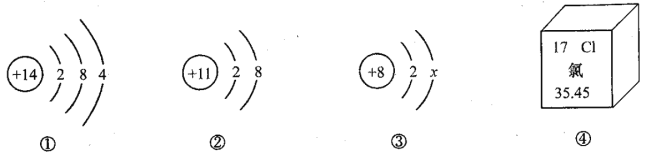
A. 硅单质是制造芯片的重要材料,图①是硅原子的结构示意图
B. 图③对应的元素属于非金属元素
C. 图②④对应元素组成的化合物是由分子构成的
D. 在化学反应中③的原子容易得到电子形成O2-
查看答案和解析>>
科目: 来源: 题型:
【题目】某硫酸厂欲测定排放的废水中硫酸的质量分数(假设废水中只含硫酸一一种溶质),取废水样品200g,逐滴加入溶质质量分数为5%的氢氧化钠溶液,废水中硫酸的质量随加入氢氧化钠溶液质量变化如下图所示,

(1)要配制100g5%的氢氧化钠溶液,需氢氧化钠固体质量为___________g;
(2)计算该废水中硫酸的质量分数为_____________(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
(查阅资料)
20℃时,几种物质在水中的溶解度见表:
物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
(实验探究)
(1)实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是_____。
(2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为_____。实验中不宜将BaCl2溶液换成CaCl2溶液的原因是_____。
(3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈_____色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚酞试液,理由是_____。
(4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中温度变化,结果如图所示。图中,AB段温度变化的原因是_____。
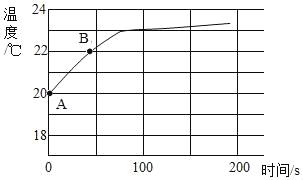
(反思感悟)
(5)实验从CO2减少、NaOH减少、Na2CO3生成等物质的变化,以及_____转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁、M是初中化学常见的化合物,其中甲、乙、丙、丁分属酸、碱、盐、氧化物中不同类别的化合物,M与甲属于同种类别的化合物。甲是石灰石的主要成分,它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件已略去,“一”表示物质之间能发生反应,“→”表示物质之间的转化关系)。
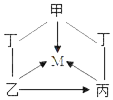
(1)甲的化学式为_____,M的化学式为_____;
(2)乙→丙的反应方程式为_____;
(3)甲→M的反应类型为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】从2012年中国第一艘航母“辽宁舰”入列到2018年第三艘航母在建,标志着中国海军从此迈入航母时代和海军发展强国,开拓中国新蓝海。

(1)“航母”舰体材料为合金钢。国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是_____(填字母)。
a合成材料
b复合材料
c金属材料
(2)“航母”升降机可由铝合金制造。用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到Al和O2,阳极区使用的石墨易消耗的原因是_____。
(3)“航母”螺旋桨可由铜合金制造。铜合金比铜的硬度_____(填“大”或“小”),铜比铁在海水中耐腐蚀的原因是_____。
(4)“航母”船体需做特殊防锈处理才能耐腐蚀。请写出生活中防止钢铁生锈的一种方法:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种不含结品水的固体物质的溶解度曲线如图:
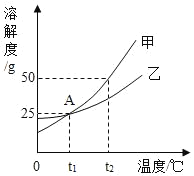
(1)A点的含义是_____。
(2)t2℃,将25g甲物质放入60g水中,充分溶解后,所得溶液是_____(填“饱和”或“不饱和”)溶液。
(3)t2℃,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水(温度不变)的是_____(填“甲”或“乙”)物质的饱和溶液。
(4)根据图中的溶解度曲线,下列说法正确的是_____。
A 温度由t2℃降到t1℃,含甲的溶液溶质质量分数一定减小
B t2℃时,可以配制溶质的质量分数为25%的甲溶液
C t2℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液先达到饱和
D 甲中混有少量乙,可用蒸发结晶法提纯甲
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图提供的实验装置回答问题:
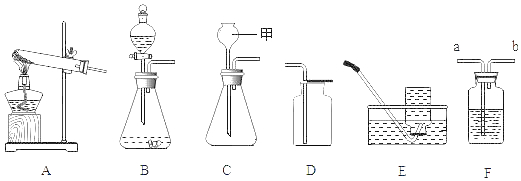
(1)图C装置中,甲仪器的名称是_____。
(2)实验室将双氧水加入二氧化锰粉末制取氧气,发生装置是_____(填序号),反应的化学方程式为_____,若用E装置收集氧气,当有_____时,开始收集气体。
(3)实验室可以按照“B→F→F→真空气囊”的装置顺序制取纯净的CO2气体,B装置中发生反应的化学方程式为_____,第一个F装置盛放试剂的作用是_____,第二个F装置盛放的试剂为_____,混合气应由_____端通入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com