
科目: 来源: 题型:
【题目】分子筛(又称为沸石,主要成分为水和硅铝酸钠)可作为催化剂或吸附剂等,以高岭土[主要成分为Al2(Si2O5)(OH)4]、烧碱等为主要原料生产分子筛的工艺流程如下:
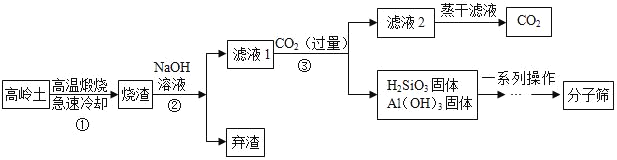
(1)步骤①所得烧渣中主要含有两种固体氧化物,分别为SiO2和___(写化学式)。
(2)步骤②加入NaOH溶液前需将烧渣粉碎,其目的是___。
(3)步骤②和③均涉及的操作是___,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、___。
(4)步骤③发生的反应之一是Na2SiO3溶液和通入的CO2气体反应生成偏硅酸(H2SiO3)沉淀和碳酸氢钠,该反应的化学方程式为___。
(5)上述流程中可以循环利用的物质(水除外)是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙晶体(CaO2xH2O)是优良的供氧剂,受热会逐渐失水,120℃时完全分解为CaO2,350℃时CaO2迅速分解为CaO和O2。
(一)【性质探究】取少量CaO2于试管中加过量稀盐酸,无气泡产生;再加少量MnO2粉末,产生大量气泡。静置、取上层清液,逐渐加入碳酸钠溶液,先产生大量气泡,再出现白色沉淀。
(1)CaO2和盐酸发生复分解反应的化学方程式为____________________________。
(2)加入碳酸钠溶液,产生的气体是______;出现白色沉淀,说明上层清液中含________。
(二)【制备流程】
方法1:由Ca(OH)2为原料制备CaO28H2O流程如下:
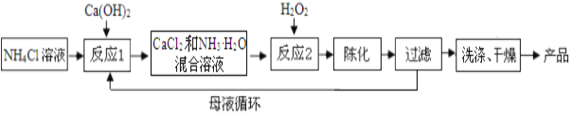
陈化:让初生晶体和母液放置一段时间,使晶体由小长大。
(1)将反应2及陈化的化学方程式补充完整:
CaCl2+H2O2+2NH3H2O+6_____=CaO28H2O↓+2NH4Cl。
(2)检验固体是否洗净的方法是:___________________________________。
(3)制备过程中除水外可循环使用的物质是:___________(填化学式)。
方法2:由鸡蛋壳(含较多CaCO3)为原料制备CaO28H2O流程如下:
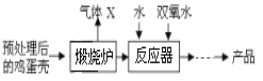
(4)反应器中由化合反应生成CaO2·8H2O,反应化学方程式为:_________________。
(5)在反应器中,应__________。
①先加水冷却后再加双氧水 ②先加双氧水冷却后再加水
(6)若煅烧充分,则获得的CaO28H2O中还含有的固体杂质是_______(填化学式)。
(7)“绿色化学”是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2·8H2O的反应符合“绿色化学”的是_________(填“方法1”或“方法2”)。
(三)【组成测定】若所得产品为CaO2·xH2O,下列装置可测定该产品的组成(样品中的杂质受热不反应)。
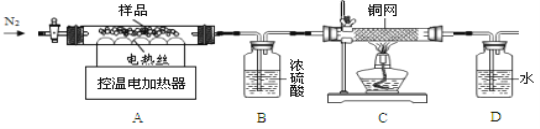
(1)实验前先缓慢通N2一段时间,控温将样品加热到350℃至CaO2分解完全;继续缓慢通N2,其目的是_________________________________(答一点即可)。
(2)装置B作用是________________(填序号)
①测定产生的H2O质量 ②便于观察和控制气流速度
(3)若2.7g样品,加热到350℃至CaO2分解完全,测得B装置重1.44g、C中铜网增重0.16g。
则x=________。
【反思】若先加热A,后加热C装置,测得X值______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组用下列药品和仪器,准备进行制取气体的实验。
药品:氯酸钾、块状石灰石、二氧化锰、稀硫酸、5%的过氧化氢溶液
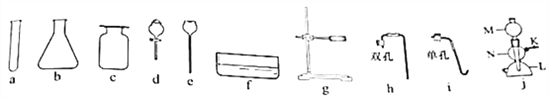
①写出仪器a的名称:____________。
②图j是启普发生器,下列说法正确的是________
A. 可作为固体和液体反应制取气体的发生装置
B. 可以打开或关闭活塞K,控制反应速率
C. 若加入液体过多,关闭活塞K,会导致固液无法分离
D. 若实验中关闭活塞K,N内液面不下降,可能需要补充反应物
③用5%的过氧化氢溶液和二氧化锰制取并收集氧气,为使反应较平稳的进行,需要的仪器是_______(选填仪器编号),反应的化学方程式是_________________。若用氯酸钾和二氧化锰制取氧气,除上述仪器外还缺少的仪器是______________。
④计算多少摩尔氯酸钾分解可生成0.96g氧气?_____________________(根据化学方程式计算)
⑤利用上述仪器和药品能否完成实验室制取二氧化碳的实验?若能,写出化学方程式;若不能请说明原因。_________________________________________________
⑥用wg氯酸钾和yg二氧化锰的混合物制取氧气,一段时间后停止加热,测得残余固体的质量为zg,产生氧气的质量为mg。为判断氯酸钾是否已全部分解,下列方法正确的是_____
A. 观察反应后固体颜色 B. 再加热,是否还有氧气产生
C. 计算W+Y-Z是否等于m D. 计算![]() 是否等于
是否等于![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】铅蓄电池在生产、生活中使用广泛,其构造如图所示。
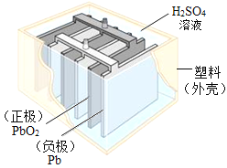
(1)铅蓄电池充电时是将电能转化为_____(填序号)
a.机械能 b.热能 c.化学能
(2)铅蓄电池的工作原理可以表示为:2PbSO4+2H2O![]() Pb+PbO2+2H2SO4。据此可知,铅蓄电池在放电时,溶液pH将不断填_____(“增大”“减小”或“不变”)。
Pb+PbO2+2H2SO4。据此可知,铅蓄电池在放电时,溶液pH将不断填_____(“增大”“减小”或“不变”)。
(3)从材料分类角度看,塑料属于_____材料。
(4)废硫酸直接排放会污染环境,用石灰浆处理废硫酸的化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】图中A、B、C、D、E、F分别表示六种物质,B、C、D、F分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前世界年产量最高的金属,B是可溶性银盐,D与E发生的反应属于中和反应(图中用“﹣”或“︵”表示两种物质之间能发生化学反应,用“→”或“![]() ”表示一种物质可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中各部分反应需在溶液中进行)。下列说法不正确的是( )
”表示一种物质可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中各部分反应需在溶液中进行)。下列说法不正确的是( )

A. D可能是Ca(OH)2
B. E转化为F发生反应的化学方程式可以是2NaOH+H2SO4═Na2SO4+2H2O
C. 上述反应中涉及了四种基本反应类型
D. B与C发生反应的实验现象是有白色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的有( )
①除去二氧化碳中混有的少量氧气,可以通入一氧化碳后点燃,将氧气转化为二氧化碳
②实验室用6%的氯化钠溶液配制3%的氯化钠溶液,量取6%的氯化钠溶液时俯视读数,若其他操作均正确,则所配溶液中溶质的质量分数大于3%
③某固体可能由氯化钠、硫酸钠、氯化钡、氯化镁、硫酸钾中的一种或几种组成,取少量该固体,加入足量的稀氢氧化钠溶液,产生白色沉淀,过滤,向沉淀中加入足量稀硝酸,沉淀部分溶解,则该固体的组成有5种情况
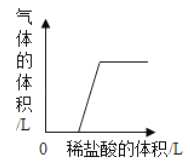
④某碳酸钠溶液中可能含有另一种溶质,取一定量该溶液,逐滴滴加稀盐酸,产生气体的体积与加入稀盐酸的体积关系如图所示,则该碳酸钠溶液中一定含有氢氧化钠
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验不能达到目的是( )
A. 探究金属的活动顺序
B. 测定空气中氧气的含量
C. 证明CO2不能燃烧、不能支持燃烧,密度比空气大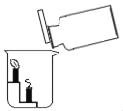
D. 证明分子不断运动
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲、乙、丙三种物质的溶解度曲线如图所示,但不知它们分别对应哪条曲线。根据以下信息
(1)甲和乙不可能配制成相同浓度的饱和溶液
(2)甲和丙中有一种物质,其接近饱和的溶液可通过升温达到饱和
(3)将t2℃三种物质的饱和溶液降温到t1℃,乙的溶质质量分数大于丙
下列说法正确的是( )

A. 曲线Y代表丙
B. t1℃时,三种物质的溶解度大小为:甲>乙>丙
C. t2℃时,分别将X、Y的饱和溶液降温至t1℃,X析出的晶体一定比Y多
D. t2℃时,等质量的甲、乙、丙饱和溶液中,甲的溶质质量分数最小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四种粒子的结构示意图中,说法正确的是

① ② ③ ④
A. 它们表示四种不同的元素
B. ②表示的元素在化合物中通常显+2价
C. ①③④表示的元素都是非金属元素
D. ①④表示的是阳离子
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为某反应的微观模拟示意图。下列从图中获得的有关信息中,不正确的是( )
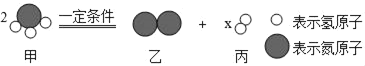
A. 图示中X的数值为3
B. 该化学反应类型属于分解反应
C. 该反应中分子和原子的种类都发生了改变
D. 该反应前后各元素的化合价都发生了变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com