
科目: 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列叙述中正确的是( )
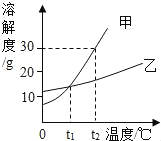
A. 甲物质的溶解度大于乙物质的溶解度
B. t1℃时,甲、乙两物质饱和溶液的溶质质量一定相等
C. t2℃时,将20g乙物质放入100g水中,所得溶液的质量为120g
D. t2℃时,等质量甲、乙两物质的饱和溶液降温到t1℃,析出晶体质量甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某化学兴趣小组。设计的金属活动性顺序的探究实验。
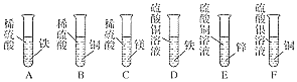
(1)上述实验中,有气泡生成的是________(填写装置序号)。
(2)试管F中出现的实验现象是______________。
(3)上述实验能否证明镁、锌、铁、铜、银五种金属的活动性强弱?____请说明理由_____。
(4)我国古代“湿法炼铜”就是利用了试管D中的反应原理,请写出该反应的化学方程式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业作出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。表格中是几种物质在不同温度时的溶解度:
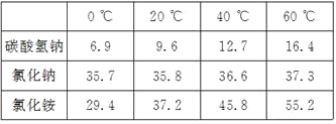
(1)从表中数据可以看出,温度对_____的溶解度影响不大。
(2)要使氯化铵饱和溶液中的氯化铵结晶析出,在____(填“较高”或“较低”)温度下进行比较合适。
(3)写出“侯氏制碱法”制碳酸氢钠的方程式_____。
(4)有人认为侯氏制碱法的优点有四:
A 生产过程中部分产品可选为起始原料使用
B 副产品是一种可利用的氮肥
C 反应不需要加热
D副产物不会造成污染环境
你认为其中正确的是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是费俊龙和聂海胜在“神舟”六号飞船中的照片,请你从化学的视角对“神六”飞船的有关信息进行思考并完成下列问题:

(1)航天员在太空中每人每天大约需要0.9kg氧气、2.5L水、0.6kg食物,排出1.0kg二氧化碳、1.8kg水蒸气等。上述物质中,属于单质的是____,属于化合物的是____,属于混合物的是___。
(2)“神六”飞船的外壳是用金属、玻璃、工程塑料等材料制成的。其中属于有机合成材料的是__。
(3)为了处理人体排出的CO2,飞船上采用了与氢氧化钠化学性质相似的氢氧化锂(LiOH)作为吸收剂。LiOH中锂元素的化合价是___,飞船上LiOH吸收CO2的化学方程式是:___。
(4)在“神六”飞船中有篮球大小的储氧瓶6个,储氮瓶2个,它们是航天员的生命之源。舱内空气一天一换。宇航员说:“舱内的空气比地面还好。”请你设计:怎样使得舱内气体成分大致和地面保持一致___?〔请注意题(1)所给信息〕。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。

(1)向固体乙上滴加盐酸时____________(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?(写化学式)__________________
(3)请写出该实验过程中所发生反应的化学方程式。______________________
查看答案和解析>>
科目: 来源: 题型:
【题目】金属材料在国防建设中起着重要的作用

(1)改装前的“辽宁舰”锈迹斑斑,钢铁锈蚀主要是铁与__的结果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为___。
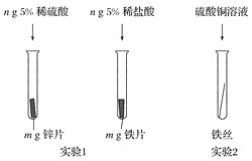
(2)为避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了下图的两个实验:
①实验1中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不合理,理由是____。
②通过实验2,可证明铁的活动性比铜强,反应的化学方程式是___。
(3)某电镀厂排放的污水中含有CuSO4、ZnSO4、FeSO4,为减少水污染及节约成本,回收重要物质硫酸锌及有关金属,设计如下所示流程。
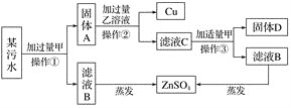
该回收流程中:固体A的成分是__;含铁元素的物质(污水除外)有__(填字母序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】将质量相等的甲、乙两块金属,分别放入质量和溶质质量分数均相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(反应后无固体残余)。下列分析正确的是( )
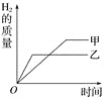
A. 金属乙反应后产生的氢气多一些
B. 金属乙的活泼性比金属甲强一些
C. 金属甲的反应速率比金属乙快一些
D. 反应后所得的溶液质量甲一定比乙小
查看答案和解析>>
科目: 来源: 题型:
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146 mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表
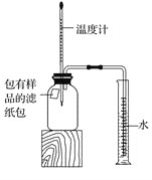
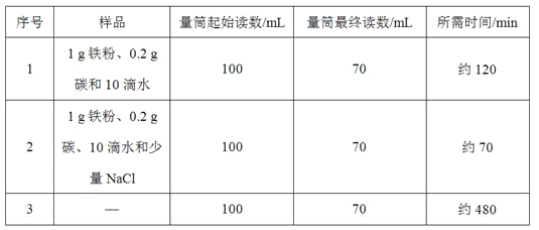
(1)实验①和②说明NaCl可以____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是______。
(4)已知碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成___。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是___(小数点后保留1位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)下图实验中,当试管1中气体的体积为6 mL时,试管2中气体体积约为___mL;电解时往往要加入少量稀硫酸或氢氧化钠,其作用是____。

(2)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300g25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为___g。
(3)甲、乙两物质的溶解度曲线如图所示。20℃时,将等质量的甲、乙两种固体,分别加入盛有10g水的A、B试管中,充分溶解后,可观察到如图所示的现象。则20℃__t℃(填“>”“<”或“=”)。
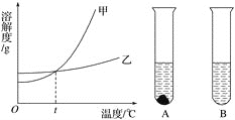
20℃时,对A试管进行如下操作,最终A试管中溶液的溶质质量分数一定发生变化的是__(填字母序号)。
a加少量水
b加入少量甲物质
c升温到40℃
d蒸发部分溶剂,恢复到20℃
e加入少量40 ℃甲的饱和溶液,恢复到20℃
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25 g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8 g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:

(1)当加入212 g稀盐酸时,放出气体的质量为___________g。
(2)碳酸钠样品中碳酸钠的质量分数为_____?(写出计算过程)
(3)加入106 g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为____?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com