
科目: 来源: 题型:
【题目】小明同学对所学部分化学知识归纳如下。其中不正确的是( )
A | 须辨清的物质 | B | 初中化学中常见的“三” |
干冰不是冰﹣而是固体CO2 纯碱不是碱﹣而是盐 | 三种常见还原剂CO、H2、C 三种基本粒子﹣﹣原子、分子、离子 | ||
C | 化学巨匠及其杰出贡献 | D | 符号中数字“2”的意义 |
张青莲﹣测量相对原子质量 侯德榜﹣﹣发明联合制碱法 |
2O:两个氧原子 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对“NaOH溶液与盐酸是否恰好完全反应”进行探究,请你参与他们的探究活动,并回答有关问题。
(实验探究)
(1)方案一:甲同学按如图所示的方法先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为_____色,证明NaOH溶液与稀盐酸恰好完全反应。
![]()
①请指出如图操作中的错误_____。
②写出NaOH溶液与稀盐酸反应的化学方程式_____。
(2)方案二:乙同学按照下面的方案进行实验证明盐酸与氢氧化钠恰好完全反应。
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,再滴加无色酚酞试液,充分振荡 | 没有明显现象 | 二者恰好完全反应,溶液显中性 |
(实验反思)
①方案一在滴入稀盐酸的过程中,若观察到曾有少量气泡出现,请分析产生气泡的原因可能是_____(写出化学方程式)。
②有同学提出方案二不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是_____。为此,还需要选择_____(填一种试剂),再进行实验即可。
(3)某化学兴趣小组为了测定某工厂废水中硫酸的含量,取100g废水于烧杯中,加入80g质量分数为10%的氢氧化钠溶液,恰好完全反应(废水中无不溶物,其它成分不参与反应),请计算:废水中硫酸的质量分数。_____
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)盛有石灰水的试剂瓶常有一层白色固体,该固体物质是怎样形成的_____?可以用什么方法除去_____?写出相应的化学方程式_____。
(2)实验室的废硫酸不能直接倒入下水道(为铁制管道)因为_____?
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入广口瓶中,振荡,一段时间后可见小气球a膨胀鼓起。下表中的各组物质不会出现上述现象的是( )
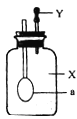
X | Y | |
A | CO | Ca(OH)2溶液 |
B | CO2 | NaOH溶液 |
C | HCl | Ca(OH)2溶液 |
D | SO2 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图,下列说法错误的是( )
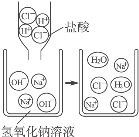
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
查看答案和解析>>
科目: 来源: 题型:
【题目】以硫酸镁与氯化钾为原料制备K2SO4的流程如下。

已知:20℃各物质的溶解度如表。
物质 | MgSO4 | MgCl2 | K2SO4 | KCl |
溶解度/g | 33.7 | 54.6 | 11.1 | 34.2 |
(1)沉淀池中相关物质的溶解度如表所示,写出沉淀池中发生的复分解反应的化学方程式_____,反应能在常温下发生的原因是_____。
(2)沉淀池中加入甲醇的目的是_____。
(3)操作b的名称是_____。进行操作b需要的玻璃仪器有烧杯、_____、_____、
(4)检验沉淀是否洗涤完全的试剂是_____。(填序号)
a氢氧化钠溶液 b氯化钠溶液 c稀硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】(一)2014年4月10日兰州发生自来水苯含量超标事件。
自来水人生产流程可简化如图:
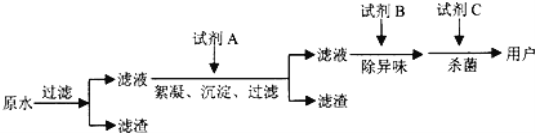
(1)流程中试剂A常用_____(填一物质名称,下同)试剂B常用_____,试剂C的化学名称叫二氧化氯,其化学式为_____。
(2)家庭常用煮沸的方法对水进行_____
(二)实验室用98%(密度为1.84g·ml—1)的浓硫酸配制60ml40%(密度为1.30g·ml—1)的稀硫酸。40%的稀硫酸溶液中溶质与溶剂的质量比为_____,配制时需要水_____mL(精确到小数点后一位)。量取浓硫酸时,若仰视读数(其他操作均正确),则所配稀硫酸的质量分数_____40%(填“>”或“=”或“<”),配制过程不需要的仪器是_____。
A托盘天平 B量筒 C烧杯 D玻璃棒 E胶头滴管 F铁架台
查看答案和解析>>
科目: 来源: 题型:
【题目】绿矾(FeSO4·7H2O)、硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]是重要的化工试剂。工业上常利用机械加工行业产生的废铁屑为原料制备绿矾、硫酸亚铁铵(如下图)。
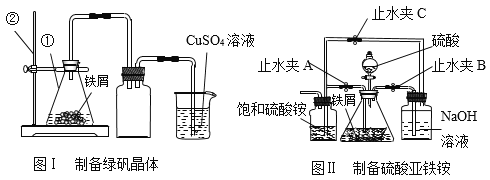
已知:
(1)废铁屑中含有FeS等杂质,FeS+H2SO4=FeSO4+H2S↑,生成的H2S气体有毒。
(2)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的小,冷却混合液至室温便析出硫酸亚铁铵。
(3)硫酸亚铁易被氧气氧化为硫酸铁,影响硫酸亚铁铵的等级。
请回答下列问题:
实验一:制备绿矾:
图Ⅰ中仪器①盛放的液体是_____,除了发生的反应FeS+H2SO4=FeSO4+H2S↑外,还发生的另一个反应的化学方程式是_____。广口瓶的作用是_____,烧杯中主要的反应是CuSO4+H2S=CuS↓+H2SO4,硫酸铜溶液的作用是_____;此处烧杯中的导管最好换成多孔球泡,目的是_____。
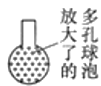
实验二:制备硫酸亚铁铵:
如图Ⅱ。实验步骤如下:
①连接仪器,_____
②制备FeSO4溶液:先关闭止水夹A,再打开止水夹_____,从分液漏斗滴入稀H2SO4至锥形瓶中。其中NaOH溶液中发生反应的化学方程式为_____,此过程中氢气的作用是_____。
③制备硫酸亚铁铵:待锥形瓶中的铁屑快反应完时,关闭止水夹_____,打开止水夹_____,不久会看到锥形瓶中的液体被压入饱和硫酸铵溶液中,放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体。
实验三:对所制得的硫酸亚铁铵样品进行加热
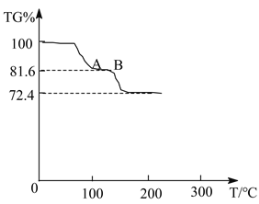
温度与TG%的关系如图所示,已知,200℃以前只有结晶水失去。[Mr(FeSO4·(NH4)2SO4·6H2O)=392],已知:TG%=![]() ×100%。
×100%。
TG%从100%降低为72.4%时,发生反应的化学方程式是_____。试计算AB段物质的化学式_____(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为实验室常用的实验装置,请回答问题:
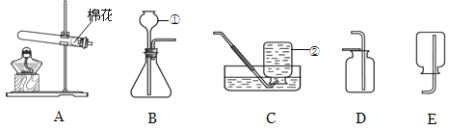
(1)写出带有标号仪器的名称:①_____;②_____;
(2)若用A、C装置组合制取氧气,实验中当观察到_____(填序号)时,开始收集气体。气体收集完毕时,应先_____(填序号);
a:水槽中导管口气泡刚一冒出 b:水槽中导管口连续均匀冒出气泡
c:熄灭酒精灯 d:从水中取出导气管
(3)写出一种能用B、E装置组合制取的气体的化学式_____;
(4)实验室制取二氧化碳时:①化学方程式为_____;
②在反应后的溶液中滴入几滴紫色石蕊,发现溶液变红色,则反应后的溶液中一定含有的溶质是_____
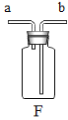
(5)若用如图F装置收集氧气,气体应从_____(填“a”或“b”)端通入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com