
科目: 来源: 题型:
【题目】钼具有高强度、高熔点、而腐蚀等优点,在工业上得到广泛的利用。图1是化工生产中制备金属钼的部分流程图(假设杂质不与空气反应)。
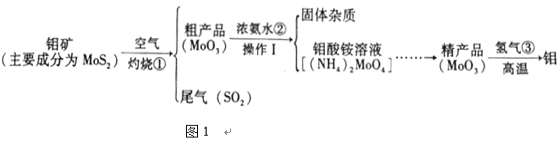
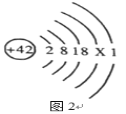
(1)钼是人体及动植物必需的_______________(选填“微量元素”或“常量元素”),原子的结构示意图2,其中X是_________________。
(2)步骤①反应的化学方程式_________________________________。
(3)下列物质可以用来吸收SO2尾气的是_________(填字母)。
A 氢氧化钠溶液 B 浓硫酸 C 氨水
(4)(NH4)2MoO4中Mo的化合价是_____________,在农业上既是钼肥又是_______肥。
(5)如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、________。
(6)利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂的质量比为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组做酸和碱的中和反应时,往NaOH溶液中滴入几滴酚酞溶液,发现溶液刚变
红瞬间又褪成无色。讨论并猜想。
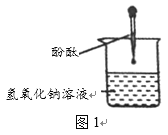
猜想一:可能是酚酞溶液变质
猜想二:可能与NaOH溶液的浓度有关
猜想三:可能是酚酞溶液在滴入过程中被O2氧化
……
(1)甲同学认为猜想一是不对的。其理由是_________________________。
(2)取3mL不同浓度的NaOH溶液,分别滴入3滴酚酞溶液,观察现象。得到NaOH溶液的浓度与酚酞溶液褪色时间关系如图2所示。
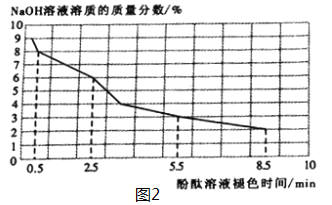
①根据图2所示,NaOH溶液溶质的质量分数________,酚酞溶液由红色褪为无色的时间越短。
②做酸和碱的中和反应时,滴加酚酞溶液的目的是________________________________。若用做实验的NaOH溶液溶质的质量分数为4%,完成该实验的操作时间应控制在_______之内。
(3)请设计实验,验证猜想三是否正确。
实验操作 | 实验现象 | 实验结论 |
__________ | 5.5min酚酞溶液褪色 | 酚酞溶液先变红后褪色与O2_______ (选填“有关”或“无关”) |
(4)探究酸碱中和反应时,逐滴加入稀盐酸的过程,并不断搅拌的目是_________________,写出该反应的化学方程式___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙是初中常见的物质,它们由H、C、O、Cl、Ca五种元素中的一种或几种组成。它们之间的关系如图所示,图中“→”表示物质间存在的转化关系,部分反应物、生成物及反应条件均已略去。
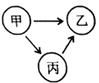
(1)若甲、丙组成元素相同,甲可用于实验室制取氧气。乙是___________,其主要用途有_____________________________________________(写一点)。
(2)若乙、丙组成元素相同,甲是一种黑色固体,常温下很稳定。丙转化成乙的化学方程式___
。
(3)若甲、乙、丙均含有金属元素,丙可用来改良酸性土壤。甲转化为乙的化学方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】微笑自行车、高铁、网购和扫码支付等方便我们的日常生活。
(1)微笑自行车的推行符合________环保理念。
(2)高铁车体外壳采用铝合金材料,是利用该合金的_________性能。
(3)许多商品的二维码印在PVC不干胶贴纸上,PVC是一种塑料。下列图标中表示塑料回收标志的是_________(填字母)。
A.  B.
B.  C.
C. 
(4)芯片是智能手机的核心部件,单质硅是由石英固体(SiO2)与碳在高温条件下反应制得,同时生成一种可燃性气体,该反应的化学方程式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为氢气与氯气反应的示意图。
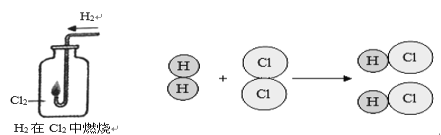
(1)集气瓶口出现白雾的原因是_______________________________________________。
(2)从微观角度分析能闻到刺激性气味的原因____________________________________;
该化学反应的微观实质是_________________________。
(3)该反应的化学方程为_______________________________________,基本反应类型__________________。
(4)从该反应谈谈你对燃烧条件的新识______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为实验室制取二氧化碳及验证其性质的实验(夹持装置略去)。
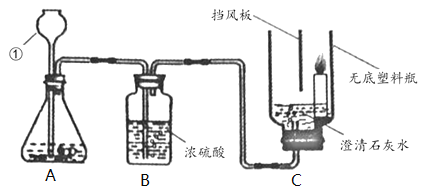
(1)仪器①的名称___________。
(2)装置A中发生反应的化学方程式为_________________________________________,实验室还可以用该装置制取_________________
(3)装置B中浓硫酸的作用_______________________________________。
(4)装置C中观察到的现象____________________,说明CO2具有的性质________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )
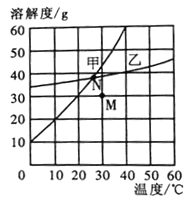
A. 40℃时,甲物质饱和溶液溶质的质量分数为60%
B. N点状态的甲、乙两种溶液中溶质的质量相等
C. 当乙中含有少量的甲,可用降温结晶法提纯乙
D. M点状态的甲溶液通过降温并加入甲物质可转化为N点状态
查看答案和解析>>
科目: 来源: 题型:
【题目】粗盐中除含有NaCl、泥沙外,还含有少量MgCl2、CaCl2、Na2SO4等杂质。某兴趣小组设计了如下实验除去粗盐中的杂质
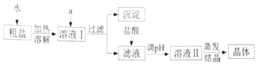
(1)试剂a包括:①过量的氢氧化钠溶液:②过量的氯化钡溶液;③过量的碳酸钠溶液。加入三种溶液的顺序是_____(填序号)。
(2)过滤后所得的沉淀中,除了泥沙外,还有_____(填化学式)
(3)过滤后,加入盐酸的目的是什么?_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F是初中化学常见的六种物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质。其相互反应情况如图所示(“一”表示相连的物质能发生反应,“→”表示一种物质能生成另一种物质)。

(1)A与C发生反应的基本反应类型为_____
(2)F转化为D的化学方程式为_____
(3)写出F的一种用途_____
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为甲、乙两种物质的溶解度曲线,根据图回答下列问题
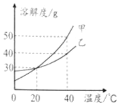
(1)40℃时相等质量的甲、乙的饱和溶液降温到_____℃,它们的溶质质量分数相等。
(2)40℃时,将30g甲物质加到50g水中,所得溶液中溶质的质量分数是_____
(3)40℃时,将70g乙的饱和溶液稀释为质量分数为20%的溶液,需加水的质量_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com