
科目: 来源: 题型:
【题目】用图所示装置研究二氧化碳的性质。其中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。
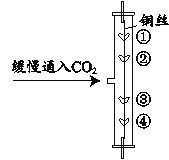
(1)说明CO2密度大于空气的实验现象为_____;除此之外,该实验还能研究的二氧化碳的性质是_____。
(2)某同学将变红了的棉球用吹风机烘干后,观察到棉球又变回紫色。但是,他认为此现象不足以说明“碳酸受热发生化学反应”,理由是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】走进“碳村庄”的格局如图1。
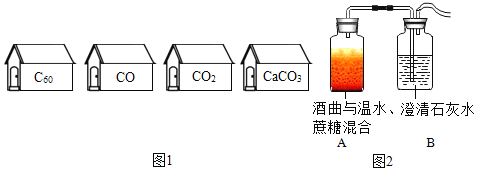
(1)“碳村庄”的居民中.属于单质的是______。
(2)大理石的主要成分是______。
(3)“碳村庄”中的部分居民可以相互转化。写出通过化合反应将CO转化为![]() 的化学方程式:______。
的化学方程式:______。
(4)“碳村庄”又来了一位新成员——蔗糖(![]() ),它在酒曲的催化下,经过发酵过程可以转变成酒精和二氧化碳。如图2所示实验中,可以说明该反应已经发生的现象是______,B中相应反应的化学方程式为______。
),它在酒曲的催化下,经过发酵过程可以转变成酒精和二氧化碳。如图2所示实验中,可以说明该反应已经发生的现象是______,B中相应反应的化学方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】页岩气是指蕴藏于页岩层中的天然气,是一种新开发的能源。
(1)页岩气的主要成分甲烷,其完全燃烧的化学方程式为_____。
(2)页岩气做燃料,对于降低空气中SO2含量,解决酸雨污染具有重要作用。酸雨形成过程中,其中部分SO2会在一定条件下转化成SO3,其微观示意图如下:
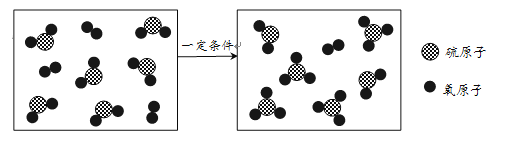
①该反应属于基本反应类型中的_____。
②反应消耗的O2与生成的SO3的分子数之比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】联欢会上,萌萌给同学们表演了魔术。她先向烧杯中倒入无水乙醇,将布手帕放入其中,完全浸透,取出手帕,轻轻挤干,用镊子夹住,从下方点燃,片刻后,手帕烧成灰烬(如图1所示)。之后,她向另一只烧杯中倒入白酒,取另一块材质、大小完全相同的手帕重复上述操作,火焰熄灭后,手帕依然完好如初(如图2所示)。已知:白酒由乙醇和水组成。

(1)白酒属于_____(填“混合物”或“纯净物”)。
(2)布手帕“烧不坏”的原因有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】小明做了一个名为“覆水可收”的兴趣实验。他将蜡烛粘在盘子的底部,向盘子中加入适量水,点燃蜡烛后,将玻璃杯倒扣在盘子中(如下图所示)。玻璃杯倒扣在盘子中后,相关分析不正确的是
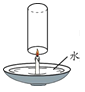
A. 一段时间后,蜡烛熄灭
B. 一段时间后,玻璃杯内水面上升
C. 水面高度不再改变时,玻璃杯内水面上方气体压强不再变化
D. 水面高度不再改变时,玻璃杯内水面上方气体只含有二氧化碳和水蒸气
查看答案和解析>>
科目: 来源: 题型:
【题目】膨松剂是一种食品添加剂,它受热分解产生的气体,能使面胚在焙烤过程中变得松软、多孔。碳酸氢钠(NaHCO3)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一。它既可以作为碱性膨松剂单独使用,也可以与酒石酸氢钾、淀粉按一定比例混合制成复合膨松剂。复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是

A. 任何受热分解能产生气体的物质都可以做食品膨松剂
B. 碳酸氢钠受热分解的化学方程式为:NaHCO3![]() CO2↑+ H2O + Na2CO3
CO2↑+ H2O + Na2CO3
C. 碳酸氢钠做膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D. 复合膨松剂应在干燥的环境中保存
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 加入足量锌粉 |
B | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
C | 检验蜡烛燃烧的产物中是否有水 | 在火焰上方罩一只冷而干燥的烧杯 |
D | 分离铜粉和铁粉 | 加水,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文(原文作者:许谦,有删改)
酸奶口感酸甜,营养丰富,是深受人们喜爱的一种乳制品。与普通牛奶比较,酸奶中的蛋白质和钙更易被人体消化吸收,是乳糖不耐症患者的良好食品。
通常的酸奶是将牛奶发酵而制成的。牛奶中主要含有蛋白质、乳糖和脂肪。在发酵过程中,乳酸菌把乳糖(C12H22O11)转化成乳酸(C3H6O3),使得牛奶的酸度升高。随着酸度增加,蛋白质分子互相连接,形成了一个巨大的“网络”,这个“蛋白质网络”把乳糖、水、脂肪颗粒都“网”在其中。所以,奶变“粘”、变“酸”了。

酸奶中含有大量活力较强的乳酸菌。乳酸菌可抑制某些腐败菌和病原菌的繁殖,从而维持人体内,尤其是肠道内正常的微生态平衡,促进食物的消化吸收。酸奶在储藏和配送过程中,乳酸菌的数量会因乳酸的过量积聚而明显减少,而酸奶的乳酸积聚又会影响到酸奶的酸度。有研究者选取某种市面常见的酸奶进行实验,数据如下表所示。
表某品牌酸奶酸度的变化
温度/℃ 时间/天酸度/°T | 4 | 28 | 37 |
0 | 67.7 | 67.7 | 67.7 |
2 | 73.9 | 77.1 | 79.2 |
4 | 76.4 | 82.7 | 86.3 |
6 | 85.5 | 92.2 | 98.9 |
8 | 90.2 | 98.7 | 113.2 |
1999年颁布的国标GB2746-1999中,对成品酸奶的酸度规定为“酸度不小于70°T”。按照一般人的接受程度,酸奶酸度不能超过100°T。
依据文章内容回答下列问题。
(1)乳酸是由乳糖转化生成的,请比较二者的化学式,分析它们的相同点和不同点。
相同点:_____。
不同点:_____。
(2)实验中所用酸奶若在37℃条件下储存,_____天后,酸度一定会超出一般人的接受程度。(填字母序号,下同)
A 2 B 4 C 5 D 8
(3)由表中实验数据可知,影响酸奶酸度的因素有_____。
(4)下列关于酸奶的说法正确的是_____。
A 酸奶适用于乳糖不耐症患者食用
B 酸奶放置时间越长,乳酸菌含量越高
C 酸奶中的乳酸菌对人类身体有害无益
D 酸奶变“粘”与蛋白质分子相互连接形成巨大“网络”有关
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液中的溶质质量分数,取出50.0克该溶液,向其中逐滴加入溶质质量分数为16.0%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:请回答下列问题:
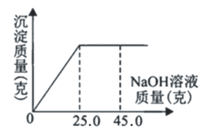
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算恰好完全反应时所得溶液中溶质的质量分数_____。(精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。
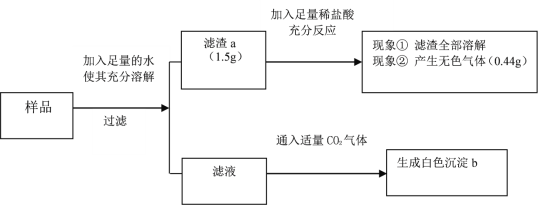
请回答下列问题:
(1)过滤操作中玻璃棒的作用是____________;
(2)加入足量的稀盐酸,滤渣a全部溶解的化学方程式为_________(若有多个反应,写出一个即可);
(3)样品中一定不含有的物质是___________(写名称或化学式均可,下同),滤液中溶质是__________;
(4)若现象① “滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品中不能确定是否存在的物质是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com