
科目: 来源: 题型:
【题目】下图为A~G(初中常见物质)的转化关系:
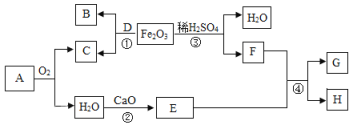
根据以上信息回答下列问题:
(1)若A是一种最简单的有机物,则其化学式是________。
(2)若反应①为置换反应,则该反应的化学方程式为_____________________________。
(3)写出反应②的化学方程式___________________________。
(4)反应③可应用于__________________(填一种用途),反应的现象是______________________。
(5)在图示转化反应中,属于复分解反应的是____________(填序号)。
(6)若A为其他的可燃性气体,则A中一定含有的元素是____________,且A_______(选填字母序号)
A只能是纯净物 B只能是混合物 C既可能是纯净物,也可能是混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下列各图中的有关信息,回答下列问题:

(1)仪器a、b的名称:a_________,b____________。
(2)用装置A制取氧气的化学方程式是_____________________________,若要收集到较纯净的氧气,应选用的收集装置是_____(填字母)。
(3)检查装置B的气密性时,向仪器b中注入水至形成液封,关闭活塞,再向仪器b中注入水,若观察到______________________________________,则该装置气密性良好。
(4)若用锌和稀硫酸反应制取氢气,则反应的化学方程式是________________________,用F装置收集氢气,气体应从_____端(填“c”或“d”)进入。
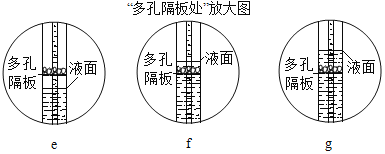
(5)用B装置制取气体时,若要使反应停止,应进行的操作是_____________;该操作后,B中多孔隔板处依次观察到的现象是___________(用字母e、f、g对如图进行排序)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活息息相关。观察,化学就在我们身边。请用所学知识填空:
(1)我们所说的“加碘食盐”,就是在食盐中掺入一定量的碘酸钾(KIO3),以补充人体所需的碘元素。碘元素是人体健康生命所必需的_____(填“常量”或“微量”)元素。人体缺碘或碘过量均会导致____________________。
(2)碘酸钾(KIO3)中碘元素(I)的化合价是__________。碘酸钾与氯酸钾相似,加热碘酸钾会分解,生成碘化钾和氧气。写出该反应的化学方程式___________________________。在加热过程中,生成的碘化钾还能与未分解的碘酸钾反应:5KI + KIO3 ![]() 3X + 3I2 ,其中X的化学式是________。因此,烹饪时不宜过早加入加碘盐。
3X + 3I2 ,其中X的化学式是________。因此,烹饪时不宜过早加入加碘盐。
(3)日常生活的牛奶包装盒、塑料袋都属于_____(填序号).
①金属材料 ②有机合成高分子材料 ③复合材料
(4)黄铜是铜与锌的合金,其硬度______(填“大于”或“小于”)纯铜。将足量的锌片放入硫酸铜溶液中,观察到_________________________的现象,说明锌比铜活泼。
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:
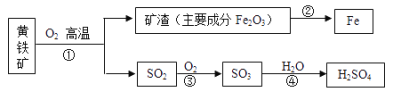
下列说法错误的是( )
A. 反应③和④可表示“硫酸型”酸雨的形成过程
B. 反应①中各元素的化合价均发生了改变
C. 可用石灰浆吸收该工业生产中产生的SO2:SO2+Ca(OH)2=CaSO4 + H2O
D. 向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
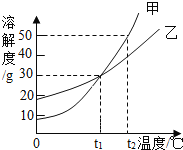
A. t1℃时,甲和乙的溶解度均为30
B. t1℃时,甲和乙的饱和溶液中溶质的质量相等
C. t2℃时,在100g水中放入60g甲,其溶质的质量分数为37.5%
D. t2℃时,分别在100g水中各溶解20g甲、乙,同时降温,甲先达到饱和
查看答案和解析>>
科目: 来源: 题型:
【题目】银杏果中含有银杏酸(化学式为C22H34O3),下列有关银杏酸说法正确的是
A. 银杏酸分子由碳、氢、氧三种元素组成
B. 银杏酸由22个碳原子、34个氢原子和3个氧原子构成
C. 银杏酸属于有机化合物
D. 银杏酸中氢元素的质量分数最大
查看答案和解析>>
科目: 来源: 题型:
【题目】MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
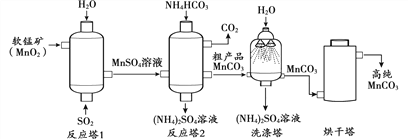
(1)反应塔1中的反应为:MnO2+SO2==MnSO4,其中化合价发生改变的元素是________。
(2)洗涤塔中喷水的目的是__________。
(3)烘干塔中需选择“低温”干燥的原因是_______________。
(4)上述流程中的产品除高纯MnCO3外,还有______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活息息相关,请用化学知识回答下列问题:
(1)用嘴吹能把燃着的生日蛋糕蜡烛吹灭,利用的原理是_____;
(2)当空气中悬浮着一定量的汽油时,一个小火星就足以使其燃烧,这说明汽油的着火点较_____ (填“高”或“低”);
(3)用墨书写或绘制的字画能够保存很长时间不变色的原因是_____;
(4)无定形硅为黑色粉末,可用镁与二氧化硅反应制取,其化学方程式为:SiO2+2Mg![]() Si+2MgO,该反应中还原剂是_____;
Si+2MgO,该反应中还原剂是_____;
(5)汽车是现代生活中不可缺少的交通工具,对汽车的部分钢铁部件进行喷漆可以防止其生锈,原因是_____.
(6)用石灰浆粉刷墙壁,干燥后墙面就变硬了,这是由于_____(用化学方程式表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】金属材料同人类文明的发展和社会的进步关系十分密切。
(一)铁的广泛应用
(1)人体缺铁会造成贫血,这里的铁是指_________。(选填序号)
A.单质 B.元素 C.原子
(2)双吸剂的主要成分是铁粉,作用是防潮和防氧化,原理是铁锈蚀,过程中吸收_______。
(3)暖宝宝的主要成分是铁粉、氯化钠等,原理也是铁锈蚀,锈蚀过程中发生__________。
A.剧烈氧化 B.缓慢氧化
(二)铁的冶炼
实验室用工业铁红(主要成分是Fe2O3,还含有少量的FeO、Fe3O4)模拟工业炼铁并测定铁红中铁元素的质量分数,进行了实验,装置如下:
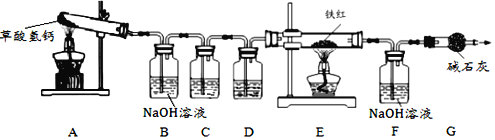
【资料】1.草酸氢钙是白色固体,化学式为Ca(HC2O4)2,加热易分解,生成四种氧化物
2.NaOH溶液能很好地吸收CO2,碱石灰能吸收CO2和H2O。
3.浓硫酸具有吸水性,是气体干燥剂。
【问题讨论】
(1)实验前应先________________。
(2)写出A中发生的反应化学方程式___________________。
(3)进入E中的气体是纯净、干燥的CO,则C、D中的试剂依次是_______、_______(选填序号)。
a.浓硫酸 b.澄清的石灰水 c. 氢氧化钠溶液
(4)C装置的作用是_________________。
(5)实验结束后,对E装置停止加热,继续通入CO至冷却,其目的是:______________。
(6)写出E装置中Fe2O3所发生的反应化学方程式________________。
(7)称取铁红样品7.0 g,用上述装置进行实验,测定铁红中铁元素的质量分数。
实验前后称得F装置增重4.4g,则此铁红中铁元素的质量分数是____________。
【实验反思】
1.本实验中如果缺少G装置(不考虑其它因素),则测得样品中铁的质量分数会_________(填“偏大”、“不变”或“偏小”)。
2.请指出上述实验装置的一个明显缺陷_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答问题。
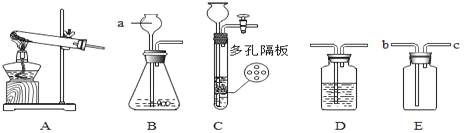
(1)图中标有a的仪器名称是_____。
(2)实验室用氯酸钾与二氧化锰的混合物制取氧气,选用的发生装置是_____(填字母),试管口略向下倾斜的原因_____,反应的化学方程式为_____。
(3)实验室用盐酸和锌粒制取氢气,反应的化学方程式为_____。若将B装置改进为C装置,其改进后的优点是_____。若用E装置收集氢气,则气体从_____端进入(填“b”或“c”)。若要除去氢气中混有的氯化氢,则D装置中可放入的试剂有_____(填字母)。
A 氢氧化钠溶液 B 碳酸氢钠溶液
(4)实验小组用如图装置进行以下实验。
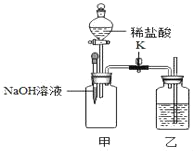
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。
①将胶头滴管中的浓NaOH溶液挤入瓶中,振荡,该反应的化学方程式为_____。
②打开K,观察到乙中导管口有气泡冒出,原因是_____。
③将分液漏斗中的稀盐酸注入甲中,观察到乙中的现象是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com