
科目: 来源: 题型:
【题目】硅的原子结构示意图及在元素周期表的信息如图,下列说法错误的是( )
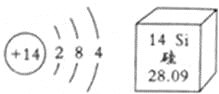
A. 硅属于非金属元素
B. 硅原子核内有14个质子
C. 硅原子核外有3个电子层
D. 硅的相对原子质量是28.09g
查看答案和解析>>
科目: 来源: 题型:
【题目】在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净后在天平上称得质量为56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉一起放在天平上称量,记录所称得质量m1.将上述铁钉浸到硫酸铜溶液中,待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质量为m2。
(1)m1_____m2(填“>”或“=”或“<”)。
(2)锥形瓶的质量为_____(用含m1或m2的代数式表示)。
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。_______
查看答案和解析>>
科目: 来源: 题型:
【题目】超市购物小票上含有BPA(双酚A),网上流传消费者接触小票会致癌。我国规定:超市购物小票上双酚A的含量应不超过0.6mg/Kg.按照这个标准,收银员即使每天接触小票10个小时,双酚A通过接触进入人体的量也不会比安全剂量低几十倍。因此,普通消费者一天接触几张购物小票,致癌概率是完全可以忽略不计的。
(1)双酚A的化学式为C15H16O2,其相对分子质量为_____。
(2)若每张超市购物小票的质量为5g,则其中含有双酚A的质量应不能超过_____mg才能符合国家标准。
查看答案和解析>>
科目: 来源: 题型:
【题目】菱铁矿和赤铁矿一样,也是工业上冶炼铁的一种矿物。某种菱铁矿中铁元素的主要存在形式是碱式碳酸亚铁,为测定碱式碳酸亚铁[xFeCO3yFe(OH)2zH2O]的组成,华雪同在老师的指导下设计了如图实验装置:
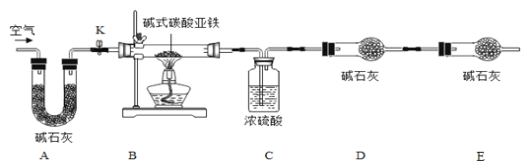
(查阅资料)
a.碱式碳酸亚铁受热会完全分解生成FeO、CO2以H2O。
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
(1)检查装置的_____后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接仪器。
(2)_____,鼓入一段时间空气,准确称量装置C、D、E的质量。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,缓缓通空气一段时间,这样操作的目的是_____。
(4)再次准确称量装置C、D、E的质量,所得数据如下
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 200.36 | 180.88 | 180.00 |
(5)分析图、表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H2O的质量为_____g,CO2的质量为_____g,装置E的作用是_____。
(实验结论)
在xFeCO3yFe(OH)2zH2O中,氢原子与氧原子的个数之比为_____。
(实验反思)
(1)装置A的作用是_____。
(2)实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe3O4.还可能是_____。
(3)为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g后,通过计算可知:残留固体的组成及各成分的质量为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选用的装置如图所示:
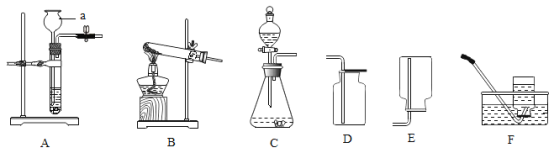
(1)写出仪器a的名称为_____。
(2)若要制取并收集一瓶CO2,不可以选择的装置是_____(填图中装置对应的字母)。
(3)CO2是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO2确实能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。请回答下列问题:
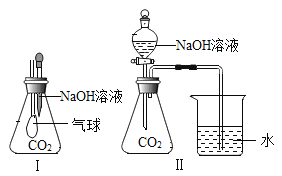
①选择装置I时,可观察到的实验现象为:_____。
②选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是:_____。
③CO2和NaOH溶液反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在汽油中加入适量的乙醇(C2H5OH)作为汽车燃料(车用乙醇汽油),可适当节省石油资源,并在一定程度上减少汽车尾气的污染。请回答下列问题:
(1)乙醇完全燃烧的化学方程式为_____。
(2)二氧化碳和水在一定条件下可发生反应,若反应属于化合反应,则在反应后的溶液中滴加紫色石蕊溶液,溶液呈_____色:若反应生成了葡萄糖,则反应条件为_____。
(3)C2H5OH在物质的分类上属于_____。
A 化合物 B 氧化物 C 碱 D 有机物
(4)甲醇(CH3OH)与乙醇_____(填“属于”或“不属于”)同一种物质。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化锌软膏可用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃疡。闪锌矿(主要成分为ZnS)是含锌的主要矿物质之一,高温煅烧闪锌矿生成氧化锌和SO2,以氧化锌产品为原料制备纯氧化锌的生产工艺流程如图:
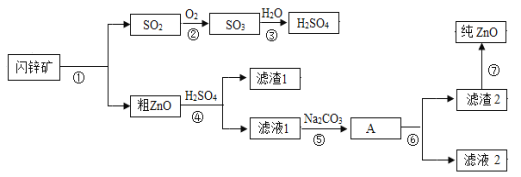
(1)已知A为硫酸锌和硫酸钠的混合物,则滤渣2的化学式为_____。
(2)上述步骤中,步骤⑥的操作是_____(填操作名称)。
(3)在上述步骤中,步骤_____发生的反应属于分解反应。
(4)步骤④中发生的反应化学方程式为_____(提示:ZnO与酸反应和Fe2O3与酸反应类似)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为KNO3和NaC1的溶解度曲线,下列说法不正确的是( )
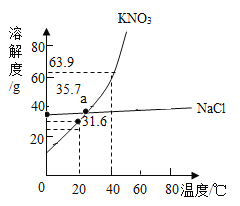
A. 20℃时,KNO3的溶解度为31.6g
B. a点处KNO3和NaCl两种溶液中溶质的质量分数相等
C. 40℃时,100g水中可溶解KNO3固体63.9g
D. 0℃时,NaC1饱和溶液中溶质的质量分数为35.7%
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒,如图为过氧乙酸的分子结构图(其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,
代表氢原子,![]() 代表氧原子),下列有关说法正确的是( )
代表氧原子),下列有关说法正确的是( )
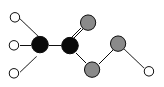
A. 过氧乙酸的化学式是CH3COOOH(或C2H4O3)
B. 过氧乙酸是由碳、氢、氧三种元素构成的
C. 过氧乙酸中碳、氢、氧三种元素的质量比是12:1:16
D. 过氧乙酸中碳元素的质量分数是40%
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们总结了氧气和二氧化碳的实验室制法,并利用下列装置进行练习和拓展.
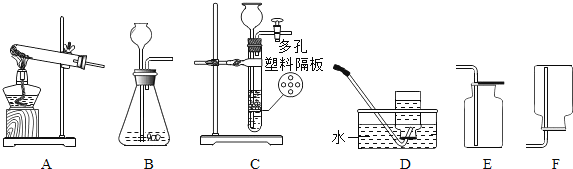
Ⅰ、知识总结:
(反应原理)
(1)用氯酸钾和二氧化锰混合加热制取氧气的化学方程式为_______________.
(气体制备)
(2)氯酸钾和二氧化锰混合制取氧气,选择的发生装置为______(填编号,下同).
(3)用于大理石与稀盐酸制取二氧化碳的发生装置C优于B的原因是______.
(气体收集)
(4)实验室收集CO2的装置是______,选择的理由______.
(实验步骤及注意事项)氯酸钾和二氧化锰混合加热制取氧气过程中:
(5)A装置中试管口略向下倾斜的原因是______;用排水法收集氧气,开始收集的适宜时刻是______.
(气体验满)
(6)检验CO2是否收集满的方法是______.
(气体检验)
(7)检验瓶中气体是否为O2的方法是______.
Ⅱ、知识拓展:
请仔细观察下列装置的特点并回答相关问题:
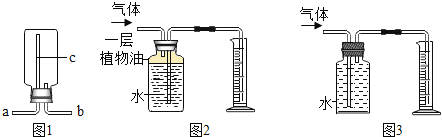
(8)①实验室若用图1装置收集氧气,则氧气应从______(口进入(填“a”或“b”);仪器c的名称是______.
②若要收集一定体积的二氧化碳气体,应选用______装置(填装置序号).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com