
科目: 来源: 题型:
【题目】某无色气体X可能常有氢气,一氧化碳、二氧化碳和甲烷四种气体中的一种或两种,为确认其组成,某间学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g,下列关于气体X成分的分析中,正确的是( )
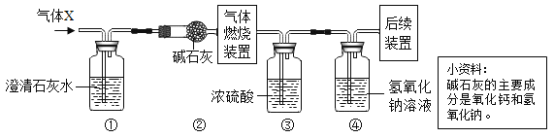
A.可能有二氧化碳B.可能同时含有甲烷和氢气
C.不可能只有甲烷D.可能含有氢气和一氧化碳
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温时,m克某物质溶液蒸发掉0.6m克水,能析出0.1m克不含结晶水的该物质的晶体,再蒸发0.1m克的水,又能析出0.lm克晶体,则原溶液中溶质的质量分数为( )
A.70%B.25%C.50%D.30%
查看答案和解析>>
科目: 来源: 题型:
【题目】有一部分潮解和变质的苛性钠样品Wg,为验证其变质的程度,将其加入98g质量分数为20%的稀![]() 中,充分反应后,再加入20g 20%的NaOH溶液恰好呈中性,则把溶液蒸干,可得固体的质量为( )
中,充分反应后,再加入20g 20%的NaOH溶液恰好呈中性,则把溶液蒸干,可得固体的质量为( )
A.28.4gB.l4.2gC.19.6gD.30.4g
查看答案和解析>>
科目: 来源: 题型:
【题目】金属A和非金属B可直接合成化合物AB,甲、乙、丙三人分别做A和B化合反应的实验,充分反应时各人所用A和B的质量不同,但总质量都是9g。甲、乙所用A和B的质量及三人得到化合物AB的质量如下表,请填写表中的空格。
A的用量 | B的用量 | 得到的AB的质量 | |
甲 | 7g | 2g | 6g |
乙 | 4g | 5g | 6g |
丙 | __________ | _________ | 7.5g |
查看答案和解析>>
科目: 来源: 题型:
【题目】将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2的质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( )

A.图线X表示镁的反应情况
B.铁消耗的稀盐酸的质量最大
C.镁、锌一定过量,铁可能反应完
D.镁一定过量,锌、铁可能反应完
查看答案和解析>>
科目: 来源: 题型:
【题目】在“绿色化学工艺”中,最好是反应物中原子全部转化为欲制得的产物。即原子的利用率为100%。在用![]() (丙炔)合成
(丙炔)合成![]() (2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和COD.
和COD.![]() 和
和![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法.正确的一组是( )
序号 | 物质 | 杂质 | 除杂应选用的试剂或操作方法 |
① |
| KOH | 加入 |
② |
|
| 加入足量铁粉 |
③ |
|
| 依次通过盛有浓硫酸和NaOH溶液的洗气瓶 |
④ | CaO |
| 加入稀盐酸,再蒸发 |
A.①④B.②C.②④D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是( )
A.NaCl、![]() 、
、![]() 、NaOH、
、NaOH、![]() B.
B.![]() 、NaCl、
、NaCl、![]() 、
、![]() 、HCl
、HCl
C.NaOH、![]() 、
、![]() 、
、![]() 、KClD.
、KClD.![]() 、HCl、
、HCl、![]() 、KCl、
、KCl、![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室获取氮气有多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(![]() )和氯化铵的混合溶液加热,氮元素全部转化为氮气。
)和氯化铵的混合溶液加热,氮元素全部转化为氮气。
进行试验时可选择的实验仪器如下图所示(省略夹持装置与加热装置)

(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用_______(填标号)。请写出生石灰在此反应中的两个作用:①_____________;②_____________。
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置______(填标号)_______中加入__________以除去其它杂质气体。
(3)方法三:写出制氮气的化学方程式_____________。
(4)在以上制取氮气的3中方法中,联合使用方法一和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价_____________。
(5)实验发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大。若上述实验设计与操作均无错误,且氮气己完全干燥,请介绍产生这一现象的原因_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】欲在室温和1.01×105Pa条件下测定镁的相对原子质量,请利用下图给定的仪器(盛放镁条的隔板有小孔)组装成一套实验装置(每种仪器只允许用一次)。请回答下列问题:
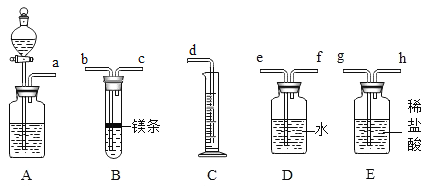
(1)装置A中的分液漏斗中盛放的液体是_______,其作用是_____________;
(2)假设气流方向由左向右,则各仪器的接口连接的先后顺序(填小字母) ________;
(3)连接好仪器后,要进行的操作有以下几步:①待仪器B中的物质恢复到温室时,测得量筒C中水的体积(若假设将测定的体积换算为标准状况下为VmL);②擦掉镁条表面的氧化膜,将其置于天平上称量(假定其质量为mg)并将其投入试管B中;③检查各装置的气密性;④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞。上述几步操作的先后顺序为_____________;
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所得镁的相对原子质量数据(选填“偏高”或“偏低”或“无影响”)_____________;
(5)若未擦净镁条表面氧化膜就进行试验,这将会使所测镁的相对原子质量数据(选填“偏高或“偏低”或“无影响”) _____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com