
科目: 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
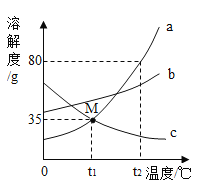
A. t1℃时a的饱和溶液,升温到t2℃时仍为饱和溶液
B. 降温可以使c的不饱和溶液变为饱和溶液
C. t1℃时,a和c的溶解度相等
D. t2℃时,在100g水中加入80gb能形成180g溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(![]() )]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(![]() )和氯化物(如
)和氯化物(如![]() )。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。

用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由__________转化生成的。
(2)室温下,用芹菜制作的泡菜,最佳食用时间是__________(填字母序号,下同)。
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(3)下列关于制作泡菜的说法中,合理的是__________。
A.最好加入一些姜汁 B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(4)请你为喜欢吃泡菜的人提一条食用泡菜的建议:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室现有氯酸钾、二氧化锰、石灰石、蜡烛、火柴及以下仪器(如图),请回答:
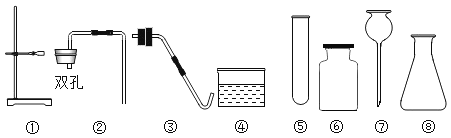
(1)仪器⑦的名称是____________;
(2)若补充一种常见仪器,并利用上述部分仪器和药品可制取一种气体,该反应的化学方程式是_______________。
(3)若补充一种药品,还能制取二氧化碳,并探究其性质(如图)
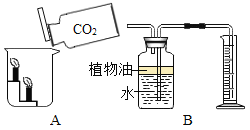
①补充的药品是_________________;
②图A观察到的现象说明二氧化碳具有的化学性质是______________;B中可用来测量生成二氧化碳气体的体积,其中在水面上放一层植物油的原因是______。
(4)2018年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考。
(提出问题)排污管道中的毒气有什么成分?
(查阅资料)
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
II.H2S气体能与CuSO4溶液反应生成黑色沉淀。
(提出猜想)小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO、CO2、H2S、CH4。
(实验方案)小组同学共同设计了如图所示的装置并进行探究(夹持仪器已省略)。
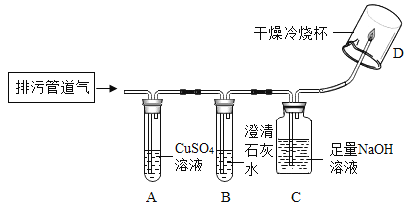
(问题讨论)
①如果A装置没有明显变化,则猜想__________成立;如果B装置没有明显变化,则猜想_________成立。
②要确证猜想4中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个____________装置。改进后,若气体燃烧,且D装置内壁出现__________,证明气体中一定含有CH4。
查看答案和解析>>
科目: 来源: 题型:
【题目】目前人类可以从多方面获取能源,我国在能源获取方面取得较大突破。
(l)氢氧燃料电池是一种新型电池。氧气可从空气中获取,氢气可通过以下反应获取: 2NaCl+2H2O![]() 2X+Cl2↑+H2↑ 。其中X的化学式是_________。
2X+Cl2↑+H2↑ 。其中X的化学式是_________。
(2)截止2017年6月2日,我国在南海神狐海域连续开采可燃冰超过22天。可燃冰(化学式CH4·8H2O)能释放出甲烷气体,是未来洁净的新能源。请写出甲烷燃烧的化学方程式:_______________。
(3)后面是水与其他物质之间的转化关系(反应条件及部分反应物已省去).其中属于化合反应的化学方程式为______________。 CH4→H2O→Ca(OH)2→H2O
(4)用水枪灭火的原理是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】M元素的一种粒子结构示意图是
(1)若M元素组成的单质是空气的成分之一,约占空气总体积的1/5,则该单质是 。
(2)元素的化学性质与其原子的最外层电子数有关。若x=9,M元素与下列 (填序号)的元素化学性质相似。
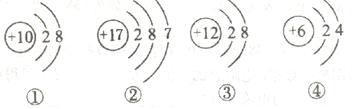
(3)若x=7,M元素的这种粒子可与上图中的一种粒子相互作用形成化合物,该化合物由离子构成。写出该化合物的化学式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于1/5。
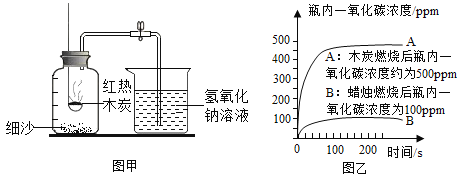
(1)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是___________;
(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为____同学的猜想不合理.
(查阅资料)
①木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%;
②一氧化碳不能被氢氧化钠溶液吸收;
乙同学又利用上述装置设计了如下实验,请你横线上填空。
实验步骤 | 实验现象 | 实验结论 |
1.将足量木炭点燃,迅速插入集气瓶中 | / | 木炭燃烧没有消耗完集气瓶中的氧气 |
2.待冷却后,将燃着的_________(填“棉花”或“蜡烛”)再伸入该集气瓶中 | _______________ |
(交流与反思)
(2)丙同学使用了一氧化碳浓度传感器测得木炭、蜡烛分别在密闭集气瓶里燃烧停止后,瓶内一氧化碳的浓度变化曲线如图乙。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因是_________;
查看答案和解析>>
科目: 来源: 题型:
【题目】用下图装置测定空气氧气的体积分数。实验步骤为:集气瓶里先装a体积的水,在酒精灯灯焰上把玻璃棒下端加热,装置如图密封。用力把玻璃棒按下与白磷接触,白磷燃烧,开始时瓶中少量水被压到烧杯中,稍后,烧杯内水又被压入瓶中,燃烧停止后,稍振荡,完全冷却后,量出集气瓶中水的体积(b)和整个集气瓶体积(c)。下列说法正确的是(_____)
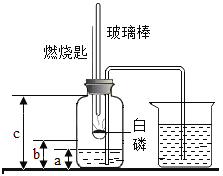
A反应过程中集气瓶内液面的变化是先下降后上升
B燃烧匙中的白磷可以换成细铁丝或镁条
C集气瓶中预先放的a体积水仅有液封导管,防止气体受热膨胀逸出的作用
D该实验测得氧气与空气的体积比为________(用a、b、c表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A~K是初中化学中常见的物质,C、H为黑色固体,J是人类使用最早的金属,它们之间的转化关系如下图所示,其中“→”表示能转化,“—”表示相互间能反应,部分条件已省略。请回答以下问题:
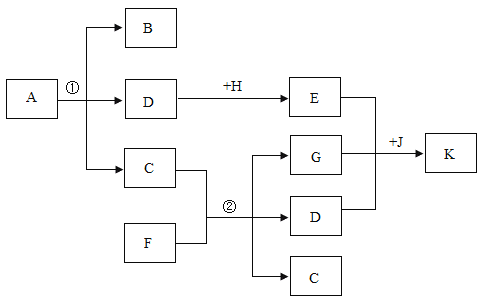
(1)写出物质D的一种用途:____________;
(2)写出E的一种化学性质:____________;
(3)写出反应①的符号表达式:____________;
(4)已知E、G、D、J在加热条件下发生化合反应生成物质K[化学符号为Cu2(OH)2CO3],写出该反应的符号表达式:____________;
(5)反应②的基本反应类型为:____________;
查看答案和解析>>
科目: 来源: 题型:
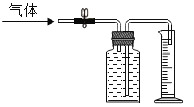
【题目】(1)若要收集含氧气的体积分数约为80%的气体。如图在集气瓶中装满水,塞紧胶塞并打开活塞通入氧气,当量筒中的水达到设定的体积V mL后立即通入空气,当量筒中的水的体积达到100 mL时,立即关闭活塞。则设定体积V约是_________mL(用整数表示,空气中氧气体积分数按照20%计算)
(2)小康欲称量5.6g胆矾用于实验,但是称量的时候砝码和胆矾放反了,这时托盘上的胆矾实际质量是_______g。
(3)某同学利用如图装置测定空气中氧气含量:
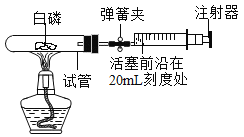
已知试管的体积为60 mL,注射器前沿停在20 mL处,关闭弹簧夹,对白磷进行加热,充分反应后,打开弹簧夹,注射器活塞将停在_______mL刻度处。
查看答案和解析>>
科目: 来源: 题型:
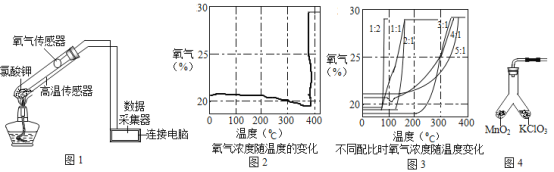
【题目】课后查阅资料后,小丽和小明利用如图1所示装置对氯酸钾制氧气进行了深入的探究学习。
资料:
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃.用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:
请回答问题:
(1)分析图2,氯酸钾熔点_______(填“高于”、“等于”或“低于”)其分解温度;
(2)分析图2,在氯酸钾分解前,传感器得到氧气浓度降低的可能原因是__________;
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是___________;
(4)为证实二氧化锰的催化作用,小丽利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查气密性 | 方法:___ |
Ⅱ | 分别在“Y”形管两侧支管中加入少量二氧化锰和氯酸钾,塞紧橡皮塞。 | 不填 |
Ⅲ | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星木条放在导管口。 | 加热左侧支管,可观察到___;加热右侧支管,可观察到木条较长时间才能复燃。 |
Ⅳ | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口。 | 加热后可观察到木条立刻复燃。 |
请回答:①步骤Ⅰ中检查气密性方法是:_________;
②完善步骤Ⅲ中的填空:加热左侧支管,可观察到___________;
③小丽认为根据步骤Ⅳ的实验现象就能说明二氧化锰是氯酸钾分解的催化剂,但小明不同意她的观点,小明认为还需证明在此反应中二氧化锰的_________不变。
后来在老师的指导下,小丽完善了实验方案,最终验证了自己的结论,则实验室利用氯酸钾和二氧化锰制取氧气的符号表达式为:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com