
科目: 来源: 题型:
【题目】实验室制取气体的装置如下图所示,根据所学的知识回答下列问题。
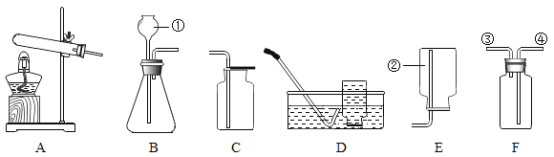
(1)图中标有①、②的仪器名称:① _____;② _____;
(2)写出用装置A制氧气的一个化学方程式____________
(3)用D装置收集氧气的依据是____;若用D装置收集氧气,检验氧气是否集满的方法是_____。
(4)若用装置F收集O2,则氧气从 ______ 端通入( 填接口序号);
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水。
①制取氨气反应的方程式:2NH4Cl + Ca(OH)2![]() CaCl2 + 2NH3↑+ 2 H2O。
CaCl2 + 2NH3↑+ 2 H2O。
②制取并收集NH3,应该从上图中选择的发生装置是_______,收集装置是______。
(6)一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2=2NO2,则收集一氧化氮气体时的收集装置是(填序号)______。
查看答案和解析>>
科目: 来源: 题型:
【题目】水是人类不可缺少的物质。
(1)净水时,通常用_____的方法,除去水中难溶性杂质,常用__________做吸附剂除去水中的色素和异味。家庭生活中降低水的硬度常用的方法是_________;
(2)电解水时,与正极相连的试管中收集到的气体是______;电解水的化学方程式为:_______。
(3)自来水中含有少量Ca(HCO3)2 等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。Ca(HCO3)2受热分解的化学方程式为:____________
(4)水的用途广泛,实验室常常需要用到水。请分析下图并回答有关问题:
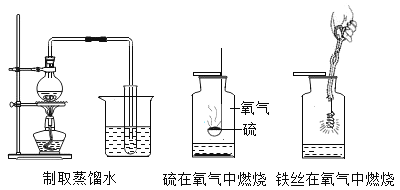
①制取蒸馏水时,烧杯内水的作用是________;
②硫和铁丝在氧气中燃烧,集气瓶内都盛水,前者瓶中水的作用是 _______而后者瓶中水的作用________;写出上述两个集气瓶中所发生的化学反应方程式____,_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)A中产生的气体是_____________。
(2)实验Ⅱ、Ⅲ证明:氧化铁的___________和____________在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(3)写出氧化铁催化过氧化氢溶液分解的化学方程式 ____________。
(实验评价)
(1)实验设计Ⅳ的目的是比较__________________。
(实验拓展)
(1)查阅资料得知:CuO、CuSO4、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是______________(填序号)。
A MnO2只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质不可能是其他反应的反应物或生成物
查看答案和解析>>
科目: 来源: 题型:
【题目】近来,乳酸(其化学式为C3H6O3)成人们研究的热点,在医药、食品等工业中得到广泛应用。
(1)乳酸分子的相对分子质量________。
(2)乳酸中碳元素、氧元素的质量比为________________
(3)乳酸中碳元素的质量分数_______________
(4)90克乳酸中碳元素的质量是____________.(计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】我国是燃煤大国,燃煤机组发电在我国一直占主导地位。煤燃烧产生大量污染物,如氮氧化物、二氧化硫等,对人体、环境和生态系统危害极大。近年来世界各国,尤其是工业发达国家都相继开展了同时脱硫硝技术的研究开发,并进行了一定的工业应用。尿素溶液可同时吸收氮氧化物、二氧化硫。总反应为:![]() 。
。
请回答下列问题:
(1)根据上述化学方程式,尿素溶液吸收![]() 、
、![]() 、
、![]() 质量比为______。
质量比为______。
(2)1000![]() 尿素溶液完全反应,吸收污染物得到硫酸铵132
尿素溶液完全反应,吸收污染物得到硫酸铵132![]() ,问所使用尿素溶液的溶质质量分数是多少?__________
,问所使用尿素溶液的溶质质量分数是多少?__________
查看答案和解析>>
科目: 来源: 题型:
【题目】在20℃时,将20g硝酸钾固体加入50g水中,搅拌充分溶解后,仍有4.2g硝酸钾固体未溶解。请填写下列空白:
(1)所得溶液是20℃时硝酸钾的________溶液(填“饱和”或“不饱和”)
(2)20℃时硝酸钾的溶解度为__________;
(3)所得溶液中硝酸钾的溶质质量分数为________(精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图1是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
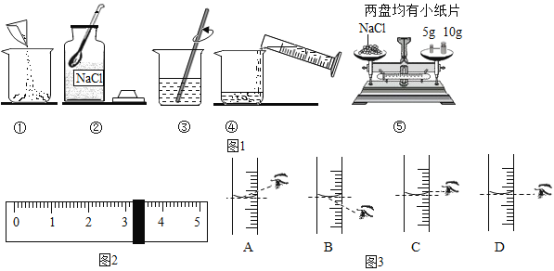
(1)图1中表示配制溶液的正确操作顺序:_________(用序号表示);
(2)图1③中玻璃棒的作用是____________;
(3)称量NaCl时,天平平衡后的状态如图1⑤所示,游码标尺示数见图2,则称取的NaCl质量为_______;根据题目要求和信息,计算需要量取水的体积是________(已知水的密度为1g/mL);读取量筒液体数值,若仰视读数,(其它步骤都正确)则所配制的溶液的溶质质量分数会______(填“偏大”、“偏小”或“不变”)
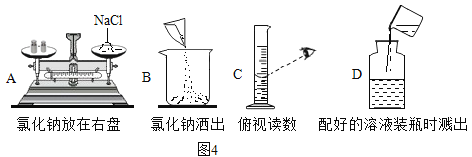
(4)分析图4中展示的四种错误操作,请你分析一定不影响溶液溶质质量分数的是操作是________(填操作序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】老师为同学们提供了如下实验装置:
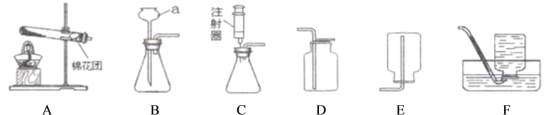
(1)写出仪器a的名称:________.
(2)实验室用加热高锰酸钾制取氧气时采用A装置作发生装置,写出高锰酸钾制取氧气的化学反应方程式__________。若要收集一瓶氧气,供“硫在氧气中燃烧”实验使用,收集装置最好选择F,理由是___________;__________。
(3)实验室利用锌粒和稀硫酸在常温下制取氢气发生装置可选用装置B或装置C,装置C与装置B相比,装置C的优点是_______;收集比较纯净的氢气应选择________(填装置字母)实验室制取氢气的化学方程为____________.
(4)如果改用氯酸钾和二氧化锰制取氧气,反应前后二氧化锰在固体混合物中的质量分数________(填“增大”、“减小”或“不变”)
(5)在通常情况下硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,密度比空气大。实验室可用硫化亚铁固体和稀硫酸在常温下反应来制取硫化氢。分析以上信息可知,实验室制取硫化氢应选用的装置组合是________(填字母)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线。
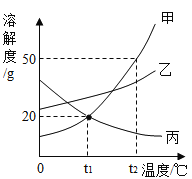
(1)要使甲物质的饱和溶液变为不饱和溶液,可将溶液的温度________(填“降低”或“升高”);
(2)甲中混有少量的丙,要提纯甲可以采用________(填“降温”或“蒸发”)结晶;
(3)![]() ℃时,将25g甲物质放入100g水中充分溶解。根据甲物质的溶解度曲线计算:未溶解的甲物质的质量是________g,所得溶液质量是________。
℃时,将25g甲物质放入100g水中充分溶解。根据甲物质的溶解度曲线计算:未溶解的甲物质的质量是________g,所得溶液质量是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们通过化学学习,了解了很多有关金属材料的知识,请你运用所学解决(或解释)以下问题。
(1)“沙里淘金”说明黄金在自然界中能够以________(填“单质”或“化合物”)形式存在。
(2)铁比金活泼,因此钢铁易腐蚀.工业生产中常对钢铁零件“发蓝”处理,以减缓其腐蚀。所谓“发蓝”,就是将钢铁零件等进行氧化处理,使其表面形成一层致密的蓝黑色氧化膜,其处理过程可表示如下:
![]()
经“发蓝”处理后的钢铁零件表面上的蓝黑色氧化膜能够减缓钢铁腐蚀的原因是________;发蓝过程的化学方程式![]() ,式中X的化学式为____.为检验处理后的成品表面是否形成致密的氧化膜常往其表面滴5%硫酸铜溶液一段时间。如果氧化膜不致密(铁部分裸露出来),将观察到红色物质,试写出反应的原理_______(用化学方程式表示)
,式中X的化学式为____.为检验处理后的成品表面是否形成致密的氧化膜常往其表面滴5%硫酸铜溶液一段时间。如果氧化膜不致密(铁部分裸露出来),将观察到红色物质,试写出反应的原理_______(用化学方程式表示)
(3)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜铁质船底镶嵌的金属是________(填选项)
A Pb(铅) B Cu C Pt(铂) D Zn
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com