
科目: 来源: 题型:
【题目】学完金属的化学性质后,小华用下列仪器和试剂验证影响金属与硫酸反应速率的因素:
仪器:烧杯、试管夹、酒精灯、药匙、托盘天平,镊子。
药品:铝丝、铁丝、铁粉、6%硫酸、25%硫酸。
Ⅰ、不同状态的金属与酸反应的速率不同
取质量相等的铁丝和铁粉,分别放入等浓度,等体积的稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图所示。

(1)为完成该实验,需要补充的一种仪器是_______ 。
(2)曲线B对应的物质是_____。
(3)请写出铁与稀硫酸反应的化学方程式:_______________。
(4)由此实验得到的结论是__________________。
Ⅱ、金属与不同溶质质量分数的硫酸反应的速率不同
取质量相等的铁丝,分别放入6%、25%的等量且足量稀硫酸中。请画出生成氢气的质量与反应时间的关系曲线图。__________
Ⅲ、______对金属与盐酸的反应速率也有影响
实验设计:___________
查看答案和解析>>
科目: 来源: 题型:
【题目】小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为15%.具体是什么物质无法辨认。老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种。
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是_____________
(2)小亮取少量样品于试管中,滴加______试液.试液变红色,该溶液不可能是_________,, (填写化学式),理由是________。
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告。
(设计实验方案)方案甲:选择氯化钙溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份。
(进行实验)你愿意选择方案_____ (选填“甲”或“乙”)进行实验。
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加 __________ | __________ | 该溶液是碳酸钠溶液。有关反应的化学方程式为: _____ |
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置回答问题。
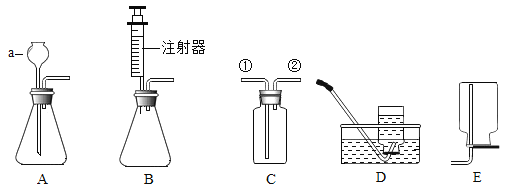
(1)图中仪器a的名称是___________。
(2)若用C装置来收集二氧化碳,二氧化碳应从______(填序号)端通入;若用B装置应来制取二氧化碳,优点为______。
(3) 丙烷(C3H8)是液化石油气的主要成分之一,燃烧产物与甲烷相同。请写出丙烷在空气中完全燃烧的化学方程式:__________
(4)纯净的丙烷无色无味,为防泄漏,需在家中安装报警器。你所选择的安装位置是________。(填墙角或者天花板)
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外研究小组通过下图所示两种不同的途径制取胆矾晶体。
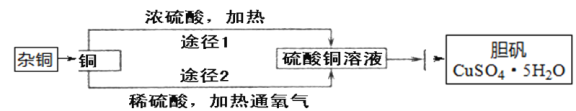
请回答下列问题:
(1)杂质铜中有含有少量的锌,可用_____浸泡几分钟的方法除去。
(2)通过途径2制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、________(填操作名称)、冷却结晶。请写出铜发生反应的化学方程式:_________。
(3)通过途径1制取胆矾的反应方程式为:Cu+2H2SO4(浓) ![]() CuSO4+2X+SO2↑,X的化学式为_______。与途径Ⅰ相比,途径Ⅱ的优点是__________(答出一点即可)。
CuSO4+2X+SO2↑,X的化学式为_______。与途径Ⅰ相比,途径Ⅱ的优点是__________(答出一点即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列生活物品中,所使用的主要材料属于合成材料的是____,属于金属材料的是______。 (填字母代号)

(2)不锈钢锅的组成元素之一碳属于_______(填“金属”或“非金属”)元素,日常生活中对铁制品的防锈除了制成不锈钢之外,还可以采取的措施是_________。
(3)围巾上的油渍可以用洗衣液清洗。该过程中洗衣液的作用是__________。
(4)塑料的不合理使用会造成白色污染,请说出防止“白色污染”的方法_________
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜是铜和锌的合金。向一定质量的黄铜样品中加入154.7g稀硫酸,恰好完全反应,产生0.2g氢气。
(1)求所用稀硫酸的溶质质量分数_____
(2)除了可求出稀硫酸的溶质质量分数外,你还能求出的化学量有_____。(填序号)
①锌的质量②铜的质量分数③锌的质量分数④硫酸锌的质量⑤硫酸溶液的体积⑥反应后溶液溶质质量分数,就其中一个量写出计算过程_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验时,有同学不小心放错了胶头滴管,使得NaNO3溶液的试剂瓶中可能混入NaCl、NaOH、Na2CO3和 Na2SO4中的一种或几种。为了验证,他进行了如图所示的实验。
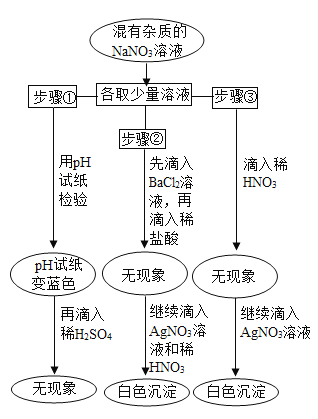
请回答:
(1)由步骤①得知,此溶液中含有(写化学式,下同)_____。
(2)由步骤②得知,此溶液中不存在_____。
(3)由步骤③得知,此溶液中含有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】结合下列各图装置,回答有关问题。
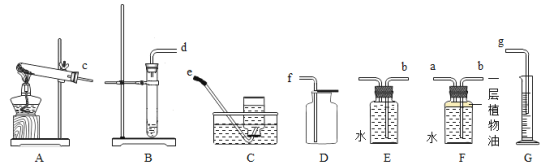
(1)实验室中,用加热高锰酸钾的方法制取氧气,发生装置可选用_____(填序号),该反应的化学方程式为_____。
(2)氢气是最清洁的燃料,密度比空气小,难溶于水,实验室常用锌粒与稀硫酸反应来制得。其制备氢气发生装置和收集装置可选用_____。(填序号)。
(3)实验室用石灰石与稀盐酸反应制备二氧化碳,并测定所收集的二氧化碳的体积,应选用的装置是(填序号)_____。
(4)用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的的是_____。
A 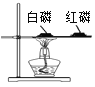 红磷、白磷着火点比较
红磷、白磷着火点比较
B 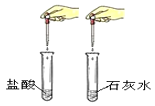 用碳酸钠溶液鉴别盐酸和石灰水
用碳酸钠溶液鉴别盐酸和石灰水
C 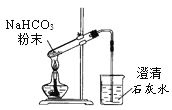 NaHCO3受热分解
NaHCO3受热分解
D 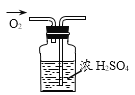 干燥O2
干燥O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化。请从图像中获取信息,回答下列问题:
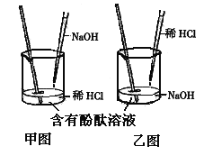
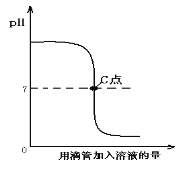
(1)进行该反应的实验操作是按照以上_____(填甲或乙)图所示进行,烧杯中溶液的颜色变化是_____。
(2)所发生的中和反应的化学方程式为_____。
(3)曲线上C点表示_____。
(4)用溶质的质量分数为36.5%的盐酸40g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液_____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】通过学习,我们可以从化学的角度看问题。豆浆机由于快捷方便而进入千家万户。请根据图示回答:
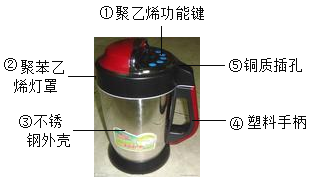
(1)制作材料中属于金属或合金的是_____(选填一种物质编号),属于有机合成材料的是_____(选填一种物质编号);
(2)制作手柄的塑料属于_____塑料(填“热塑性”或“热固性”);
(3)豆浆已成为众多家庭的早餐饮品,以下是豆浆中一些营养成分的平均质量分数。请根据下表回答:
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素A |
质量分数/% | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
①豆浆中含有的微量元素是_____;
②青少年缺乏_____元素易患有佝偻病。
③在豆浆所含的营养素中能供给人体能量的营养素有_____。
④若成年人每天食用90g豆浆,则摄入蛋白质的质量为_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com