
科目: 来源: 题型:
【题目】FeSO4·7H2O是一种重要的食品和饲料添加剂。某工业废渣主要成分是Fe2O3,还含有CaCO3和SiO2(既不溶于水也不溶于稀硫酸)。实验室用此废渣制备FeSO4·7H2O的流程如下:
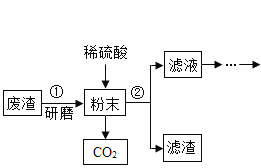
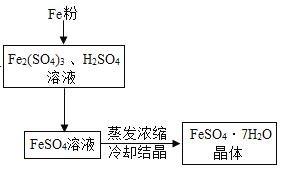
回答下列问题:
(1)废渣研磨的目的是_______
(2)稀硫酸与粉末中的氧化铁反应的化学方程式为_____。
(3)步骤②的操作名称是过滤,其中需要用到的玻璃仪器是烧杯、漏斗和__,经测定,滤渣中只含有CaSO4和SiO2。你认为实验室____(填“能”或者“不能”)用粉末状的石灰石与稀硫酸反应制二氧化碳。
(4)Fe与Fe 2(SO4)3反应的化学方程式为____。
(5)硫酸亚铁的溶解度曲线如图。
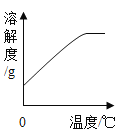
待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次。用冰水洗涤的目的是:
Ⅰ 除去晶体表面附着的杂质;
Ⅱ _______。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答相关问题。
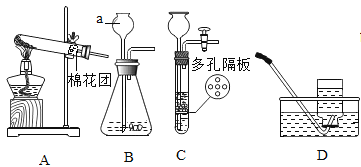
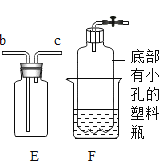
(1)图中标有 a 的仪器名称是____
(2)用高锰酸钾制取较纯净的氧气,装置组合是__(填字母),化学方程式为____,试管口放一团棉花的作用是__。
(3)实验室制取二氧化碳的化学方程式为___,
选择 E 装置收集二氧化碳,气体应从___(填“b”或“c”)端通入。小明组装了 F 装置用于制取二氧化碳,该装置能达到的效果相当于图中的__(填字母)装置,F 装置中的石灰石可用_________(填字母)替代。
A 大理石
B 洗净的鸡蛋壳
C 苏打粉
(4)在20mL溶质质量分数为1.60%的硫酸铜溶液中,逐滴加入某浓度的氢氧化钡溶液,用电导仪测得溶液的电导率(电导率越高表示溶液的导电性越好),如图所示。溶液的pH随滴入Ba(OH)2溶液体积的变化曲线(假设所有稀溶液的密度均为l g/cm3),如图所示:
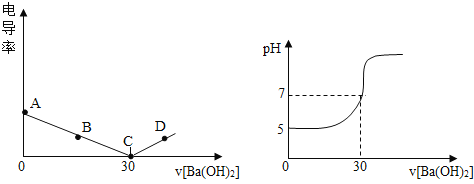
①硫酸铜和氢氧化钡溶液发生反应的化学方程式为:_________。
②图中C点所示溶液中,含量较多的微粒是水分子,D点所示溶液能导电是因为溶液中含有_______(填粒子符号)。
③由图可知:将打磨过的铝片放入上述硫酸铜溶液中,可以观察到的现象是:铝片表面有红色物质生成,溶液由蓝色逐渐变无色,同时还可以看到 ___。
查看答案和解析>>
科目: 来源: 题型:
【题目】我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分。
(1)用合适的化学用语填空。
①幼儿和青少年缺______会得佝偻病及发育不良;
②不同的碱溶液具有相似的化学性质,是由于溶液中都含有相同的_____ ;
③西气东输的气体的主要成分为________;
④车用铅酸蓄电池中的酸是_________
⑤纯碱不是碱是一种盐,这种盐是_________
(2)汽车是现代生活中重要的交通工具。请回答下列问题:
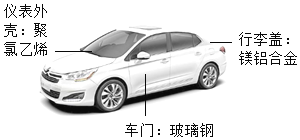
①玻璃钢属于________(填“金属材料”或“复合材料”或“合成 材料”)。
②家用汽车燃料通常是汽油,它是利用石油中各成分的_______ 不同而分离得到的。
(3)下列化肥中,属于复合肥料的是_____(填序号)。
a NH4Cl
b Ca(H2PO4)2
c KNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体物质可能含有硫酸钠、碳酸钠、氯化钙、硫酸铜、氯化钾和氢氧化钾中的一种或几种。为探究其组成,进行如下实验,流程和现象记录如下:
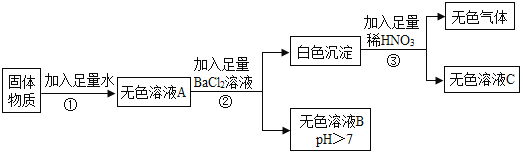
(资料)氯化钙、氯化钡、氯化钾三种溶液均呈中性
下列推论正确的是
A.原固体中一定含硫酸钠、碳酸钠
B.原固体中一定含碳酸钠,氢氧化钾,可能含氯化钾
C.此流程共发生三个复分解反应
D.原固体中一定含碳酸钠、氯化钾,可能含氢氧化钾
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是
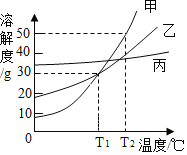
A.T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙
B.T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和
C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲
D.T1℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】理科实验操作考试中,小明同学在做铝和稀盐酸反应时无意中加入硫酸铜溶液,发现铝片表面上产生气泡速率明显增快,对此他产生了兴趣。
(提出问题)硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
(设计实验1)室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10﹪稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率。
实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
硫酸铜饱和溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(1)上述表格中V=__________。
(2)写出铝和稀盐酸反应的化学方程式__________。
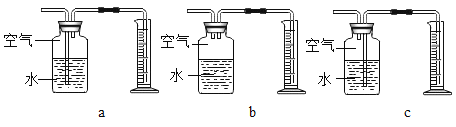
(3)定量收集氢气体积可用如图__________(填字母序号)装置。
(实验现象)随着硫酸铜溶液体积的增加,产生氢气的速率先快后慢,且铝片表面附着的红色物质逐渐增加。
(结论与解释)
(4)随着硫酸铜溶液体积的增加,反应速率明显变慢可能的原因是_______________。
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是______________。
(实验反思)加快铝和稀盐酸反应速率还可以采取的措施是(写一点)_____________。
(设计实验2)根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10﹪稀盐酸混合后加入不同的盐溶液,实验现象如下(加号越多,代表反应速率越快)。
实验 | ① | ② | ③ | ④ | ⑤ |
加入试剂0.5mL | 水 | 5﹪NaCl溶液 | 5﹪Mg(NO3)2溶液 | 5﹪FeSO4溶液 | 5﹪CuSO4溶液 |
产生气泡速率 | + | + | + | ++ | +++ |
(6)上表中,用水进行实验的目的是_______________。
(7)上述实验设计存在有缺陷,该缺陷是_____________。改进实验后,仍符合上表中的实验现象,可得到的实验结论是_________(写一点)。
查看答案和解析>>
科目: 来源: 题型:
【题目】老师要求用规定的BaCl2溶液与适量的Na2SO4溶液制备BaSO4。完成操作Ⅰ后,小红发现自己错把Na2CO3溶液当成Na2SO4溶液,而此时BaCl2溶液已完全消耗。老师启发他,可用生成物和其他试剂完成制备BaSO4的实验。整个实验流程如图所示:

(1)试剂M是__________,气体C是__________。
(2)操作Ⅱ的名称是_________。
(3)反应①的化学方程式为________,溶液a中溶质是_______。
(4)反应③的基本反应类型为___________。
(5)从理论上讲,该实验过程最终得到的BaSO4质量与原方案得到的BaSO4质量是否相等?_________(填“是”或“否”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、盐酸、氢氧化钙溶液、硫酸铜溶液五名“队员”组成,比赛中,由硫酸铜溶液“队员”发球,“队员”间传接球,最后由丁位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示,图中连线物质间能发生反应。回答下列问题:
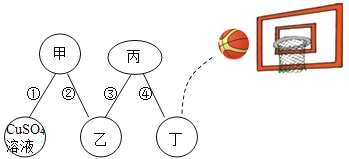
(1)已知丁位置上投篮的“队员”是个灭火“能手”,则丙位置的“队员”代表的物质是_________(填化学式)。
(2)乙位置的“队员”所代表的物质的一种用途是_____________。
(3)反应①的现象是____________。
(4)连线③代表的物质间发生反应的化学方程式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】多角度认识“二氧化碳与氢氧化钠溶液”反应。
(1)从反应物角度。
如图所示,甲同学往广口瓶内注入氢氧化钠溶液,U型管右边液面_______(填“升高”或“降低”),他认为二氧化碳和氢氧化钠发生了反应。乙同学认为还需将滴管内液体换成___________(写物质名称)进行对比实验,才能说明二者发生反应。

(2)从生成物角度。
①丙同学认为可用酚酞溶液验证二者发生了,该方法__________(填“可行”或“不可行”),原因是______________。
②丁同学建议,往反应后的溶液中滴加稀盐酸,观察到_____________现象,反应的化学方程式为_____________,说明二者发生反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用催化剂可消除室内装修材料释放的甲醛,其反应微观示意图如下:
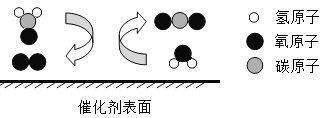
(1)图中的物质中,属于氧化物的是__________(填化学式)。
(2)该反应的化学方程式为____________。
(3)该反应过程中两种生成物的质量比为__________。
(4)对于该反应的下列说法正确的是__________(填序号)。
A能够实现无机物转化为有机物
B该反应没有遵循质量守恒定律
C催化剂增加生成物的质量
D反应中的四种物质均是由分子构成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com