
科目: 来源: 题型:
【题目】将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下。下列说法不正确的是
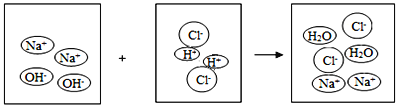
A. 反应前后阴、阳离子的总数目不变
B. 反应前后溶液的总质量不变
C. 反应后溶液呈中性
D. 反应前后元素种类不变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列属于复分解反应的是( )
A.2H2O 2H2↑+O2↑B.CO+CuO
2H2↑+O2↑B.CO+CuO![]() Cu+CO2
Cu+CO2
C.NaOH+HCl=NaCl+H2OD.Fe+CuSO4=Cu+FeSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:

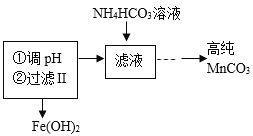
已知:①SO2与MnO2反应生成硫酸锰MnSO4;
②SO2与Fe2O3 在一定条件下生成FeSO4和H2SO4。
(1)“过滤”用到的玻璃仪器有烧杯、玻璃棒和__________。
(2)向过滤Ⅱ所得的滤液中加入NH4HCO3 溶液时温度控制在30-35℃,温度不宜太高的原因是____________。
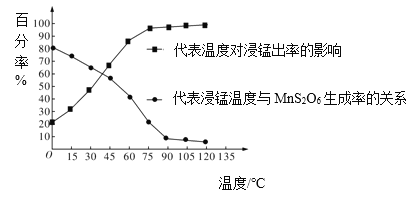
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少 MnS2O6 的生成,“浸锰”的适宜温度是__________。
(4)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_______。
(5)软锰矿中锰的浸出有两种工艺。
工艺A:软锰矿浆与含SO2的工业废气反应;
工艺B:软锰矿与煤炭粉混合,焙烧后加稀硫酸溶解。其中,工艺A的优点是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】乳酸亚铁(C6H10FeO6)是一种很好的食品铁强化剂,吸收效果比无机铁好,可由乳酸与FeCO3反应制得。乳酸亚铁溶于水形成带绿色的透明溶液,几乎不溶于乙醇。
(查阅资料)(1)Fe2+容易被氧气氧化成Fe3+。
(2)碳酸亚铁在空气中灼烧会生成一种铁的氧化物和CO2气体。
I.制备碳酸亚铁(装置如下图所示)
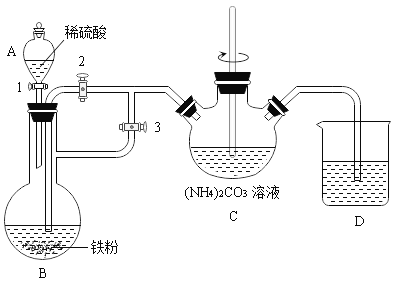
(1)B装置中反应的现象为_________(至少写两条)。C中玻璃棒的作用是_______。
(2)为了成功制得碳酸亚铁,实验开始时打开止水夹1、3关闭止水夹2。待B中反应即将结束时再打开止水夹2关闭止水夹3,目的是__________。反应结束后,将制得的碳酸亚铁浊液过滤、洗涤。
II.探究碳酸亚铁性质
(3)利用如图,称取11.6g纯净的碳酸亚铁固体放入硬质玻璃管中,打开K,通入氧气,加热硬质玻璃管,B瓶中澄清石灰水不再产生沉淀停止加热,继续通入氧气至玻璃管冷却,称得剩余固体质量净减3.6g。通过计算确定剩余固体的成分________(写出计算过程)。
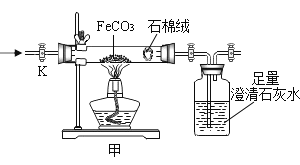
(4)写出A中反应的化学方程式__________。
III.制备乳酸亚铁
将制得的FeCO3加入到足量乳酸溶液中,再加入一定量铁粉(防止Fe2+被氧化),75℃以下搅拌反应。
(5)反应结束后,无需过滤,除去过量铁粉所需的试剂是__________(填字母)。
A 盐酸 B 硫酸铜 C 乳酸 D 氯化亚铁
(6)从乳酸亚铁溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气蒸发浓缩、________、过滤、洗涤、干燥。
(7)已知人体不能很好地吸收利用Fe3+,科学家研究表明服用含乳酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收,维生素C在这一过程中的作用是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下图所示实验装置,请根据实验装置(部分固定装置已省略) 回答问题:
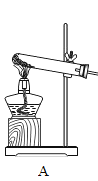
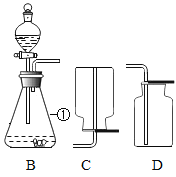
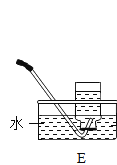
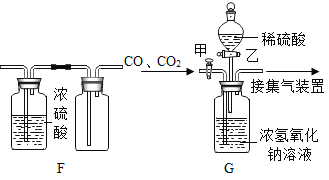
(1)图中标识①仪器的名称是:__________;
(2)实验室用 A 装置制取氧气的化学方程式为:______,实验室制取二氧化碳选择的装置组合是_____(从A~E中选),证明集气瓶已充满CO2的方法是_______。
(3)若用 F 装置收集一瓶干燥的某气体,则该气体可能是__________(填字母代号)
A NH3 B H2 C O2 D CH4
(4)工业上常需分离 CO、CO2 的混合气体,某同学采用装置 G 也能达到分离该混合气体的目的,操作步骤如下:
① 关闭活塞乙,打开活塞甲,通入混合气体,可从导管乙处收集到_______气体;写出G中发生反应的化学方程式____________。
②然后,关闭活塞甲,打开活塞乙,又可收集到另一种气体。
(5)电导率传感器可辅助探究水溶液中复分解反应的实质。相同条件下,溶液中离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的Ba(OH)2溶液平均分成两份置于两个烧杯中并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,测得溶液的电导率变化如图所示。
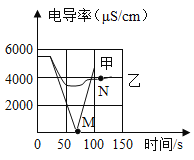
① 写出甲曲线对应的化学反应方程式__________。
② 分析曲线乙,下列说法错误的是__________(填字母)
A 开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B 整个实验过程中,溶液中Na+数目一直增大
C 电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
③ N点时,溶液中含有的离子是__________(填离子符号)
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年12月17日中国首艘国产航母“山东舰”交付中国海军入列,开拓中国新蓝海。
(1)航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是__________(填“分子”“原子”或“离子”)。
(2)航母舰体材料为合金钢,国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是__________(填“金属”或“合成”)材料。
(3)硝酸铵可用于制造导弹炸药,农业上还可用作__________。
(4)由生铁炼钢时,硅(Si)与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为_______,该反应的基本类型为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学就在我们身边,它与我们的生活息息相关。
(1)“健康饮食、均衡营养”是青少年健康成长的重要保证。下列物质中富含蛋白质的有________(填字母)。
A 米饭和馒头 B 大豆油和花生油 C 牛肉和鸡蛋 D 蔬菜和水果
(2)“食品安全”是一个永恒的话题。你认为下列认识科学的是________(填字母)。
A 任何食品都不可以使用食品添加剂
B 霉变的大米、花生,即使经过蒸煮也不能食用
C 含钙、锌的奶粉有利于补充人体所需的常量元素
D 用工业用盐亚硝酸钠代替食盐来腌渍食品
(3)生活中可用__________鉴别硬水和软水。
(4)加入洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的________作用。
(5)尿素是一种常用的化肥,工业上生产尿素反应的微观示意图如图:
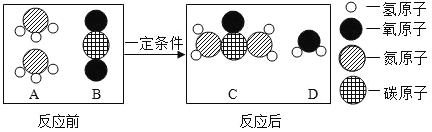
该反应中两种反应物A和B的质量比为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G都是初中化学常见的物质,它们的部分反应及转化关系如图所示。其中A为目前世界年产量最高的金属,A、B、C、D物质类别不同,其中C和D中不含相同的元素,E、F的组成元素相同。图中“→”表示转化关系,“﹣”表示相互反应关系(部分物质和反应条件未标出)下列说法正确的是
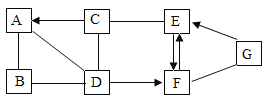
A.F→E是吸热反应
B.C和E 的反应属于置换反应
C.D一定是稀硫酸
D.C→A 反应的现象是红色固体变成银白色
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线。下列叙述错误的是
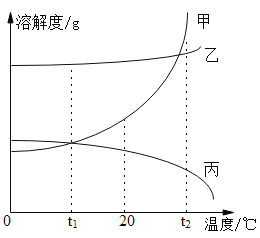
A.t1℃时,甲、丙的溶解度相等
B.20℃时,甲物质饱和溶液中溶质、溶剂的质量比为2:5
C.将t1 ℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是:乙>甲>丙
D.将t2 ℃时三种物质的饱和溶液降温到t1℃,乙溶液中析出的固体质量最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com