
科目: 来源: 题型:
【题目】某校研究性学习小组进行了一个有趣的实验探究:
[提出问题]实验室有一瓶久置的NaOH,变质程度怎样?
[设计方案]先称取21.2g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数。
[进行实验]实验测得加入稀硫酸的质量与产生CO2气体的质量关系如下图所示。
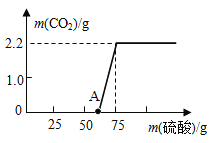
[数据处理]写出以下计算过程:
(1)该样品中Na2CO3的质量为多少?
(2)该样品中NaOH的质量分数为多少?
(3)NaOH变质的原因(用化学方程式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验结束时。同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里。如果将废液直接排放就会造成水污染。于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
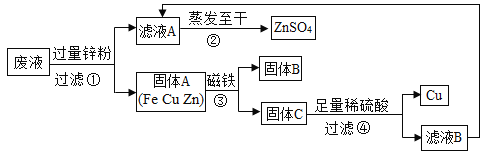
(1)滤液A和滤液B含有相同的溶质,其名称是_____;固体B的化学式为______.
(2)写出步骤①其中一个反应的化学方程式______。步骤④发生反应的化学方程式_______。
(3)要检验步骤④中加入的稀硫酸是否足量的方法是________。
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和____的质量
查看答案和解析>>
科目: 来源: 题型:
【题目】将相同体积、相同溶质质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种化合价相同的活泼金属中,生成H2的质量与反应时间的关系如图所示。下列说法中正确的是(___)
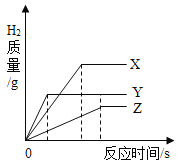
A三种金属的活动性顺序为Y>X>Z
B产生氢气的速率顺序为X>Y>Z
C相对原子质量由大到小的顺序为X>Y>Z
D_______
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是初中化学中常见物质间的转化关系,其中只有甲为单质,其他都是化合物; A是植物进行光合作用的一种重要原料,C可用于中和酸性土壤,反应②属于中和反应,其余反应条件、部分反应物和生成物已略去,试推断:
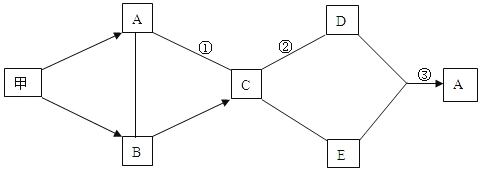
(1)B物质的化学式_______;E物质的类别是_________。
(2)写出下列化学方程式:甲→B:_________。反应③:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学甲设计了如图1所示的实验验证质量守恒定律.
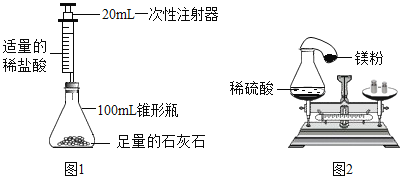
(1)按图1装配好仪器,检查装置的气密性的方法是_______;
(2)拔掉橡皮塞(注射器不要拔掉),装入足量石灰石,再用注射器吸入2mL的稀盐酸,注意盐酸不能多吸,原因是__________;
(3)再按图连接好装置,塞紧橡皮塞;
(4)将装置放在天平左盘,并用砝码游码使天平平衡;
(5)快速下推注射器活塞,使反应发生,此时锥形瓶内现象为_______、瓶外的现象为_______;
(6)反应结束后,再进行第2次称量,发现称量值没有发生变化;
(7)同学乙设计了如图2所示的装置来验证质量守恒定律,先把锥形瓶倾斜,再把气球中的铁粉倒入瓶中.试判断反应后,他的装置再次放在天平上_______(填“能”或“不能”)保持平衡.为什么________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是实验室常用的部分仪器。
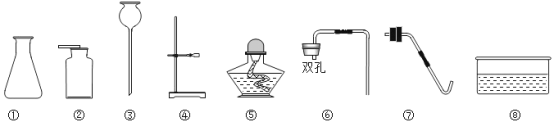
(1)仪器③的名称是________;
(2)用双氧水和二氧化锰混合物制氧气时,选用的发生装置是______(填仪器的序号,下同)
(3)同学们用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊。小英认为澄清石灰水已经变质:小青认为得到的CO2中混有_____(填名称)气体。他们为了证明自己的猜想进行了如下实验:
①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊;
②小青取______与块状石灰石反应制取的CO2,并将产生的气体通入原澄清石灰水中,变浑浊,请写出石灰水变浑浊的化学方程式_________。
(4)乙炔是一种无色、无味、难溶水的气体。密度和空气接近,收集乙炔气体可选用的装置是_______。
查看答案和解析>>
科目: 来源: 题型:
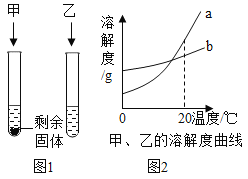
【题目】20°C时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图1所示的现象。20°C时,________(填“甲”或“乙”)的溶液不一定是饱和溶液。
图2中表示乙物质的溶解度曲线的是________(填“a”或“b”),要使试管中剩余的甲固体继续溶解可采用的方法是_______。把10°C a的饱和溶液升温到20°C,其溶质质量分数将_____ (填“变大”、 “变小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图象不能正确反映实验事实的是()
A.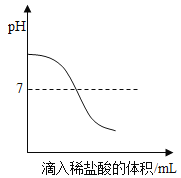 向氢氧化钠溶液中滴加过量的稀盐酸
向氢氧化钠溶液中滴加过量的稀盐酸
B.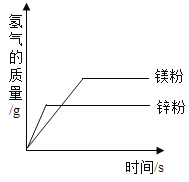 等质量的锌粉、镁粉与等质量相同溶质质量分数的稀盐酸(足量)反应
等质量的锌粉、镁粉与等质量相同溶质质量分数的稀盐酸(足量)反应
C.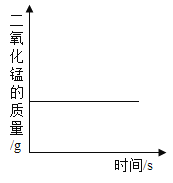 加热氯酸钾和二氧化锰的混合物
加热氯酸钾和二氧化锰的混合物
D.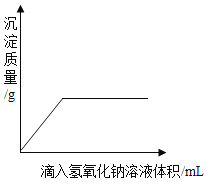 向一定量的硫酸铜溶液中滴加氢氧化钠溶液
向一定量的硫酸铜溶液中滴加氢氧化钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:___________________________,发生的反应方程式是:__________________________.
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为______________________________;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
实验步骤 | 实验现象 | 实验结论 |
取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后,___________观察现象 | 溶液依然为红色 | ____________________ |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.
猜想3:_____________
方案3:
实验步骤 | 实验现象 | 实验结论 |
_________________ | _______________ | ______________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】铝土矿的主要成分是氧化铝(所含杂质不参与反应,也难溶于水),工业上用铝土矿制取金属铝的过程如下图所示,请你回答以下问题:
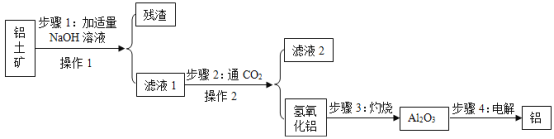
(1)步骤1中发生如下反应:Al2O3+2NaOH═2NaAlO2+X,X的化学式是__.
(2)操作1和操作2中均用到玻璃棒,其作用是__,滤液2的PH为10显__性(填“酸或碱”).
(3)步骤2得到的氢氧化铝可以用于治疗胃酸过多,该反应属于__反应(填“化合、分解、复分解”).
(4)步骤3中发生了分解反应,除了生成氧化铝,还有一种氧化物生成.请写出该反应的化学方程式__.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com