
科目: 来源: 题型:
【题目】小强和小明两位同学对黄色的FeCl3溶液产生了浓厚的兴趣,查阅资料获得如下信息:
①FeC13能与Cu、Fe、Al等金属反应生成FcCl2,如:2FeCl3+Cu=2FeCl2+CuCl2;
②FeCl3溶液能使无色的苯酚溶液变成紫色。
(提出问题)①FeCl3溶液与金属铝反应有哪些现象?②FeCl3溶液中的哪种微粒使苯酚溶液变成紫色?
(实验探究)取适量FeCl3溶液于试管中,进行如下实验
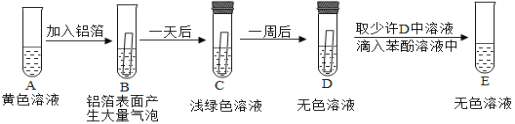
(思考与交流)
①实验前,铝箔表面需要进行打磨处理,其目的是____________。
②根据试管_________(填“A”、“B”、“C”、“D”、“E”、)中现象,可以推断FeCl3溶液的pH_______7(填“>”“<”或“=”)
③溶液由黄色变成浅绿色的化学反应方程式为_____________。
④D中无色溶液的溶质主要是____________________________(填化学式)
⑤经分析,小强同学认为是Fe3+使苯酚溶液变成紫色,但小明同学认为若要得出此结论还需补做如下实验:在苯酚溶液中滴加稀盐酸,观察溶液是否变成紫色。小明的理由是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】CaCO3在生产生活中有广泛的用途。
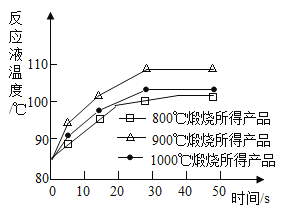
(1)烧石灰石可制得活性CaO,反应的化学方程式为_________________________。为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图所示。由此可知:CaO与水反应会__________热量(填“放出”或“吸收”),上述温度中,_________℃煅烧所得CaO活性最高。
(2)以电石渣[主要成分为Ca(OH)2还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
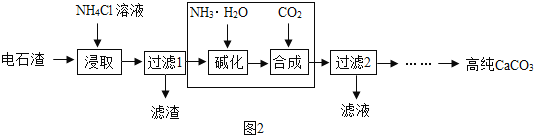

①上图为NH4Cl浓度对钙、镁浸出率的影响(![]() ),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
②流程中框线内若改用溶液_________________(填化学式),可一步得到与原流程完全相同的生成物。
③流程中框线内若改用Na2CO3溶液,也能得到高纯CaCO3。试从生成物的角度分析原流程的优点:a.NH3可循环利用;b._______;
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组利用实验室制CO2的废液得到CaCO3和NaCl晶体,过程如下:
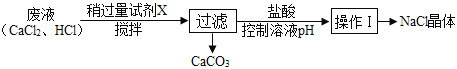
(1)试剂X可用___________(填序号)。
a NaOH溶液 b Na2CO3 溶液 c K2CO3 溶液
(2)过滤时使用的过滤器由___________和_________组成,过滤后滤液中的溶质有_________种。
(3)使用pH试纸测定溶液酸碱度的操作是_______________________________,当溶液pH的范围在___________时,可以进行操作Ⅰ。
(4)操作Ⅰ的名称为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某新型能源转换与利用模式示意图:
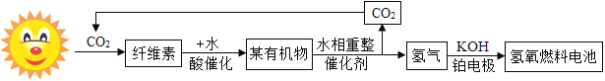
(1)该模式中涉及的能源转化依次为:太阳能→生物质能→_____能→电能,其中太阳能转化成生物质能用化学方程式可以表示为_____
(2)某有机物水相重整制取氢气的反应可表示为:CxHyOz+3H2O 2CO2+6 H2,则x:z=_____;
2CO2+6 H2,则x:z=_____;
(3)该系统中循环使用的物质是___________和H2O ;
(4)与电解水相比,该模式制取氢气的主要优点是:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某白色固体由BaCl2,NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组为确定其成分,进行了如下实验探究。
Ⅰ.初步探究:小金同学设计的实验过程及现象如下图所示
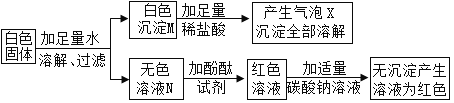
(查阅资料)BaCl2溶液显中性,BaSO4沉淀不溶于稀硝酸等酸。
(初步分析)(1)白色沉淀M的化学式是________________,产生气体X的化学方程式是_______________
(2)溶液N中的溶质一定有_____________________,一定没有氯化钡。
(3)原白色固体中一定有的物质是____________,一定没有的物质是_________________。
(交流讨论)小英同学认为:无色溶液N滴加酚酞试液后变红,说明溶液N中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠,若要进一步确定,需对溶液N继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液N中有氢氧化钠吗?
(猜想与假设)猜想1:有NaOH;猜想2:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
取无色溶液N加入过量BaCl2溶液,振荡后静置 | ______ | 证明溶液N中有碳酸钠并已被除尽 |
取上述步骤所得上层清液于试管中,加入________ | _______ | 猜想1正确 |
查看答案和解析>>
科目: 来源: 题型:
【题目】酒精(C2H6O)、硫酸铜、甲醛(CH2O)、过氧乙酸(C2H4O3)、次氯酸钠( NaClO)都是生产和生活中常用的消毒剂。
(1)上文所述杀菌消毒剂中属于有机物的有________种。
(2)次氯酸钠( NaClO中氯元素的化合价是___________。
(3)生活中常用酒精(C2H6O)杀菌消毒,其原理是________________
(4)过氧乙酸分子中含有一种叫“过氧基”的结构(—O—O—),据此推测下列物质也可作杀菌消毒剂的是________。
A H-O-H B O=C=O C 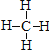 D H-O-O-H
D H-O-O-H
(5)工业上用低品位的氧化铜矿加稀硫酸浸渍,然后进行浓缩,可以制取硫酸铜。写出上述过程中生成硫酸铜的化学方程式___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】奶油的主要成分为脂肪和蛋白质,还富含维生素A(C20H30O),呈弱酸性。
(1)奶油是一种高热量食品,原因是成分中富含_______________和蛋白质。
(2)蛋白质中一定含有氢、氧、________和____________元素。
(3)维生素A中碳元素:氢元素质量比________。
(4)奶油的pH约为_________(填序号)
a 0.2 b 6.6 c 7.3 d 14.0
查看答案和解析>>
科目: 来源: 题型:
【题目】测定氢氧化钠溶液与盐酸反应时的pH,得到如图所示曲线,下列有关判断不正确的是
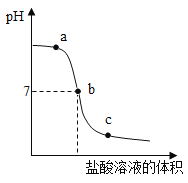
A.实验过程是在氢氧化钠溶液中不断滴加盐酸
B.a点溶液的物质有氢氧化钠,氯化钠和盐酸
C.b点溶液的温度高于a点
D.c点与b点溶液中氯化钠的质量相等
查看答案和解析>>
科目: 来源: 题型:
【题目】甲乙两组同学为探究氢氧化钙的化学性质,分别做了如下相同的四个实验:
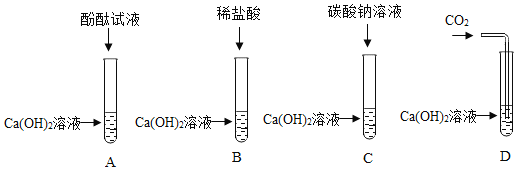
请回答下列问题:
①上述实验中,能发生反应但无明显现象的化学方程式_____。
②实验结束后,甲、乙两组同学分别将本组A、B、C、D四支试管中的物质各倒入一个洁净的大烧杯中,充分反应后静置,发现;
甲组烧杯底部有白色沉淀,上层清液为红色,则下列说法错误的是_____。
A 沉淀是碳酸钙
B 清液中一定含有氢氧化钠
C 清液中一定没有氯化氢
乙组烧杯底部有白色沉淀,上层清液为无色。则上层清液中一定含有的溶质是_____,可能含有的溶质是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是几种实验室制取气体的发生装置和收集装置。请回答下列问题:
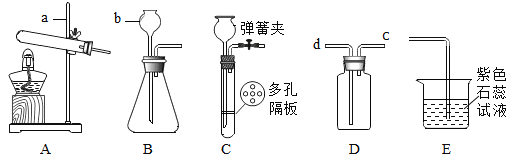
①请写出标有序号的仪器的名称:a_____;b_____。
②小华同学用浓盐酸与大理石在C装置中反应,制取CO2后通入到盛有紫色石蕊试液的烧杯E中,观察到紫色石蕊试液变红,对这一现象的解释合理的是_____。
a、产生的CO2直接使石蕊变红
b、挥发出的氯化氢气体溶于水,使石蕊试液变红
c、产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
③采用装置A加热氯酸钾和二氧化锰的混合物制取氧气,若用D装置采用排空气法收集氧气,氧气应从_____(选填“c”或“d”)进。
④实验室加热氯酸钾和二氧化锰的混合物28.0g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
I、生成氧气的质量为_____g。
II、求原混合物中氯酸钾的物质的量_____。(根据化学方程式列式计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com