
科目: 来源: 题型:
【题目】结合配制245g质量分数为20%的稀 H2SO4溶液的实验,回答下列问题。
(1)计算:需要质量分数为 98%的浓H2SO4溶液_______g;
(2)量取:量取所需的水时俯视读数,其他操作均正确,则配制出的稀溶液的质量分数_______20%(选填“大于”、“等于”或“小于”);
(3)混匀:将准确量取的水和浓 H2SO4 依次倒入_______(填写一种仪器名称)中,用玻璃棒搅拌,使产生的热量随时散发掉并使溶液混合均匀;
(4)装入试剂瓶中,贴好标签,密封保存。
查看答案和解析>>
科目: 来源: 题型:
【题目】烧碱、熟石灰是两种重要的碱,回答与它们有关的下列问题。
(1)用于改良酸性土壤是熟石灰、烧碱中的_______;
(2)实验室常用石灰水来检验二氧化碳气体,其发生反应的化学方程式是_______;
(3)烧碱溶液、石灰水都能使无色酚酞溶液变红、与酸反应生成盐和水、与某些盐反应生成新盐和新碱,从微观角度看它们具有这些相似化学性质的原因是_______;
查看答案和解析>>
科目: 来源: 题型:
【题目】回答下列与含碳物质有关的问题。
(1)制糖工业中利用活性炭的_______性脱色制白糖;
(2)CO2与H2O反应,生成一种能使石蕊溶液变红的物质,这种物质是_______;
(3)在高炉炼铁的核心反应Fe2O3+3CO![]() 2Fe+3CO2里,其中_______发生氧化反应。
2Fe+3CO2里,其中_______发生氧化反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】分析图中KNO3、NaCl两种固体的溶解度曲线,回答下列问题。

(1)在35℃时NaCl的溶解度_______(选填“大于”“等于”“小于”)KNO3的溶解度。
(2)20℃时将25gKNO3放入100g水中充分搅拌,得到该溶液的质量为______g。
(3)10℃时将10gNaCl和30gKNO3加入到100g的水中,充分搅拌。发现有固体剩余,则剩余的固体是_______(不考虑两物质对溶解性的影响);
(4)硝酸钾溶液中混有的少量氯化钠,提纯硝酸钾可采取_______(选填“降温结晶” 或“蒸发结晶”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学用语回答下列问题。
(1)氧化镁中镁元素的化合价_______;
(2)3个铝离子_______;
(3)化学反应 4HNO3![]() 2H2O+4NO2↑+X↑中X的化学式是_______。
2H2O+4NO2↑+X↑中X的化学式是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】西汉东方朔所撰的《申异经》中有“西北有宫,黄铜为墙,题曰地皇之宫”的记载。黄铜是铜锌合金。为测定某黄钢样品中铜的质量分数,某同学取黄铜样品与足量稀硫酸充分反应(如图所示),测得相关数据如表。

反应前 | 反应后 | ||
装置质量 | 黄铜样品质量 | 稀硫酸质量 | 装置及装置内物质的总质量 |
260.0g | 50.0g | 100.0g | 409.5g |
计算:
(1)实验过程中,产生氢气的质量为 g。
(2)该黄铜样品中铜的质量分数(计算结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用电解饱和食盐水的方法制备烧碱(NaOH)、氯气(Cl2)和氢气,并以它们为原料生产一系列化工产品,称为氯碱工业,某化学兴趣小组同学在实验室进行如下探究:
探究一:验证电解饱和食盐水的产物
(查阅资料)(1)氯气在通常情况下呈黄绿色、是一种有强烈刺激性气味的有毒气体;(2)氯气能与碱溶液发生反应,能使湿润的淀粉碘化钾试纸变蓝。
(实验验证)按图甲所示装置进行实验探究
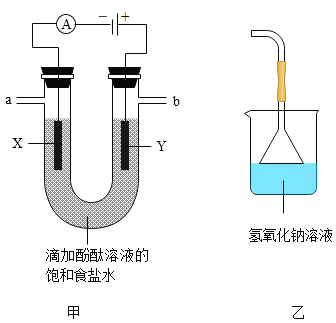
接通电源一段时间后,观察到X、Y电极周围均有气泡产生,溶液由无色变为红色。用小试管在a端收集气体,移近酒精灯火焰,松开拇指,发出轻微的爆鸣声。将湿润的淀粉碘化钾试纸放在b端,试纸变蓝。
(实验分析)
(1)a端收集到的气体是_____。
(2)电解饱和食盐水的化学方程式为_____。
(3)b端后连接乙装置,乙装置中氢氧化钠溶液的作用是_____。
(拓展延伸)上述电解饱和食盐水实验中,电解产物之间能发生化学反应。为避免产物混合发生反应,工业上常用离子交换膜法进行生产制备,将得到的溶液蒸发结晶获得烧碱。
探究二:工业上生产的烧碱中含有哪些杂质?
(猜想假设)
猜想一:NaCl
猜想二:Na2CO3
猜想三:NaCl和Na2CO3
工业上生产的烧碱中可能含有Na2CO3,作出此猜想的依据是_____。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液 | _____ | 猜想三正确 |
(反思评价)
(1)小乐同学认为上述实验中可用稀盐酸代替稀硝酸,小娟不同意,小娟的理由是_____,
(2)除去烧碱溶液中少量的碳酸钠,可选用的药品是_____ (填标号)。
A CuCl2溶液
B Ba(NO3)2溶液
C Ba(OH)2溶液
D KOH溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】五氧化二钒(V2O5)是一种重要的化工催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分有V2O5、V2O4、K2SO4、Fe2O3、Al2O3和SiO2等,其中SiO2既不溶于水也不溶于H2SO4.以下是一种回收V2O5的工艺路线:
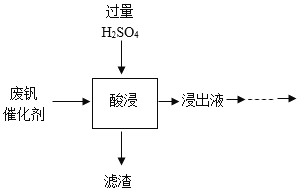
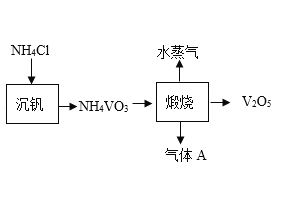
(1)“酸浸”时V2O5转化为(VO2)2SO4.写出V2O5和H2SO4发生反应的化学方程式_____。
(2)滤渣的主要成分为_____。
(3)“煅烧”中生成的H2O和V2O5的化学计量数之比为1:1.该反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普材料。
铁元素是人体必需的元素之一。人体缺铁会引起贫血,缺铁性贫血是世界卫生组织确认的四大营养缺乏症之一,人体中的铁元素主要靠食物摄入,猪肝、猪血、瘦肉、木耳、红枣、菠菜等是铁元素的主要食物来源,人类最早使用的铁,是来自太空的陨铁,自然界中的铁主要以化合物的形式存在于矿石中,工业炼铁的原理是用还原的方法把铁从铁矿石中提炼出来,常见的铁矿石有赤铁矿(主要成分是Fe2O3 )、磁铁矿(主要成分是Fe3O4)、黄铁矿(主要成分是FeS2)等。其中黄铁矿由于含量高,冶炼过程产生的SO2会对环境造成影响,不适宜炼铁,但可作为工业制硫酸的重要原料。铁的氧化物除Fe2O3、Fe3O4外还有FeO,FeO可用于瓷器制作,在隔绝空气的条件下加热草酸亚铁(FeC2O4)可制得FeO。
金属资源的储量有限,而且不能再生,保护金属资源迫在眉睫。铁制品在自然条件下容易锈蚀,在纯金属铁中熔合一定量的铬和镍制得的不锈钢具有很好的抗腐蚀性能,不仅延长了铁制品的使用时间,而且有效的保护了金属资源,随着科学技术的发展新材料层出不穷,目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等,
回答下列问题:
(1)铁是人体中必需的_____元素(填“常量”或“微量”)。
(2)用一氧化碳把铁从赤铁矿中还原出来的化学方程式为_____。
(3)黄铁矿不适宜炼铁的原因是_____。
(4)草酸亚铁固体在隔绝空气的条件下加热,生成FeO的同时还生成两种相对分子质量相差16的氧化物。该反应化学方程式为_____。
(5)保护金属资源的途径除了防止金属腐蚀之外还有_____(任写一条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com