
科目: 来源: 题型:
【题目】材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
(一)实验室用赤铁矿模拟工业炼铁的化学方程式为_____,炼得的铁是_____(填“单质铁”或“合金”),该反应_____(填“是”或“不是”)置换反应。
(二)FeCO3是菱铁矿的主要成分,具有还原性,在空气中灼烧生成铁的氧化物和CO2气体。要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与小华同学的探究:
(查阅资料)
① FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水。
②FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色。
(猜想与假设)
猜想1:固体成分是氧化铁;
猜想2:固体成分是四氧化三铁;
猜想3:_____。
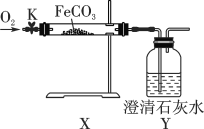
(活动与探究)连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X。当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验。
实验编号 | 实验步骤 | 实验现象 |
a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
b | 向乙溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(结论与反思)
(1)由上述实验现象可知,FeCO3在氧气中高温灼烧得到的固体产物是_____,因此,猜想_____(填“1”“2”或“3”)是正确的。
(2)FeCO3在氧气中高温灼烧的化学方程式为_____。
(3)上述实验_____(填“a”或“b”)是多余的,因为_____。
(总结与提升)
(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙。碳酸氢钙的化学式为_____。
(2)CO2使澄清石灰水变浑浊的化学方程式为_____。
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到_____,就不能确定哪个猜想是正确的。所以小华同学又对该实验进行了定量探究:取11.6 g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6 g。通过计算即可确定:FeCO3和氧气充分反应后的固体成分是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】作为推行“低碳经济”的重要科技进步成果。太阳能光伏发电成为上海世博会的“亮点”。太阳能光伏发电最关键的材料是高纯硅,生产高纯硅的流程示意图如下: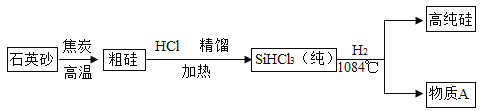
(1)地壳中含有大量的硅元素,它的含量仅次于_____元素(填元素符号)。
(2)粗硅生成SiHCl3的同时,还产生一种气体单质,写出反应的化学方程式_____。
(3)“精馏”也是蒸馏的一种形式。通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的_____(填“熔点”或“沸点”)不同。
(4)整个制备过程必须达到无水无氧。在H2还原SiHCl3过程中若混入O2,可能引起的后果是①发生爆炸,②_____。
(5)为了达到资源综合利用的目的,上述生产流程中某些物质可循环使用,这些物质是_____(填化学式)。
(6)石英砂含有少量杂质Al2O3。已知其主要成分SiO2不溶于水且不溶于酸,若要除去其中的杂质Al2O3,可选用的试剂是_____(填化学式)。
(7)实验室盛放氢氧化钠的试剂瓶不能用玻璃塞,是因为大多数玻璃中含较多的二氧化硅。和二氧化碳与氢氧化钠的反应类似,请写出二氧化硅与氢氧化钠溶液的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下列实验装置,回答问题
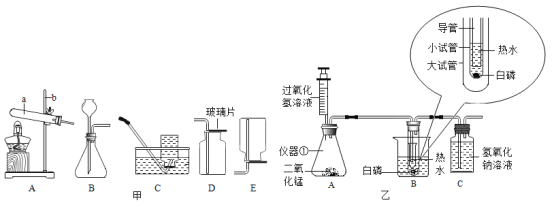
(一)(l)写出仪器a和b的名称:a_____,b_____。
(2)加热氯酸钾和二氧化锰的混合物制取氧气,该反应的化学方程式为_____。
(3)用石灰石和稀盐酸制取并收集纯净的二氧化碳,选用的装置为_____(填字母)。
(二)图乙是某实验小组探究白磷在水中燃烧的改进实验装置,由F、G、H三部分组成。请认真阅读下列内容并回答有关问题。
资料卡:凡能与碱反应生成盐和水的氧化物,称为酸性氧化物。常见的酸性氧化物有CO2、SO2、SiO2、P2O5等。
(1)在仪器①中加入1药匙二氧化锰,用注射器吸入约40 mL 5%的过氧化氢溶液,然后将注射器的针头刺入橡皮塞中。实验室中的_____(填仪器名称)和该实验中注射器有相同的作用。
(2)在广口瓶H中加入氢氧化钠溶液至其中上部,旋紧双孔塞。加入氢氧化钠溶液的目的是_____。
(3)取一块绿豆大小的白磷放入小试管中,再加入少量约80 ℃的热水(热水的高度以小试管高度1/2为宜);将大试管稍作倾斜,让小试管沿大试管内壁滑入大试管中;将双孔塞的长导管伸到小试管中接近白磷正上方的位置,旋紧双孔塞;最后将大试管放入烧杯中。放白磷的试管应选择尽可能小的较为适宜,其原因是_____。
(4)按图乙连接好装置。在烧杯中加入200 mL约80 ℃热水,烧杯中热水的作用是_____。
(5) 缓慢推动注射器。仪器①中发生反应的化学方程式为_____。装置G小试管中观察到的现象为:① 有气泡产生,②_____;G中反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】水是人类赖以生存的物质之一,也是实验室最常用的物质之一。
(1)下列含“水”的物质属于纯净物的是_____(填字母序号)。
A 自来水 B 冰水混合物 C 河水 D 蒸馏水
(2)明矾是常用的净水剂之一,其作用是_____;用明矾净化后的水是_____(填“软水”或“硬水”);高铁酸钾(K2FeO4)也可用来净化水, K2FeO4中铁元素的化合价为_____。制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,则X的化学式为_____。
(3)为了防止水的污染,下列做法有利于保护水资源的是_____ (填编号)。
①抑制水中所有动、植物的生长 ②不任意排放工业废水 ③大量使用化肥农药 ④生活污水经过净化处理后再排放
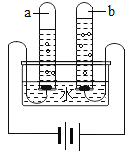
(4)如图是简易的电解水实验示意图。其中b管产生的气体为_____,反应的化学方程式为_____;晓明同学用自制电解器电解水,在水中加少许硫酸钠,目的是_____;当他在103.6g质量分数为5%的硫酸钠溶液中通电一段时间后,产生3.2 g氧气,此时另一极产生的氢气质量为_____;配制5%的硫酸钠溶液用到的玻璃仪器有烧杯、玻璃棒、_____,此时,硫酸钠的质量分数为_____(精确到0.01%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】酸奶是日常生活中常见的一种食品,下表是某酸奶外包装上标识的营养成分表。

项 目 | 能 量 | 蛋白质 | 脂 肪 | 糖 类 | 钠 |
每100 g | 329 kJ | 2.6 g | 3.1 g | 10.0 g | 60 mg |
请填写下列空格:
(1)表中“钠”是指_____(填序号)。
A 离子 B 分子 C 元素 D 单质
(2)酸奶中的_____在消化道内会逐渐被分解成可被人体吸收的多种氨基酸,氨基酸在元素组成上与糖类物质_____(是/否)相同。
(3)脂肪在人体内分解、氧化释放出能量的过程,是将_____能转化为热能。
(4)酸奶经过发酵,营养成分更易被人体吸收,但胃酸过多的病人不宜服用酸奶。某饼干中含有碳酸氢钠(俗称_____),小苏打可以用于治疗胃酸过多,反应的化学方程式为_____。
(5)该酸奶标识中还缺少的两种营养素是水和_____。
(6)无菌砖(枕)是一种常见的酸奶包装,其材料主要为PE/纸板/铝箔/PE。其中铝箔可以避光和阻断透气,减少营养损失。铝可以压成铝箔,是利用铝的_____(一种物理性质)。PE指的是聚乙烯,它属于_____(填“合成材料”或“复合材料”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有H、C、O、S、N、Cu、Ca七种元素,请从中选择适当的元素组成符合要求的物质,并按要求填空。
(1)A为碳不充分燃烧的生成物,写出A物质的化学式:_____。
(2)B为最简单的有机物,写出B物质在空气中燃烧的化学方程式:_____。
(3)C为实验室常用燃料,写出C物质的化学式:_____,C物质还可以通过淀粉类粮食发酵制得,淀粉的化学式_____。
(4)D为澄清石灰水的溶质,标出D物质中显正价元素的化合价:_____。
(5)E的水溶液为蓝色,且工业上常用E和D配制波尔多液,写出配制波尔多液的化学反应方程式_____;E中阴离子的离子符号为_____。
(6)F为一种常见的化肥,若与D混用,会产生_____(填化学式)降低肥效。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是
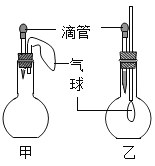
甲 | 乙 | |
A | 稀硫酸和铜片 | 水和 CO2 |
B | 双氧水和MnO2 | NaOH溶液和CO2 |
C | Na2CO3溶液和稀硫酸 | NaOH溶液和SO2 |
D | H2O和NH3 | 硝酸银溶液和HCl |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是
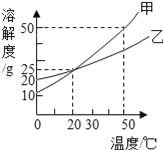
A.20℃时,100g甲溶液中含甲物质的质量为25g
B.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
C.将100g甲溶液从50℃降温到30℃时一定有晶体析出
D.将甲、乙两种物质饱和的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为20%
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生为了探究甲烷的组成元素,设计并完成了如下探究实验,请你帮他完成下面的实验报告:
提出问题:甲烷中含有哪些元素?
(查阅资料)含碳元素的物质完全燃烧生成![]() 。
。
实验探究:
实验步骤 | 实验现象 | 解释与结论 |
①在空气中点燃甲烷, ②将洁净干燥的小烧杯罩在甲烷燃烧的火焰上方。 | 烧杯内壁有水珠。 | 证明生成物有水,甲烷中一定含有_______元素。 |
③将蘸有澄清石灰水的小烧杯罩在甲烷燃烧的火焰上方。 | _____________。 | 证明生成物有 |
(1)表达与交流:经实验测定甲烷的化学式为![]() ,请你写出甲烷燃烧方程式:________________。
,请你写出甲烷燃烧方程式:________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制取气体的常用装置,请结合装置回答下列问题。
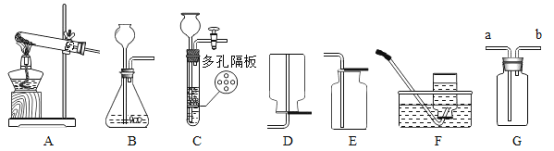
(1)实验室可以选择B装置用双氧水制取氧气,也可选择A装置用加热氯酸钾制取氧气,若两实验中都用到了同一种黑色固体药品,它在这两个反应中起________作用;请你写出用氯酸钾制取氧气的化学方程式:________________。
(2)如果要收集到较纯净的氧气应选择的收集装置是________;采用G装置收集氧气,如何确定氧气已满?________________,这说明氧气具有________性质。
(3)若实验室用C.F装置组合制取某种气体,应满足的条件是________。
A反应物是块状固体和液体,反应在常温下进行
B制得气体密度比空气大
C制得气体密度比空气小
D制得气体难(不易)溶于水
E制得气体易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com