
科目: 来源: 题型:
【题目】(1)如图是实验室制取和收集气体的一些常见的实验装置图,请根据图示回答下列问题:

①实验室制取并收集二氧化碳应选用的装置是_________;通常检验二氧化碳气体的化学方程式为___________________________。
②若用F装置收集二氧化碳气体,气体应该由_________(填 “a”或“b”)端导入, 检验D装置中二氧化碳已收集满的方法是___________________________。
③在实验室中,常用加热固体氯化铵和氢氧化钙混合物的方法制氨气,若用此法制取氨气,应选用的发生装置是________________。
(2)钙元素是一种重要的金属元素,它可组成氯化钙、氢氧化钙等多种物质。
①氢化钙(CaH2)固体是登山运动员常用的能源提供剂。某实验探究小组的同学通过查阅资料得知,氢化钙在常温下能与水反应生成氢氧化钙和氢气,请你写出该反应的化学方程式_____________。
②该实验探究小组将Na2CO3溶液滴到Ca(OH)2 :溶液中充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
[提出问题]滤液中溶质的成分是什么?
[猜想与假设]猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和__________
猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是_____________________。
[实验过程]
实验步骤 | 现象 | 结论 |
步骤I:取滤液,向其中滴入适量Na2CO3溶液 | __________ | 猜想二不成立 |
步骤II:另取滤液,向其中加入足量__________溶液 | 产生气泡 | 猜想__________成立 |
查看答案和解析>>
科目: 来源: 题型:
【题目】归纳总结是学习知识的重要方法。小军同学用图1总结了NaOH的四条化学性质。
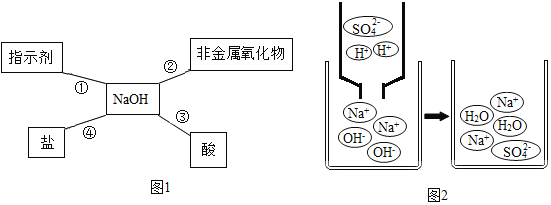
(1)图2利用微观示意图来说明反应③的发生,请写出该反应的化学方程式:______;从该图还可以看出,反应后的溶液pH______7 (填“>”“一”或“<”)。
(2)如果反应④能够发生,你选择的物质是______(填序号)。
A HCl B Na2CO3 C CuSO4
(3)另外,NaOH溶波还能与某些金属(如Al)发生反应,请配平该反应的化学方程式: NaOH+__H2O+__Al=__NaAlO2+__H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】有A,B两种金属放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )

A.金属活动性A>B B.生成氢气的质量A>B
C.反应的硫酸质量A<B D.反应的金属质量A<B
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )

A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数变小
D.70℃时,饱和石灰水中溶质和溶液的质量比为0.1:100
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组转化关系中的反应为初中化学常见的反应,其中的“→”表示某种物质可一步反应生成另一种物质。甲、乙、丙三种物质不符合对应“转化关系”的是( )
选项 | A. | B. | C. | D. | |
转化关系 |
|
|
|
| |
物 质 | 甲 | FeCl2 | HCl | CaCO3 | CuSO4 |
乙 | Fe | H2O | CO2 | Cu | |
丙 | Fe2O3 | H2 | Na2CO3 | CuO | |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示氮元素的化合价与物质类别的部分关系图。下列说法不正确的是( )
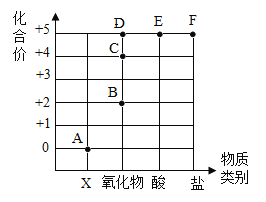
A.C 点表示物质的化学式为 NO
B.A 点对应的物质类别是单质
C.化学式为 NaNO3 的物质代表的点是 F
D.由 D 点表示的物质与水发生反应生成 E 的化学方程式为 N2O5+H2O=2HNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学用语与所表述的意义相符的是( )
①2 Mg+2-----2个镁离子
②O2----2个氧原子
③2H2O------2个水分子
④![]() ----氮气中氮元素的化合价为零
----氮气中氮元素的化合价为零
⑤氩气-----Ar2
A.③⑤B.③④C.①②D.①⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学方程式符合题意且书写正确的是( )
A.工业上用高温煅烧石灰石的方法制生石灰: CaCO3![]() CaO+CO2
CaO+CO2
B.医疗上用氢氧化镁中和过多胃酸: Mg(OH)2+HCl=MgCl2+H2O
C.正常雨水的pH小于7的原因: CO2+H2O=H2CO3
D.证明铁是金属活动性顺序表中氢之前的金属: 2Fe+6HCl=2FeCl3+3H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为: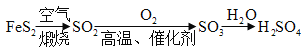
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是
A 立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液
B 立即用稀氢氧化钠溶液冲洗,然后再用水冲洗
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,反应为:H2SO4+ Ba(OH)2=BaSO4↓+2H2O,沉淀不再产生时(此时恰好完全反应),求反应中Ba(OH)2的质量。
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液。已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
![]()
小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是一定不是______。他取少量待测液于试管中,加入过量的稀HCl,看到_____________________,由此小张同学认为,溶液为Na2CO3溶液。
小李同学对小张同学的结论提出疑问,由进行了以下实验:取少量待测液于试管中,加入过量的CaCl2溶液,生成白色沉淀,该反应方程式为______________,静置,(写出还需进行的操作及现象)__________________。通过实验,小李认为小张结论正确。
二位同学给试剂瓶贴一新标签:Na2CO3。
实验结束后,同学们通过讨论认为试剂瓶原标签可能不是Na2CO3,你认为可能是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com