
科目: 来源: 题型:
【题目】在实验室,小明将稀盐酸倒入Ba(OH)2溶液中得到溶液甲,相关实验探究如下。
(提出问题)充分反应后所得甲溶液中的溶质是什么?
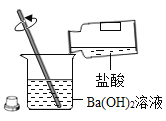
(合理猜想)(1)氯化钡
(2)氯化钡和盐酸
(3)_____________________。
(实验方案)(4)探究甲溶液中是否含有盐酸?
实验 | 操作 | 现象 | 结论 |
① | 取少量甲溶液于试管中, ______________________。 | 没有气泡产生 | 甲中不含盐酸 |
(5)探究甲溶液中是否含有氢氧化钡?
实验 | 操作 | 现象与化学方程式 | 结论 |
② | 取少量甲溶液于试管中,滴入适量的氯化铁溶液。 | _________ | 甲中含氢氧化钡 |
③用一种试剂一次性确定甲溶液中是否含有氢氧化钡还可用的试剂是___________________。 A纯碱 B盐酸 C氯化铜 D硫酸钠 | |||
(得出结论)(6)通过上面的实验(4)(5)推测,猜想合理的是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在常温下,氮气的化学性质很稳定,但在高温、高压条件下可与某些物质发生化学反应。以空气和其它必要的原料合成氮肥硝酸铵(NH4NO3)的工业流程如图所示。
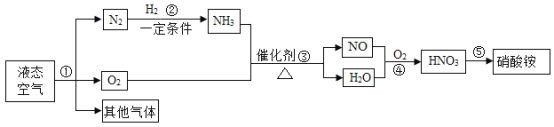
请回答下列问题:
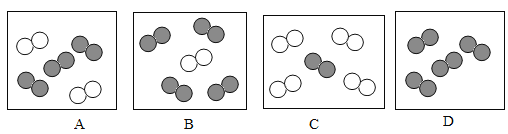
(1)若用“![]() ”表示氮原子,用“
”表示氮原子,用“![]() ”表示氧原子,且同温同压下,气体体积比等于分子数目比(忽略其它成分)。则下图中可用来表示空气微观模型的是
”表示氧原子,且同温同压下,气体体积比等于分子数目比(忽略其它成分)。则下图中可用来表示空气微观模型的是
(2)上述流程中①发生的是_________________(填“物理”或“化学”)变化。
(3)反应③中化学方程式为________,其中氮元素化合价变化情况为___________。
(4)结合下框说明可知硝酸铵物理性质为__________。
(5)适当地施用硝酸铵可使植物的叶色浓绿,但要避免与熟石灰混用的化学反应原理是___。

(6)该化肥的纯度为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】稀土,是一组典型的金属元素。其之所以异常珍贵,不仅是因为储量少,不可再生,分离提纯和加工难度较大,更因其广泛应用于农业、工业、军事等行业;稀土是新材料制造的重要依托和关系尖端国防技术开发的关键性资源,被称之为万能之土,也素有“工业维生素”之称。稀士元素铈在元素周期表中信息如图所示。
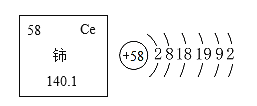
(1)铈(shi)的原子序数为_______________________。
(2)加入Ce2O3的玻璃属于________________材料;
(3)由于特殊的原子结构,铈的化学性质较为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】溶液普遍存在于生活中。通过科学探究中的控制变量法可以测得物质的溶解度。
(1)在探究固体物质溶解度时,需考虑的因素有a.溶质的种类;b.______________________;c.溶剂的温度;d.溶剂的质量;e.溶质被溶剂溶解的最大值。若要测定“某种固体物质在不同温度时的溶解度”,其研究所指的是_________________________受温度变化的影响,实验必须严格控制其它因素保持不变。
(2)下表格是根据控制变量法测得:在不同温度时,两种固体物质在水中的溶解度。
温度°C | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
硝酸钾 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
①从上表可知,两种物质溶解度受温度变化影响较小的是__________________。
②据上表推测,氯化钠和硝酸钾溶解度相等时温度范围在_________________。
A 10℃-20℃
B 20℃~30℃
C 30℃~40℃
③若在氯化钠中混有少量的硝酸钾,提纯氯化钠的方法是_________________。
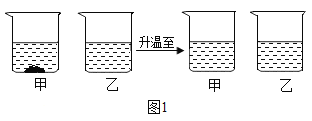
(3)20℃时,将等质量的氯化钠、硝酸钾分别放入盛有100g水的甲、乙烧杯中,充分溶解后再升温到40℃。其实验过程如图所示:40℃时甲烧杯中的溶液状态为________________(填“饱和溶液”“不饱和溶液”或“不能确定”)。
(4)乐乐同学取氯化钠、硝酸钾中的一种物质,按照下图所示进行一系列实验操作。
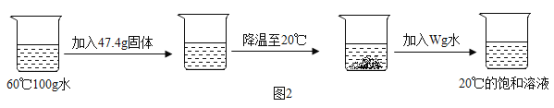
该同学所取的物质是______________________,W的数值为___________________。
(5)小明同学帮助实验员老师配制5%的氯化钠溶液80g(水的密度为1g.mL-1),正确的实验操作顺序标号为___________________。
A 用托盘天平称量4.0g的氯化钠固体
B 用托盘天平称量5.0g的氯化钠固体
C 将固体氯化钠和水在小烧杯中混合
D 将配制好的溶液装瓶,贴上标签
E 用100mL量筒量取76.0mL水
F 用200mL量筒量取75.0mL水
查看答案和解析>>
科目: 来源: 题型:
【题目】“宏微结合”——建立宏观、微观和符号之间的联系是化学学科的重要特点。如图表示氯和溴的原子结构示意图:氧气、二氧化碳和水的相互转化关系。
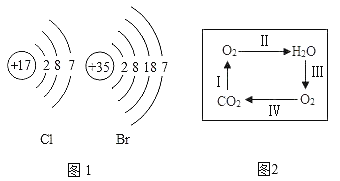
(1)图1中溴原子(Br)的核外电子层数为_________________________。
(2)氯和溴的单质具相似化学性质的原因是_________________________。
(3)从宏观角度看,图2中三种物质组成中都含有的元素是_________________________;从微观角度看,构成三种物质的微粒都是_________________________。
(4)图中Ⅲ对应的化学方程式有_________________________;以甲烷为反应物可实现转化关系的罗马数字为_________________________。
(5)在自然界中,二氧化碳转化为氧气的主要途径是_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是拉瓦锡实验所用的氧化汞分解微观示意图,下列说法不正确的是
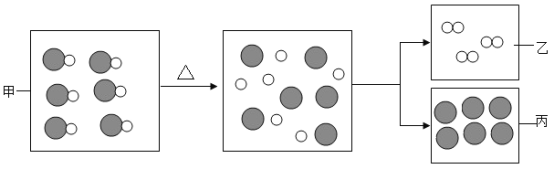
A.氧化汞属于化合物
B.构成物质的微粒是在不断运动的
C.生成物丙是金属汞
D.化学反应前后微粒的个数不改变
查看答案和解析>>
科目: 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的简要工业流程如下:
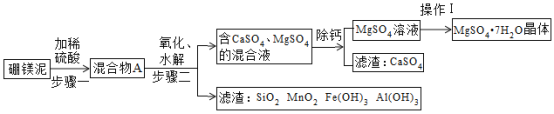
根据题意回答下列问题:
(1)实验中需要用98%的浓硫酸(p=1.84g/mL)来配制一定浓度的稀硫酸。下列所给的仪器中,属于配制过程中必须使用的有_____________(填写选项字母)。
A 普通漏斗
B 蒸发皿
C 量筒
D 烧杯
E 玻璃棒
F 药匙
(2)混合物A中,除了Mg2+、Ca2+、Mn2+、Fe2+,还含有的金属阳离子有______________(填离子符号)。
(3)经过步骤二的过程,化合价发生变化的两种金属元素是______________(填元素符号)。
(4)已知MgSO4、CaSO4溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
①从表中数据可以总结出CaSO4溶解度随温度的变化趋势是___________________。
②“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据分析,“除钙”适宜的温度是______________(填“较低温度”或“较高温度”)。
(5)“操作I”是将滤液继续蒸发浓缩,冷却结晶,________________,便得到MgSO4·7H2O。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取某些气体所用的装置如图所示,请回答:
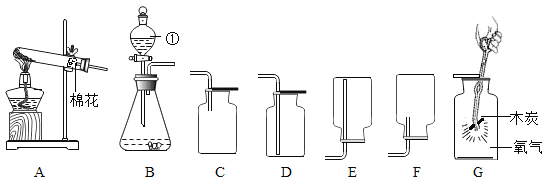
(1)图中标号①的仪器名称是__________________。
(2)组装好气体发生装置后,应该先检查装置_________________,然后再添加药品。
(3)实验室用高锰酸钾制取氧气,应选择的发生装置是________________(填序号,下同),该反应的化学方程式是__________________。
(4)欲收集密度比空气大的气体,应该选择的装置是__________________。
(5)用收集的氧气完成木炭燃烧的实验(如图G所示),观察到的现象是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组探究炼铁的反应原理。
(一)利用图装置回答问题(假设赤铁矿粉样品中的Fe2O3完全反应,赤铁矿中杂质不参与反应):
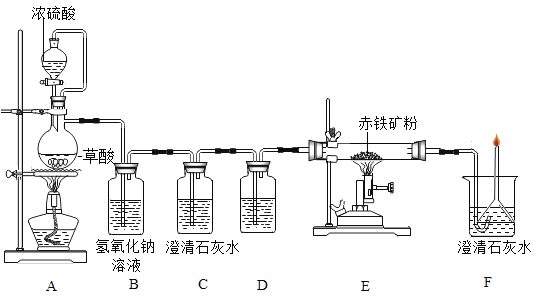
(1)A装置的作用是制取一氧化碳,反应的化学方程式为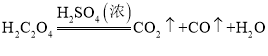 。根据反应装置判断,化学方程式中还缺少的条件是___________________。
。根据反应装置判断,化学方程式中还缺少的条件是___________________。
(2)C装置的作用是______,D装置中药品的名称是________,E装置中发生反应的化学方程式为________,F处将尾气燃烧掉的目的是______。
(3)实验中记录的数据如下表,据此计算赤铁矿中氧化铁的质量分数为________。
玻璃管质量 | 玻璃管和药品反应前质量 | 玻璃管和药品反应后质量 |
65.6g | 75.6g | 73.2g |
(4)有同学提出可以根据F装置中增加的质量来计算赤铁矿中氧化铁的质量,你同意此看法吗?
说出你的观点和理由是_______。
(二)利用图装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置和尾气处理装置略,所用固体药品为纯净物)。
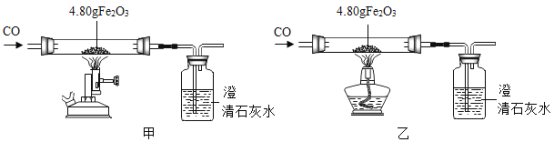
(1)反应过程中观察到,甲、乙两组的澄清石灰水均变浑浊,集气瓶中发生反应的化学方程式为________。
(2)完全反应后,甲、乙两组的生成物均为黑色粉末,分别用两组的生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 称量黑色粉末质量/g | m1 | m2 |
2 | 取黑色粉末,用磁铁吸引 | 全部被吸引 | 全部被吸引 |
3 | 取黑色粉末,加入足量CuSO4溶液 | 黑色粉末溶解,有红色物质生成 | 无明显现象 |
(注:铁的氧化物中,只有Fe3O4能被磁铁吸引)
①甲组的黑色粉末与CuSO4溶液反应的化学方程式是_____。
②小明同学查阅资料后发现Fe3O4在常温下不与CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。
小丽提出不同意见:假设乙组黑色粉末中除了有Fe3O4,还可能含有少量铁粉,铁粉的含量低,与硫酸铜溶液反应也可能无明显现象。
了进一步确定乙组生成物成分,小组同学提出,如果m2恰好为______________g,则小明的猜想正确,如果m2_____________________(填“大于”或“小于”)该质量,则乙组生成物中还含有少量铁粉。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com