
科目: 来源: 题型:
【题目】依依同学利用下列装置探究CO的还原性,并验证气体产物,实验装置如图:
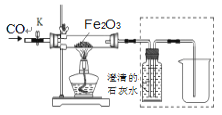
下列有关该实验的说法正确的是
A. 实验开始时,为了防止CO污染空气,应先点燃酒精灯加热,后通入CO
B. 实验中玻璃管中现象是红棕色固体变成黑色
C. 实验结束,为了防止溶液倒吸,必须先将玻璃管与虚线框内的装置断开
D. 装置图中虚线框内的装置既能检验二氧化碳,又能收集一氧化碳
查看答案和解析>>
科目: 来源: 题型:
【题目】老师为同学们提供了如下实验装置:
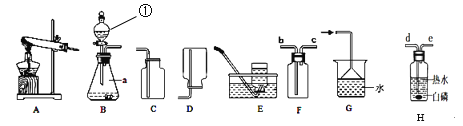
(1)实验室要用高锰酸钾制取一瓶较纯的氧气,发生和收集装置的组合是______(填字母序号),反应方程式为________;若将H装置的d端口与发生装置连接,可验证物质燃烧必需的一个条件是___________。
(2)某同学选择B装置制氧气,适合该装置的反应方程式为:________,实验仪器①的名称是____,用它代替长颈漏斗的优点是________。将完全反应后的混合物分离开来的操作是________(填一种操作名称),该操作中用到的玻璃棒的作用是________。若用F装置来收集氧气,验满的方法是_______。
(3)兴趣小组探究了影响大理石与稀盐酸反应剧烈程度的因素.
(查阅资料)反应物的浓度越大,反应速率越快.
(实验过程)(注:盐酸足量)

(实验分析)
①若要探究盐酸浓度大小对反应的影响,可选择实验甲与________对照(选填实验编号)。
②除盐酸浓度大小外,上述实验研究的另两个影响反应的因素是________和_________。
(交流讨论)与甲相比较,下列对丙的分析,错误的是_________ (选填编号)。
A、反应更为剧烈 B、产生的二氧化碳速度更快 C、产生的二氧化碳的质量更大
(4)常温下,氨气是一种有强烈刺激性气味的气体,极易溶于水,密度比空气小。实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,应该选择的发生装置是_______,若用F装置来收集氨气,气体应从________(填“b”或“c”)通入。有同学认为最好后面再连接一个G装置,这样做的目的是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下列实验常用装置,回答有关问题。
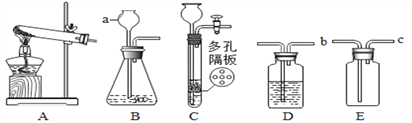
(1)图中标有字母的仪器的名称:a ______________;
(2)实验室用高锰酸钾制取氧气,应选用的发生装置_________________,反应的化学方程式是______________________________。
(3)比较用过氧化氢溶液和用高锰酸钾制取O2的方法,两者的共同点是________(填序号)。
A.发生装置相同 B.都可用MnO2作催化剂
C.反应的基本类型相同 D.完全反应后剩余固体成分相同
(4)实验室制取二氧化碳的反应方程式为____________________________;如果用E装置收集该气体,则气体从__________端进入(填“b”或“c”),若要用E装置验证二氧化碳能否与水反应,瓶中需装________,且气体从___________端进入(填“b”或“c”)。
(5)实验室常用装置C代替装置B制取气体,该装置的优点是______________________,下列反应适用于该装置的是______________(填序号) 。
a.大理石和稀盐酸 b.锌粒与稀硫酸 c. 过氧化氢溶液与二氧化锰粉末
查看答案和解析>>
科目: 来源: 题型:
【题目】水是生命之源,工业、农业、生活等各方面都离不开水。
I、下列物质加入水中能形成溶液的是_________,能形成乳浊液的是_________。(填序号)
a.植物油 b.硫酸铜 c.泥土
II、下图是实验室用溶质质量分数为10%的氢氧化钠溶液进行水的电解实验。
实验一:配制200g溶质质量分数为10%氢氧化钠溶液
(1)所需氢氧化钠的质量是______g;
(2)称量时,氢氧化钠固体应放于天平____(填“左”或“右”)盘上的_______内;量取所需的水时(水的密度为1g/cm3),应选择的量筒的规格是_______mL(选填“100”、“200”或“250”)。
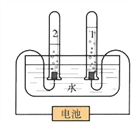
实验二:水的电解实验
(3)用如图所示装置进行水的电解实验。已知氢氧化钠在水的电解过程中,只是起到了_____________的作用。实验前管1和管2内都装满溶液,接通电源,一段时间后,两管内产生的气体情况如图所示,则管2下方的电极应连接电源的________极(填“正”或“负”),用__________的方法可验证2管中的气体。写出电解水的化学方程式:_____________。
(4)该实验能说明的事实是:___________________________。
(5)电解后溶液的溶质质量分数_____10%(填“<”、“=”或“>”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的部分信息(左下角数字表示相应元素的原子序数)。
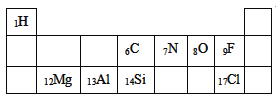
(1)上述元素中属于金属元素的有____种,决定不同元素的最本质的区别是_____不同。
(2)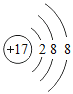 表示的是_____(写微粒符号)。
表示的是_____(写微粒符号)。
(3)地壳中含量最多的金属元素与海水中含量最多的元素组成的化合物的化学式是_____,其中显正价的元素的化合价为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学用语是学习化学的重要工具。
(1)用化学符号表示
①2个铜原子____; ②两个亚铁离子_____; ③硫酸铁中铁元素的化合价______;④地壳中含量最多的元素_____;⑤两个水分子_______;
(2)现有a.氮气 b.水 c.铜 d.武德合金四种物质,用合适的序号填空:
①常用作溶剂的是_____; ②用作导线的是______;
③用作保险丝的是_____; ④常用食品保护气的是_____;
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示的四个图像,能正确反映对应变化关系的是
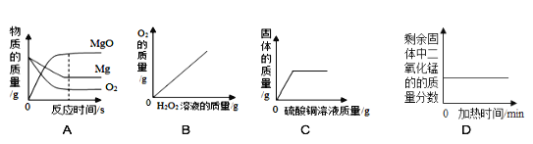
A. 一定量的镁在足量的氧气中充分燃烧
B. 向二氧化锰中加入过氧化氢溶液
C. 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
D. 加热一定质量的氯酸钾和二氧化锰的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)下图为铁元素在元素周期表中的信息,铁元素的原子序数为_______,亚铁离子(Fe2+)的核外电子数为____________。

(2)健康人体内,总量4~5g的铁元素主要以____________(选填“单质”、“化合物”)形式存在,缺铁会患上_________(填字母)。
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
【实验一】兴趣小组通过下图实验研究铁的冶炼
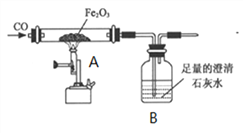
(3)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式________________________ ;
(4)实验一段时间后,观察到A处B处现象分别是____________;___________,小明将所得的黑色固体物质放入足量的稀硫酸中,发现有少量气泡。写出产生气泡反应的化学方程式___________,说明黑色固体物质___________(填字母)。
a.不含铁 b.一定全部是铁 c.含有铁
【资料1】已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
![]()
【资料2】实验研究表明:该实验得到的是四氧化三铁与铁粉的混合物
【实验二】兴趣小组用下图实验研究实验一所得黑色粉末中单质铁的质量分数
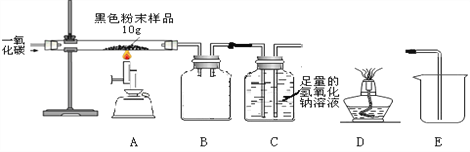
【资料3】氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,且吸收能力比石灰水强
(5)从安全与规范的角度考虑,装置C后面应连接__________(选填装置序号D或E),B装置的作用是___________。
(6)铁与四氧化三铁的混合物10 g充分反应后,玻璃管中剩余固体(单质铁)的质量为8.4g。请计算10 g黑色粉末中单质铁的质量分数________ 。
【实验三】兴趣小组为探究生铁中铁的含量(生铁中只考虑铁,碳),设计有关方案,取0.58克生铁放于试管中,实验中将注射器内76毫升稀硫酸(足量)完全注入试管中。当试管中不再产生气泡时立刻读数得到量筒中水的体积为300毫升。已知实验条件下氢气的密度为0.09g/L。
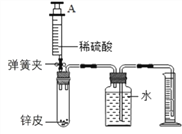
(7)计算生铁中铁的质量分数为_______?(写出计算过程,氢气质量保留两位小数,结果保留到0.1℅)
(8)上述方法测得的生铁中铁的质量分数偏小,可能的原因是_______
A.没等装置冷却就读数 B.生铁中含有少量锌
C.试管中有氢气没有排出 D. 将注射器中稀硫酸全部注入试管中后忘掉夹紧弹簧夹
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们利用如图所示装置进行气体的制备实验(A~F为装置编号)。
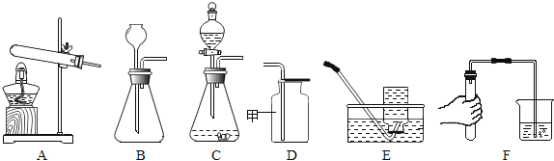
(1)写出图D装置中甲仪器的名称_____。
(2)用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为___,其中二氧化锰起____作用;收集氧气可以选择____(填装置编号)。
(3)实验室制取H2通常选择下列药品中的_____(填药品序号)。
a 浓盐酸 b 锌粒 c 铁块 d 稀硫酸
实验室制取氢气应选择的发生和收集装置的组合可以是_____(填装置编号)。
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是____(填装置编号)。
(5)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是_____(填序号)。
a 将烧杯换成水槽 b 导管深入水中位置过深,气体无法逸出
c 将水换成冰水 d 先用手捂住试管壁,再将导管另一端插入水中
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛(Ti)因为常温下不与酸、碱反应等优良性能,被誉为“未来金属”。金属钛是航空、宇航、军工、电力等方面的必需原料。由钒钛磁铁矿提取金属钛的主要工艺过程如图,请根据图示回答下列问题:
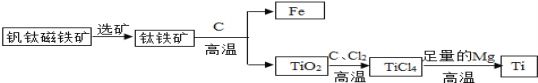
(1)钒钛磁铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为_______价。
(2)TiO2、炭粉混合在高温条件下通入氯气得TiCl4和一种可燃性气体,该步骤发生反应的化学方程式为:_________。
(3)在氩气的气氛下,用过量的镁在加热条件下与TiCl4反应制得金属钛。
①此反应的化学方程式为:____________;
②此过程中,氩气的作用是__________;
③该步骤所得金属钛中通常混有少量的杂质是______, 提纯金属钛的主要实验步骤是:先向产物中加入足量的_________充分反应后,再进行_______(填操作名称)、洗涤、干燥得金属钛。有关反应的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com