
科目: 来源: 题型:
【题目】甲、乙、丙是某同学设计的三套制取二氧化碳的发生装置,对三套装置分析不正确的是
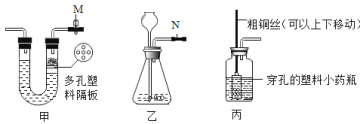
A.甲装置此时容器内右侧气压大于外界大气压
B.此时甲装置中的止水夹M处于关闭状态
C.乙装置N处添加止水夹可以与甲装置具有相同功能
D.甲装置和丙装置具有可控制反应进行或停止的功能
查看答案和解析>>
科目: 来源: 题型:
【题目】含杂质的Fe2O3固体样品20g,高温下用足量的CO完全还原(杂质不与CO反应),得剩余固体,并将生成的CO2气体用足量的澄清石灰水充分吸收后,产生30g白色沉淀.则下列说法不正确的是
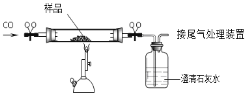
A. 通入CO质量大于8.4g
B. 反应后剩余固体质量为11.2g
C. 样品中氧化铁的质量分数为80%
D. 样品中氧元素质量分数不一定为24%
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取气体时需要的一些装置如下图所示,请回答下列问题:
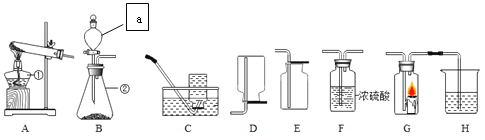
(1)标有字母a的仪器名称是________ 。
(2)实验室制取氧气和二氧化碳的发生装置都可选用装置__________(填字母序号),该装置中使用仪器a的优点是_______。
(3)检验二氧化碳是否收集满的方法是_______
(4)某兴趣小组的同学连接B、G、H装置进行实验。
①若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中反应的化学方程式为_____________________________________。
②若实验时G装置中蜡烛熄灭,H装置中溶液变浑浊,则B装置中生成的气体是__________,H装置中发生反应的方程式为_____________该气体可用于灭火的原因是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;E是易与血液中血红蛋白结合的有毒气体。它们之间的转化关系如图所示(部分转换关系反应条件已略去),请回答:
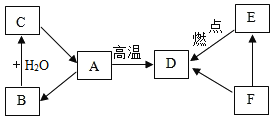
(1)写出A、C、E的化学式:A_____________C______________;E______________。
(2)写出E物质与氧化铜反应的现象:______________________________________
(3)写出A→B反应的化学方程式:________________,该反应的基本类型为_______反应。
(4)写出E转化为D的化学方程式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对CO2是否支持常见金属的燃烧进行探究活动。
(活动一)探究CO2是否支持实验室常见金属镁的燃烧
实验①:将燃着的镁条插入充满CO2的集气瓶,发现镁条仍燃烧。生成物除白色MgO外,还有一种黑色固体。(1)镁在CO2中反应的化学方程式为 ,此反应的基本类型是 。
(2)实验①的结论是 。由该结论可知 (写“能”或“不能”)用CO2灭火器扑灭活泼金属的火灾。
(3)通过实验①你对燃烧条件的新认识是 。
(活动二)探究CO2是否支持生活中常见金属铁的燃烧,兴趣小组设计如下方案:
方案①:将弯成螺旋状的细铁丝系上一支火柴,点燃火柴,待火柴快燃尽时,插入装有CO2的集气瓶中,观察铁丝能否被引燃。
方案②:将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有CO2的集气瓶中,观察铁丝能否被引燃。
实验评价:你认为方案 (填①或②)更为科学,理由是: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是
实 验 装 置 |
硫在氧气中燃烧 |
测定空气中氧气含量 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
解释 | 集气瓶中的水: 吸收放出的热量 | 集气瓶中的水: 更快的吸收白烟和反应放出的热量 | 量筒中的水: 通过水体积的变化得出氧气体积 | 集气瓶中的水: 冷却溅落融熔物,防止集气瓶炸裂 |
A | B | C | D |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是工业上将煤转化为清洁能源的微观示意图:![]()
(其中“![]() ”表示碳原子,“
”表示碳原子,“![]() ”表示氧原子,“
”表示氧原子,“![]() ”表示氢原子)有关说法不正确的是( )
”表示氢原子)有关说法不正确的是( )
A. 图中“![]() ” “
” “![]() ” 都属于氧化物 B. 该反应类型为置换反应
” 都属于氧化物 B. 该反应类型为置换反应
C. 反应前后原子的种类和数目保持不变 D. ![]() 由一个氧原子和一个氢分子构成
由一个氧原子和一个氢分子构成
查看答案和解析>>
科目: 来源: 题型:
【题目】柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:

(1)写出反应1的化学方程式:__________;
(2)操作1的名称为__________;
(3)反应3中会有气体生成,该气体是_________;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为________;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中含有丰富的氯化镁,如图是从海水中提取镁的简单流程.在提取Mg的过程中,
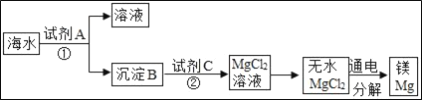
(1)试剂A最好选用_____(从我国有丰富的石灰石资源考虑).沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为_____;
(2)由无水MgCl2制取Mg的化学方程式为_____;
(3)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数. 下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
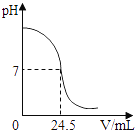
(1)根据下图曲线可以判断实验中是向________(填“酸”或“碱”,下同)溶液(待测液)中滴加________溶液(标准液).
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到________,则证明中和反应正好完成.
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com