
科目: 来源: 题型:
【题目】如图是实验室中常见的气体制备、净化、收集和性质实验的部分仪器。
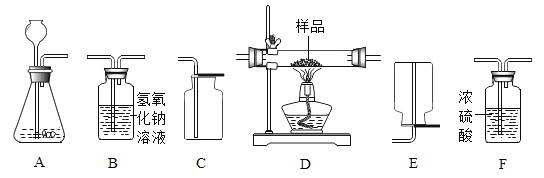
试根据题目要求,回答下列问题:
(1)在实验室中,用金属锌和稀盐酸制备氢气时,常会混有少量HCl。若收集一瓶干燥且不含HCl的氢气:
①所选装置的连接顺序为_____。
②制取气体前,需要先检查装置的_____。
③装置A中发生反应的化学方程式为_____。
④若用装置A制取CO2时,锥形瓶中应盛放的药品是_____。检验二氧化碳是否收集满的方法是_____。
(2)在实验室中,若以双氧水为原料(MnO2作催化剂)制备干燥的氧气,并用得到的氧气来测定10g由铜粉和炭粉组成的混合物样品中单质铜的含量,装置的连接顺序为:A→F→D→B(假设有关反应均恰好反应完全)。
①装置F的作用是_____。
②装置A中生成氧气的化学方程式为_____。
③D装置通入足量氧气,发生反应的类型是_____反应。充分反应后,室温下,称量玻璃管内剩余固体总质量变为8g,则原混合物样品中铜的质量分数是_____。
④实验结束后,要分离出装置A中锥形瓶内的固体,应采用的分离方法_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。该技术以从海水中提取出来的食盐(NaCl)为主要原料制取纯碱,同时还得到副产品化学肥料氯化铵 (NH4Cl)。Na2CO3、NaCl和NH4Cl的溶解度曲线如下图2所示。请回答下列问题:
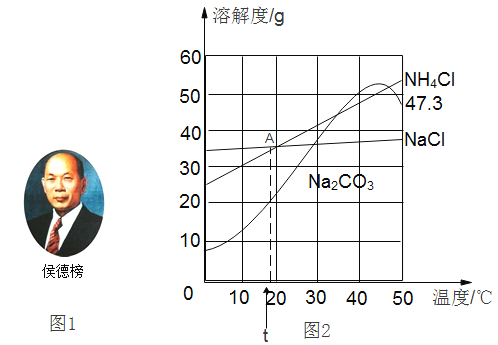
(1)图2中A点表示的含义是_____。
(2)50℃时,将碳酸钠饱和溶液降温至45℃,溶液中溶质的质量分数_____32%(选填“>”、或“<”或“=”)
(3)从下列判断中,选出有错误的一项_____。(填字母序号)
A 20℃时,将三种固体各40g分别加入100g水中,都能形成饱和溶液
B <10℃,用降温结晶法可从NH4Cl和NaCl(少量)混合溶液中分离出NH4Cl
C 50℃时,三种物质饱和溶液的溶质质量分数关系为NH4Cl>Na2CO3>NaCl
D 三种物质的饱和溶液分别从40℃降温至0℃,Na2CO3溶液中析出晶体最多
查看答案和解析>>
科目: 来源: 题型:
【题目】济青高铁是我国“四纵四横”快速铁路网青太客运通道的重要组成部分,于2018年12月26日正式开通运营。铝型材是高铁实现轻量化最好的材料。工业上利用氧化铝和六氟合铝酸钠(Na3AlF6,助溶剂,降低所需温度)在高温下炼制金属铝。请回答下列问题:

(1)氧化铝(Al2O3)中铝元素的化合价为_____。
(2)Al2O3能与氢氧化钠溶液发生反应生成偏铝酸钠(NaAlO2)和水,试写出该反应的化学方程式:_____;
查看答案和解析>>
科目: 来源: 题型:
【题目】2018年12月8日,我国“嫦娥四号”月球探测器在西昌卫星发射中心由长征三号乙运载火箭(CZ-3B)发射升空。2019年1月3日上午时分十点二十六分左右,成功降落月球背面,并通过“鹊桥”中继星传回了世界第一张近距离拍摄的月背影像图,揭开了古老月背的神秘面纱(如图),开启了人类月球探测新篇章。长征三号乙运载火箭的一、二子级推进剂都是偏二甲肼(C2H8N2)和四氧化二氮(N2O4)。试回答下列问题:

(1)N2O4属_____(选填“混合物”、“单质”、“盐”或“氧化物”中的一种)。
(2)偏二甲肼由_____种元素组成。
(3)偏二甲肼中,碳元素和氢元素的质量之比为_____(最简整数比)。
(4)偏二甲肼中,所含元素质量分数最小的元素是_____(写元素符号)。
(5)偏二甲肼和四氧化二氮发生反应的化学方程式为: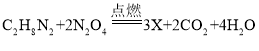 ,则X的化学式为_____。
,则X的化学式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有一定量MgO和Fe2O3组成的混合物,加入200g质量分数为9.8%的稀硫酸,恰好完全反应。下列判断中错误的是
A.上述过程中发生的都是中和反应
B.所加稀硫酸中溶质的质量为19.6g
C.所加稀硫酸中氢元素的质量为0.4g
D.原固体混合物中氧元素的质量为3.2g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应方程式书写都正确,但不符合实际的是
A.实验室加热氯酸钾(MnO2作催化剂)制氧气:
B.用适量稀盐酸除去水垢中的Mg(OH)2:![]()
C.用烧碱治疗胃酸过多:![]()
D.盛放石灰水的试剂瓶内壁易产生白膜:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示某化学反应的微观过程,其中![]() 表示氮原子,
表示氮原子,![]() 表示氧原子,
表示氧原子,![]() 表示氢原子下列结论中错误的是
表示氢原子下列结论中错误的是
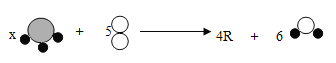
A.X=4
B.R的化学式为NO
C.反应后分子数增多
D.该反应是复分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某粒子的结构示意图为 ,下列有关该粒子的判断中错误的是
,下列有关该粒子的判断中错误的是
A.可能是原子、阴离子或阳离子
B.化学性质很稳定
C.当a=11时,x=8
D.若a-x=0,符号是O2-
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有80g碳酸钠溶液。将90g氯化钙溶液分四次加入,充分反应,四次测量所得数据如下表所示:
次数 | 一 | 二 | 三 | 四 |
加入氯化钙溶液的质量/g | 20 | 20 | 20 | 30 |
烧杯中溶液的总质量/g | 97 | 114 | 131 | 160 |
(1)恰好完全反应时,生成沉淀的总质量为_____g。
(2)第三次测量时,所得溶液中的溶质有_____(填化学式)。
(3)计算氯化钙溶液的溶质质量分数_____(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
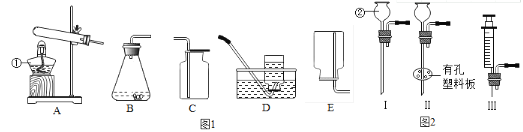
(1)写出图中带标号仪器的名称:①_____②_____。
(2)若实验室对你开放,请从图1中选择合适的装置,制取一种你熟悉的气体。你想制取的气体是_____,选择的发生装置是_____(填序号,下同),选择的收集装置是_____,选择此收集装置的理由是_____。
(3)装置B虽然操作简便,但无法控制反应速率。请从图2中选取_____(填序号)取代装置B中的单孔塞,以达到控制反应速率的目的。
(4)探究制取氧气的适宜催化剂。
实验方案如下:
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用左下图装置进行实验。改用其他三种海藻酸钠微球,分别重复上述实验,得到右下图的锥形瓶内压强随时间变化的曲线图。
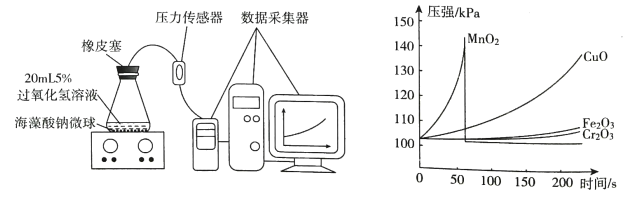
①每次实验时,海藻酸钠微球数应相同的原因是_____
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_____。
③从实验曲线看,催化效果较好、反应温和的催化剂是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com