
科目: 来源: 题型:
【题目】某化学兴趣小组通过微型实验探究蜡烛燃烧的产物,用数字化实验监测密闭容器内蜡烛燃烧时氧气、二氧化碳和水蒸气含量的变化,形成三条曲线,如图所示,说法不正确的是
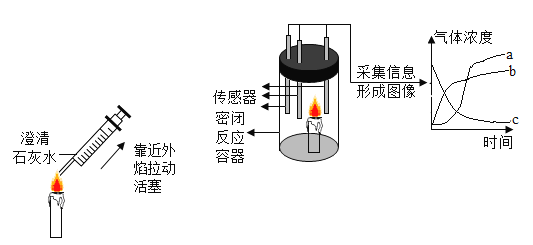
A.用注射器抽气并振荡,可观察到石灰水变浑浊
B.蜡烛在燃烧后生成了CO![]() 和H
和H![]() O的曲线是a和c
O的曲线是a和c
C.数字化实验能为科学探究提供更为直观的证据
D.微型实验可探究得出蜡烛燃烧以后的部分产物
查看答案和解析>>
科目: 来源: 题型:
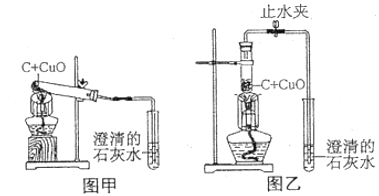
【题目】某中学化学兴趣小组按照课本实验方法(如图甲),儆木炭与氧化铜反应实验时发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。
(提出问题)
暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
(查阅资料)
铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
(猜想与假设)
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为_____。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
(分析与交流)
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是_____。
(2)小周建议用图乙装置代替甲装置。他认为这样改进有利于集中加热,获得持续高温。
(实验与结论)
同学们决定按改进后的方案进行实验,他们在检验了乙装置的_____后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,_____(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。不久,即可看到试管底部变紅热停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是_____(填“吸”或“放”)热反应。待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是_____。待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室制取和收集气体的常用装置图,请根据所给的装置图回答下列问题:
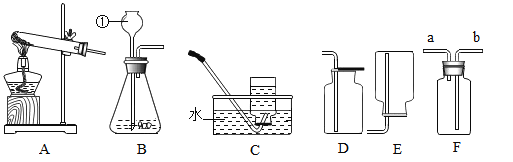
(1)请写出装置图中①的仪器名称:_____。
(2)实验室既能制取氧气,也能制取二氧化碳的发生装置为_____(填字母代号)。请写出用该装置制取二氧化碳的化学方程式_____。
(3)实验室常用氯化铵固体和熟石灰固体混合加热制取极易溶于水的氨气(NH3的相对分子质量为17),请根据以上装置图选择,在实验室制取氨气时的发生装置和收集装置_____(填字母代号)。
(4)实验室里通常用MnO2与浓盐酸在加热条件下制取氯气,如果用F装置收集氯气(Cl2的相对分子质量为71),气体应从_____(填“a”或“b”)端管口通入。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列方框图简答:
已知:A、B、C、D、E都是初中化学常见的物质。A和C在常温下均为无色液体,B是由两种元素组成的清洁能源;D与E含有相同的两种元素,且E是有毒气体;F含有A-E的所有元素。
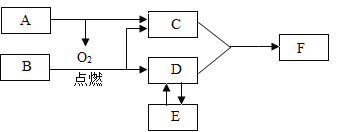
(1)请推断物质的化学式:F_____。
(2)写出物质A转化为C的化学方程式_____。
(3)写出D转化为E的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】学习化学后,我们可以用所学的化学知识回答生活中与化学相关的问题。
(1)目前部分农村的饮用水主要还是地下水。饮用遭到污染或硬度大的地下水不利于人体健康。
①检验某地下水是硬水还是软水,物质是_____。
②自来水生产过程中,可用沉降、_____方法除去水中不溶性杂质,同时还必须进行消毒。X是一种新型的自来水消毒剂,工业上制取X的化学方程式为![]() ,则X的化学式为_____。
,则X的化学式为_____。
(2)现在,我们家里厨房做饭用的主要燃料为天然气,天然气的主要成分是甲烷,家用燃料经过了如下的更新过程:

下列有关家用燃料更新的理由,正确的是_____。
A 天然气是新能源,取之不尽用之不竭
B 气体燃料的利用率更高
C 减少煤燃烧过程中产生的污染物
查看答案和解析>>
科目: 来源: 题型:
【题目】请用化学用语填空:
(1)2个氢氧根离子_____;
(2)3个铵根离子_____;
(3)空气里含量最多的气体并标出化合价_____;
(4)地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学反应的微观示意图如下,根据该图得出的结论,正确的是
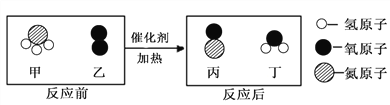
A. 四种物质中只有丙属于氧化物
B. 该反应为化合反应
C. 该化学反应方程式为4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
D. 若有17 g 物质甲参加反应,生成物丁的质量为18 g
查看答案和解析>>
科目: 来源: 题型:
【题目】因外观相似,某同学不慎将一包氯化钠粉末与一包碳酸钠粉末混在了一起。某研究小组的同学欲探究这份粉末中各组分的含量,做了如下实验:

a.将粉末混合均匀,取10g,加入45.7g水中,充分溶解配制成溶液;
b.向所配溶液中逐滴滴加溶质质量分数为10%的稀盐酸;
c.将产生的气体先通过浓硫酸,再通入足量的氢氧化钠溶液中(如图),测量氢氧化钠溶液的增重(其它误差忽略不计);
d.绘制氢氧化钠溶液增重(g)与滴加稀盐酸质量(g)的关系曲线如下图。

请完成下列问题:
(1)反应过程中,生成二氧化碳的总量为_____g。
(2)当恰好完全反应时,溶液的pH_____7(选填“>”、“<”或“=”);计算此时所得溶液中溶质的质量分数。_______(精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图,请回答下列问题:
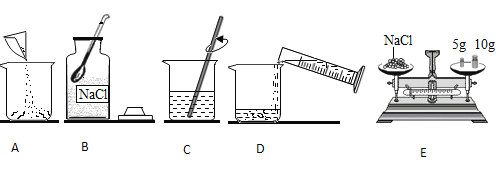
(1)配制NaCl溶液的正确操作顺序_____(填写字母标号)。
(2)称量NaC1时,天平平衡后的状态如图E所示,游码标尺示数如图,则称取的NaCl质量为_____g。
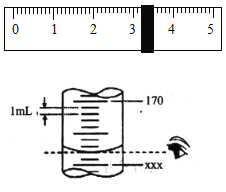
(3)通过计算求出所需水的体积(mL)用250mL量筒(每一小格代表1mL)量取水的体积,如上图中读取的数值是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】目前世界上生产的金属镁60%来自于海水。分离出食盐的海水称作苦卤水,其中含有丰富的MgCl2。工业上以苦卤水为原料制取金属镁的流程如下图

(1)生石灰转化为熟石灰的化学反应方程式为_____。
(2)Y的化学式为_____;Y与Z反应生成x,实现了Y的循环利用,X的名称是_____。
(3)烘干后得到的固体MgCl2中可能含有的少量杂质是_____(填写字母编号)。
A Ca(OH)2
B CaCl2
C NaCl
(4)简述用pH试纸测定溶液pH的方法_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com