
科目: 来源: 题型:
【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验设计 |
|
|
|
|
实验目的 | 探究二氧化锰能否加快过氧化氢分解 | 探究石蜡燃烧后是否有二氧化碳生成 | 检验氧气是否集满 | 测定空气中氧气的含量 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】冰毒(主要成分:甲基苯丙胺)对人的中枢神经系统有强烈的刺激作用,人吸食后会产生强烈的生理兴奋,大量消耗体力,降低免疫力,严重损害心脏和大脑组织,吸食过量会导致死亡,青少年应拒食毒品,远离毒品。甲基苯丙胺的化学式为C10H15N,下列有关甲基苯丙胺的说法错误的是
A. 甲基苯丙胺是一种有机物
B. 甲基苯丙胺是氢元素质量分数最大
C. 甲基苯丙胺由碳、氢、氮三种元素组成
D. 甲基苯丙胺中碳、氢、氮元素质量比为120:15:14
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒,如图为过氧乙酸的分子结构图(其中![]() 代表碳原子,
代表碳原子,![]() 代表氢原子,
代表氢原子,![]() 代表氧原子),下列有关说法正确的是( )
代表氧原子),下列有关说法正确的是( )
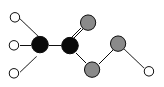
A. 过氧乙酸的化学式是CH3COOOH(或C2H4O3)
B. 过氧乙酸是由碳、氢、氧三种元素构成的
C. 过氧乙酸中碳、氢、氧三种元素的质量比是12:1:16
D. 过氧乙酸中碳元素的质量分数是40%
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为测定一瓶未知浓度稀盐酸的溶质质量分数,取146g该稀盐酸于烧杯中,然后将20 g锌粉(含部分杂质,杂质不溶于稀盐酸)分5次加入,所加锌粉的质量与烧杯中剩余物质总质量的关系如下表所示,请计算:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入锌粉的质量/g | 4 | 4 | 4 | 4 | 4 |
剩余物质总质量/g | 149.9 | 153.8 | 157.7 | 161.6 | 165.6 |
(1)生成氢气的总质量为___________________________g;
(2)该未知浓度稀盐酸的溶质质量分数_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在做完K2CO3溶液与Ba(OH)2溶液反应的实验后,将试管中的剩余物一起.倒入含有氯化铁的废液缸中,看到“白色沉淀中混有红褐色沉淀”的现象。过滤,得无色溶液。
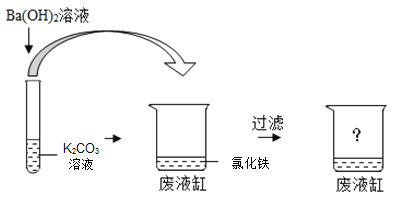
(1)写出试管中所发生反应的化学方程式____________________。
(2)为了确定所得无色溶液中溶质的组成,请你和同学们一起进行如下探究:取少量溶液于试管中,加入Na2SO4溶液,无明显现象。进行该实验的目的是为了检验溶液中是否含有__________________________ (填离子符号)。
探究过程中同学们提出了如下猜想,请完成猜想三。
猜想一:KCl和K2CO3
猜想二:KCl和KOH
猜想三:__________。
猜想四:KCl、K2CO3和KOH
查阅资料:CaCl2溶液呈中性;K2CO3溶液呈碱性。
同学们设计了如下实验方案:
方案1:取少量溶液于试管中,加入石灰水,再滴入酚酞溶液;
方案2:取少量溶液于试管中,加入足量的CaCl2溶液,再滴入酚酞溶液。
经过讨论后大家一致认为方案__________不合理,理由是____________________。
方案2中加入足量的CaCl2溶液的目的是____________________。
实验及结论:同学们用方案2进行实验,最后证明猜想四正确,则同学们在实验过程中观察到的现象是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列所给实验室常用制气装置回答问题。

(1)B装置中一处明显的错误是____________________,利用改正后的装置完成后面的实验;
(2)实验室加热二氧化锰和氯酸钾固体混合物制取氧气,若需收集一瓶较纯净的氧气,则其发生和收集装置应选择_________________,发生反应的化学方程式为___________其中MnO2起_____________________作用;
(3)若用稀盐酸与石灰石制取二氧化碳,应选用的发生和收集装置是____________________;实验中判断二氧化碳是否收集满的操作方法是____________________;反应产生的二氧化碳在收集之前,需将气体先通过F装置进行除杂,则该装置中加入的药品需更换为____________________。
(4)已知氯气(Cl2)在常温常压下为黄绿色有刺激性气味的有毒气体,易溶于水,密度比空气大,若用G装置收集氯气,气体应该从__________________________(填“a”或“b”)端通入。
查看答案和解析>>
科目: 来源: 题型:
【题目】水垢(主要成分为碳酸钙、氢氧化镁)俗称.“水锈、水碱”,是指硬水煮沸后所含矿物质附着在容器内逐渐形成的白色块状或粉末状的物质。实验室用水垢制取氯化钙的流程如下:
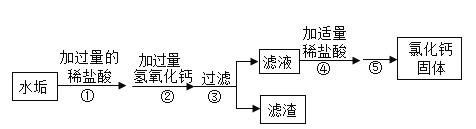
(1)过滤的目的是______________________________,过滤操作中滤纸应紧贴______________________________。
(2)写出步骤②中生成沉淀的化学方程式______________________________,该反应的基本类型是______________________________。
(3)步骤④中加入过量稀盐酸的目的是______________________________。
(4)步骤⑤是利用______________________________的方法得到氯化钙固体。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学对实验台.上的一包白色固体样品产生了兴趣,老师告诉他里面可能含有BaCl2、( NH4)2SO4、NH4Cl、CuSO4中的一种或几种,于是他取样品进行了如下实验(假设各步都恰好完全反应):

(1)A的化学式是______________________________。
(2)白色固体中一定存在的物质是__________________________(填化学式,下同),可能含有的物质是__________________________。
(3)生成白色沉淀E的化学方程式为__________________________;无色溶液D中的溶质是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图1是某同学在学习完溶解度后所做的实验,请回答下列问题:

(1)若20°C时,甲物质的溶解度为m,则m的取值范围是____________________________;A、B、C三个烧杯中一定属于甲物质的饱和溶液的是____________________________(填字母);
(2)图2是硝酸钾的溶解度曲线。硝酸钾的溶解度随温度的变化趋势是____________________________;20 °C时,在50g水中加入12.5g硝酸钾固体,此时该溶液中溶质的质量分数为____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C三种固体物质的溶解度曲线如图所示。请回答。
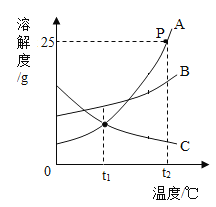
(1)t1°C时,A、C的溶解度大小关系是____________________________________。
(2)A、B、C三种物质的溶解度随温度升高而减小的是____________________________。
(3)P点时,A的溶液为该温度下的____________________________(填“饱和”或“不饱和”)溶液;
(4)t2°C时,A、B、C三种物质的饱和溶液溶质质量分数的大小关系为____________________________。
(5)C中含少量B时可采用____________________________的方法提纯C。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com