
科目: 来源: 题型:
【题目】海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是( )
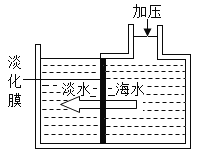
A. 溶质质量增加B. 溶液质量不变
C. 溶剂质量减少D. 溶质质量分数不变
查看答案和解析>>
科目: 来源: 题型:
【题目】PbO能溶解在不同浓度的NaOH溶液中,其溶解度曲线如图所示。下列叙述错误的是

A. 100℃时,PbO在35%NaOH溶液中的溶解度为100g·L-1
B. 60℃时,PbO在35%NaOH溶液中的溶解度大于在10%NaOH溶液中的溶解度
C. 20℃时,PbO在10%NaOH溶液中所溶解的质量,一定小于在35%NaOH溶液中所溶解的质量
D. 80℃时,将PbO溶解在10%NaOH溶液中达到饱和,然后降温至40℃,该过程中一定析出固体
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大,如表中液体X和固体Y的组合,符合题意的是( )
① | ② | ③ | ④ | ⑤ | |
X | 稀盐酸 | 水 | 水 | 双氧水 | 水 |
Y | 铁粉 | 氢氧化钠 | 氯化钠 | 二氧化锰 | 硝酸铵 |
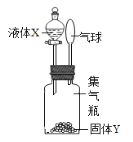
A. ①②⑤ B. ①③④ C. ①②④ D. ②③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】为了分析生铁中铁的含量,某学习小组进行了实验研究,即取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).

说明:生铁中杂质不溶于水,不与盐酸反应.
(1)铁完全反应用去盐酸的质量为_____g.
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)_____。
(3)某同学列出了如下计算式:生铁与盐酸刚好反应完全时所得溶液质量=(73+6﹣a)g小明对该计算式提出了质疑,请指出其中的错误_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下探究实验.
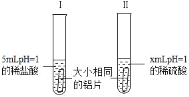
(1)铝与稀硫酸反应的化学方程式为_____.
(2)x=_____,选择此数值的理由_____.实验过程中,可以通过观察_____来比较铝与稀盐酸和稀硫酸反应的剧烈程度.
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立.
为了验证上述猜想是否正确,向试管Ⅰ中加入少量_____(填序号),向试管Ⅱ中加入少量_____(填序号),作对比实验.
A 硫酸铜 B 氯化钠 C 硫酸钠 D 浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅰ中反应快慢无明显变化,试管Ⅱ中反应明显加剧,则_____猜想成立.
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟 | 加入稀硫酸后20分钟 | 加入稀硫酸后 | 加入稀硫酸后40分钟 | 加入稀硫酸后50分钟 |
232.4g | 232.3g | 232.2g | 232.1g | 232.1g |
(1)完全反应后生成氢气的质量为______g.
(2)计算该黄铜中铜的质量分数为________(写出计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行如下实验:
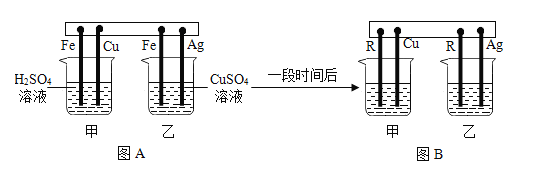
(1)如图A所示,将四根金属丝同时插入烧杯中。甲中可观察到的现象是铁丝表面产生____,溶液由无色变为____色。乙中发生反应的化学方程式是____________________。
(2)一段时间后,将烧杯中铁丝替换为R进行实验,如图B所示。若甲中出现气泡,乙中无明显现象,则烧杯乙中的溶质是___,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象,能正确反映对应变化关系的是( )
A.  向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
向氯化铜和盐酸的混合溶液中加入过量氢氧化钠溶液
B. 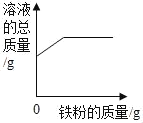 向一定量的硫酸铜溶液中加入铁粉
向一定量的硫酸铜溶液中加入铁粉
C. 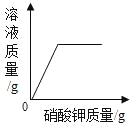 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
D. 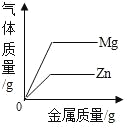 向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
向两份等质量等浓度的稀盐酸中分别加入足量的锌粉和镁粉
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组同学欲通过实验探究金属的性质。
【实验目的】证明金属活动性强弱:Al > Cu
【设计并实施实验】小组内的3位同学分别做了下述实验:
实验 | 现象 | |
甲 | 将铝片直接放入到稀CuCl2溶液中 | 一段时间后才出现了预期的实验现象 |
乙 | 将用砂纸打磨过的铝片放入稀CuCl2溶液(与甲实验浓度相同)中 | 十几秒内即观察到明显现象。 |
丙 | 将用砂纸打磨过的铝片放入稀CuSO4溶液中 | 在与乙相同的时间内没有观察到明显现象 |
(1)实验中,预期的实验现象是________。
(2)对比甲、乙两位同学的实验,推测甲同学开始时没有观察到明显实验现象的原因是________。
该小组同学进一步对实验进行探究。
【提出问题】为什么打磨过的铝片放入到CuCl2溶液和CuSO4溶液中观察到的现象不同呢?
【微观探析】查阅资料可知两个反应的微观示意图如下。

(3)图1反应的化学方程式为________;Al和CuCl2溶液、CuSO4溶液反应的微观本质是Al和Cu2+反应生成 Al3+和______ 。
【提出猜想】根据上述图示,小组同学提出了如下猜想。
猜想1:产生现象不同的原因是CuCl2溶液比CuSO4溶液中含有的Cu2+浓度大。
猜想2:溶液中Cl-对Al和Cu2+反应有促进作用。
猜想3:溶液中SO42-对Al和Cu2+反应有阻碍作用。
【设计并实施实验】
序号 | 实验方案及操作 | 现象 | 结论 |
1 | 乙、丙两位同学取Cu2+浓度相同的CuCl2溶液和CuSO4溶液重复实验。 | 与上述乙、丙同学实验现象相同 | 猜想1______(填“成立”或“不成立”) |
2 |
| 在同一时间内,③最快产生现象,②次之,①无明显现象 | 猜想2成立 |
(5)甲同学认为通过实验2得到的结论证据不充足,其理由是溶液中的__________ 对实验可能有干扰。
(6)丙同学通过查阅资料排除了上述干扰,并模仿实验2又设计了一组3支试管的实验,证明了猜想3也成立。请在下列方框中画出实验设计图示。__________

查看答案和解析>>
科目: 来源: 题型:
【题目】某同学家中有一袋化肥,可能混入了其他化肥,且化肥包装袋上的字迹模糊.该同学进行了如下探究,请你参与探究并填空:
[提出问题]该化肥中含有什么物质?
[收集信息]经询问得知,该化肥为铵态氮肥.
[提出猜想]该化肥所含的阴离子可能是Cl-、![]() 、
、![]() ;中的一种或几种.
;中的一种或几种.
[实验、记录与分析]
实验操作步骤 | 实验现象 | 实验分析 |
(1)取少量该化肥样品和少量熟石灰放在研钵中混合研磨 | ________ | 含有铵根离子 |
(2)另取少量该化肥样品于试管中,加入适量的水完全溶解,滴加足量的硝酸钡溶液,再滴加少量稀硝酸,过滤 | 产生白色沉淀,沉淀不溶解 | 没有________(填化学式)存在 |
(3)取(2)中所得滤液少量于试管中,滴加________ | ________ | 有Cl-存在 |
[实验结论]若该化肥中只含有一种阳离子,则其中一定含有的物质是(写化学式)________________________________________________________________________.
[实验反思]若步骤(2)中用氯化钡溶液代替硝酸钡溶液是否可行?________(填“是”或“否”),请简要说明原因:________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com