
科目: 来源: 题型:
【题目】化学与生活息息相关。
自热米饭的营养成分表
营养素 | 每份含量 |
油脂 | 23.5g |
糖类 | 104.7g |
维生素 | 3.5g |
钠 | 814mg |
钙 | 130mg |
水 | 小于210g |
(1)自热米饭是一种快餐食品。请根据如图及表信息,回答下列问题:

①从“自热米饭的营养成分表”看,表中没有标出的人体必须的营养素是_________;
②图 1 包装材料是符合卫生标准的铝箔。铝被压制成铝箔,说明铝具有良好的_________性;
③该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反 应的化学方程式为__________。
(2)良好的家居环境带来美好的生活。
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲 醛、苯等有毒气体,这是利用活性炭的___________性。
②如图,“火立熄”是一种新型的家用灭火用品。“火立熄”接 触到火焰 3-5 秒后炸开,释放的粉末覆盖在燃烧物上,同时放出 不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理是____________。

查看答案和解析>>
科目: 来源: 题型:
【题目】某金属冶炼厂的工业废渣中含有泥沙和某些单质,其中单质含有铜、锌和少部分 硫。现欲回收铜和锌,并对硫进行处理,主要流程如图所示:
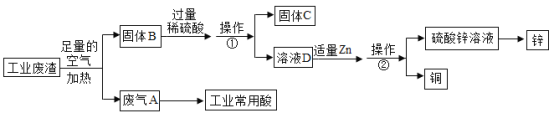
(1)在废气 A 中,一定含有的有害气体是__________(填化学式)。操作①的操作名称是___________。
(2)溶液 D 中含有的溶质是___________(填化学式)。写出由固体 B 生成溶液D 的其中一个反应的化学方程式:_______________。
(3)有人认为若第一步中空气不足量,会导致锌的回收率降低,你认为是否正确?_____(填“正确”或“不正确”),理由是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二甲醚(C2H6O)以其无污染、易于制造的特征,可能成为一种全新的替代能源而普及。 有关二甲醚的叙述正确的是
A.二甲醚由 9 个原子构成
B.2.3 g 二甲醚中含碳元素的质量为 1.2 g
C.二甲醚中碳、氢、氧三种元素的质量比为 2︰6︰1
D.二甲醚和甲烷在氧气中完全燃烧的产物不相同
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动中,学生利用下图所示的材料完成探究实验,杠杆已调至平衡。

(1)实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与_________发生了反应。将铁粉换成下列物质中的________(填序号),杠杆也会出现相似现象。
A.NaCl B.NaOH C.CaO
(2)实验2中,通入CO2一段时间,右边乒乓球___________(填“上升”或“下降”)。再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,发生反应的化学方程式为_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】石墨烯是一种革命性材料,具有优异的光学、电学和力学特性。图为金刚石、石墨和石墨烯的结构模型图,图中小球代表碳原子。下列说法正确的是( )
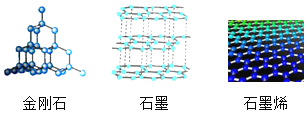
①石墨烯是一种新型化合物
②三种物质分别在足量的氧气中完全燃烧的产物相同
③金刚石和石墨烯是组成相同但结构不同的两种物质
④石墨烯有超强的导电性和导热性,说明石墨烯的化学性质和金属相似
A. ①④ B. ②③ C. ①③ D. ②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸发现于公元8世纪,在古代中国,稀硫酸被称为“绿矾油”。它是一种无色油状粘稠液体,难挥发,易溶于水,10.36℃时结晶,通常使用的是它的各种不同浓度的水溶液。硫酸是一种最活泼的二元无机强酸,能和许多金属发生反应,在有机合成中可用作脱水剂和磺化剂,是一种重要的工业原料,工业上常用塔式法和接触法制取。高浓度硫酸有强烈吸水性,与水混合时,会放出大量热,它还具有强烈的腐蚀性和氧化性,故须谨慎使用!此外,部分地区的酸雨和金星的上层大气中,均含有硫酸。

(1)下列关于硫酸用途的说法中,正确的是__________。(填序号)
①浓硫酸可作氧气的干燥剂
②稀硫酸可用于中和碱性废水
③浓硫酸主要用于生产化肥
④浓硫酸可用于冶金、制药、石油化工行业等领域
A ①②
B ③④
C ①③④
D 以上全部都是
(2)如不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的_______溶液,以防灼伤皮肤。
(3)在化学实验室中,我们往往要根据实际需要,稀释浓硫酸来配制一定溶质质量分数的稀硫酸。稀释浓硫酸的安全操作为___________________。
(4)小瑾同学想测定稀释后所得某硫酸溶液的溶质质量分数,她取了10g样品溶液,向其中滴加了足量的氯化钡溶液,所加氯化钡溶液质量与产生沉淀的质量关系如下图所示:
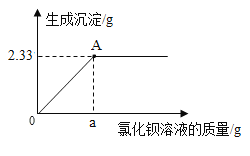
试回答下列问题:
①当滴入氯化钡溶液ag时(即图中A点),此时所得溶液中的溶质为_____________(写化学式)。
②试计算该稀硫酸样品的溶质质量分数?(根据化学方程式计算,结果精确至0.1%)_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验室现有一包固体样品A,其中可能含有Fe、NaOH、Na2CO3、Ca(OH)2四种物质中的一种或多种。小颖同学按下图所示进行成分组成探究实验,出现的现象如图中所述。(假设所有能发生的反应都恰好完全进行)
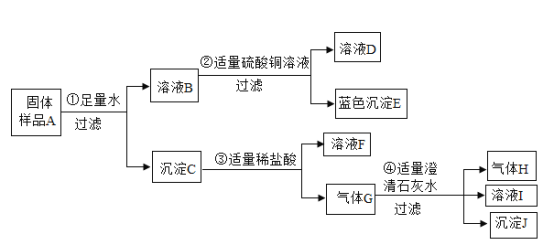
根据上述信息和分析推理,试回答下列问题:
(1)蓝色沉淀E的化学式为__________。
(2)气体H的化学式为_________,由此可推知样品A中一定含有________________。
(3)写出步骤①中反应的化学方程式___________。
(4)写出步骤③中发生的复分解反应方程式_______________,溶液F的颜色为______________。
(5)根据上述实验信息,仍不能确定是否存在的物质是______________,你的理由是:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示为实验室中常见气体制备、净化、收集实验的部分仪器装置,(组装实验装置时,可重复选择仪器),某化学小组同学欲利用其进行下列实验探究。
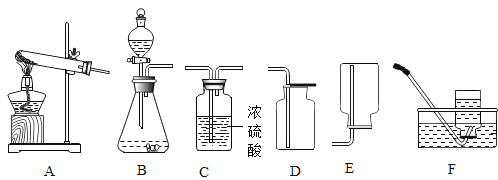
(1)小瑾同学以过氧化氢溶液为原料(二氧化锰作催化剂),在实验室中制取并收集干燥的氧气。她按照要求设计了实验装置,连接仪器,并检查了装置的气密性。
①她所选装置的连接顺序应为_______(填写装置序号字母)。
②她制取氧气所发生反应的化学方程式为__________。
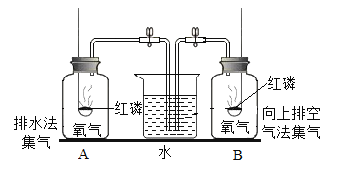
③小瑾和小颖分别用排水法、向上排空气法各收集了一瓶氧气A与B,并按下图所示进行了合作实验探究:她们将燃烧匙内的足量红磷点燃,同时伸入两个集气瓶中并迅速塞紧瓶塞,待燃烧停止并冷却后,打开止水夹,观察到进入A、B两瓶中水的体积分别约占集气瓶总体积的95%和70%。据此对两种气体收集方法进行比较,可知:___________法收集的氧气纯度更高。
(2)小黄同学想探究二氧化碳的有关性质,他设计了下图所示的实验方案,并进行了实验探究:
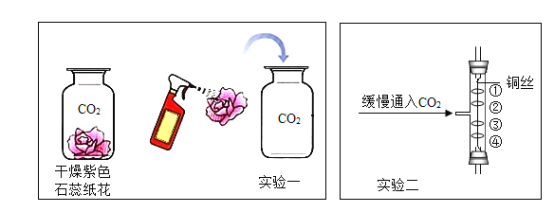
①实验(一)中,将干燥紫石蕊纸花直接放入CO2中,无明显现象;将干燥紫色石蕊纸花喷水后再放入CO2中,纸花变成红色,该现象涉及的反应方程式为__________________。
②实验(二)是升级版的改进实验,根据CO2的性质,试推测能观察到的实验现象有(注:①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。)________________。(至少写一个)
(3)将少量CO2气体通入盛有大量澄清石灰水的烧杯中,该反应的化学方程式为________。完全反应后,烧杯中溶液的质量与之前相比较会__________________。(填序号)
A 增大
B 减小
C 不变
D 无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】能源的综合利用、研发与社会可持续发展密切相关。目前应用最广泛的能源是煤、石油、天然气等化石燃料。
(1)下图是家用燃料的更新历程:

①下列有关家用燃料更新的理由错误的是。_______(填序号)
A 燃料使用更便捷
B 气体燃料燃烧的更充分
C 天然气是可再生的能源
D 减少煤燃烧过程中产生的污染物
②煤被誉为“工业的粮食”,它属于__________(填“纯净物”或“混合物”)。工厂锅炉用的煤通常加工成粉末状,原因是_______________________。
(2)汽油中加入适量乙醇即得到乙醇汽油,下列有关说法中不正确的是_______。(填序号)
A 乙醇属于可再生能源
B 乙醇汽油不能用作汽车燃料
C 使用乙醇汽油可减少大气污染
D 使用乙醇汽油可节省石油资源
乙醇C2H5OH完全燃烧的化学方程式为:________________________。
(3)天然气(主要成分是甲烷CH4)和液化石油气(主要含丙烷C3H8和丁烷C4H10)中碳元素的质量分数分别约为75%和82.3%,通过该数据相同条件下,用天然气作燃料要比液化石油气更环保的理由是______________。甲烷在空气中完全燃烧的化学方程式为_______________________。
(4)目前,化石燃料正面临着日益枯竭的危机,开发和利用清洁而又高效的能源,是21世纪人类面临的重要课题。2019年11月24日,济南首批10辆氢能源燃料电池公交车投入K115路线运营,加注一次氢气能运行350公里以上。按照每辆车每年运行3万公里计算,预计每年能替代燃油78.5吨,减少碳排放284.5吨。氢能被誉为“未来最理想的能源”,其优点为____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学学科有专用的符号语言,简称化学用语,我们应充分学好、用好它们。
(1)请按要求从氢气、二氧化碳、氧化铜、盐酸、硫酸、氢氧化钙、碳酸钙中选择合适的物质,将其化学式填写在下列横线上。
①一种气体燃料________;
②一种金属氧化物________;
③一种微溶性碱________;
④胃酸的主要成分________。
(2)尿素,又称碳酰胺,化学式为CO(NH2)2,外观为无色或白色针状或棒状结晶体,无臭无味,易溶于水,对热不稳定,在酸、碱、酶作用下能水解生成氨和二氧化碳。它是动物蛋白质代谢后的产物,通常用作植物的有机态氮肥。尿素是重要的有机化工原料,可以作为三聚氰胺、脲醛树酯、咖啡因、味精等多种产品的生产原料,它还广泛应用于医药、农药、化妆品、塑料等领域。

根据上述信息,请回答:
①上述有关尿素性质的描述中,属于物理性质的是___________(写出一项即可)。
②尿素属于___________(选填“混合物”、“氧化物”、“有机化合物”之一)
③尿素中,碳元素和氢元素的质量比为_______(填最简整数比)。
④30g尿素中含有__________g氮元素。
⑤工业上常用液氨(NH3)和二氧化碳为原料,在高温高压条件下直接合成尿素,同时生成水,该反应的化学方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com