
科目: 来源: 题型:
【题目】为验证“加热碳酸氢铵”所发生的变化和产物,两同学分别用甲、乙所示装置进行实验。

(1)甲实验中的现象是_______________。
(2)乙实验中试管口略向下倾斜的原因是_______________。乙实验中烧杯内反应化学方程式为_______________;实验中棉花逐渐变红色,则可说明反应产物中有_______________;相对于甲实验来说,乙实验的优点有(写一条)_______________。
(二)将一定量的K2CO3溶液与BaCl2溶液混合,过滤反应后的混合物。某兴趣小组的同学们欲探究滤液中溶质的组成。请你一同参与探究并回答有关问题:
[查阅资料]K2CO3溶液显碱性; BaCl2、 KCl溶液显中性。
[提出猜想]猜想1:滤液溶质是KCl;
猜想2:滤液溶质是_______________。
猜想3:滤液溶质是KCl和K2CO3。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
① 取少量滤液于试管中,滴几滴无色酚酞试液,振荡 | 无明显现象 | ①猜想_________不成立 |
② 另取少量滤液于另一支试管中,滴加K2CO3溶液 | ______________ | ②猜想2成立。 写出相关的化学方程式 _____________ |
[问题讨论]小丽同学认为要证明猜想2成立也可改用AgNO3溶液,你认为小丽同学不能达到实验目的,你的理由是_______________。
[反思拓展]实验结束后,组内同学认为K2CO3是盐而其水溶液却显碱性,这可能与它的构成微粒有关,微粒符号是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组利用废硫酸溶液制备K2SO4的流程如下:

(1)将CaCO3研成粉末的目的是___________________。
(2)上述流程中可循环使用的物质有CO2和__________________(填写化学式);
(3)洗涤反应Ⅲ所得晶体不用水而用饱和K2SO4溶液的目是___________________。
(4)检验反应Ⅲ所得晶体是否洗干净的方法是:取最后次洗涤液, 先加入过量的Ba(NO3)2溶液,振荡、过滤,再向滤液中滴加_______________, 如果没有白色沉淀,说明洗涤干净。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置。
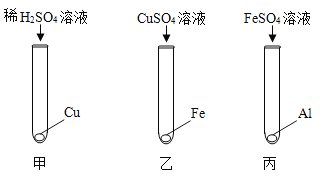
(1)乙实验的现象为___________________。
(2)丙实验中反应的化学方程式___________________。
(3)若将上述实验之一替换掉一种药品,即可达成实验目的.说明具体的改进方法:___________________。
(4)按如图实验结束后,将乙、丙实验后的剩余物倾倒至一个烧杯中, 充分反应。然后将甲实验的剩余物倒入此烧杯,无气泡产生。以下说法正确的是___________________。
A 最后烧杯中的溶液不可能是无色的
B 乙实验中,CuSO4溶液一定是过量的
C 乙、丙混合过程中,可能没有发生化学反应
D 最后烧杯中的溶液,一定含有Al2 (SO4) 3,可能含有FeSO4。
查看答案和解析>>
科目: 来源: 题型:
【题目】请用你具备的化学知识回答下面问题:
(1)收集二氧化碳不能用排水法原因是_____________________。
(2)夏天铁轨之间的缝隙变小的微观原因是_____________________。
(3)“洁厕灵”与“漂白精”不能混用,两者若混合易产生一种有毒气体X。 反应原理为:![]() ,则X的化学式为_____________________。
,则X的化学式为_____________________。
(4)暖气片表面常刷“银粉”(主要成分是铝)利用的是_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求用符号完成下面问题:
(1)标出硫酸铵中氮元素的化合价__________________________。
(2) 由H、C、O、Na四种元素组成的一种盐的化学式_____________________。
(3)由60个碳原子构成的单质分子_____________________。
(4) 黄铜的主要成分_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是()

A.t1°C时, 甲、乙两种溶液中溶质的质量相等
B.要将甲溶液的状态由a点转化为b点,可以加适量溶剂
C.t1°C时,100g 甲物质的饱和溶液中溶质的质量是20g
D.分别将t2°C时两种物质的饱和溶液降温至t1°C,均有晶体析出
查看答案和解析>>
科目: 来源: 题型:
【题目】工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液.完全反应后,过滤洗涤、干燥得沉淀20g。完成下列问题:
(1)反应后溶液中含有的溶质是_____________(写 化学式);
(2)通过已知数据能求出的量有_____________( 写字母序号);
A反应后溶液的总质量
B参加反应的氯化钙的质量
C样品中碳酸钠的质量分数
D氯化钙溶液中溶质的质量分数
(3)计算纯碱样品中氯化钠的质量__________ (写出计算过程)。.
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)实验室制取二氧化碳是中学化学的一个重要实验,同学们在制出二氧化碳后又进行了相关的系列实验,实验装置如图:
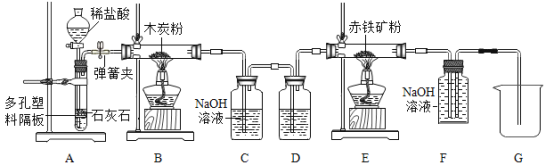
①B装置中反应的化学方程式为_____________________。
②用A装置制气体的最大优点是___________________。
③C装置的作用是__________________,D装置的作用是___________________。
④E装置中发生反应的实验现象为___________________。
⑤F装置除了吸收CO2外,还可以起到的作用是___________________。
(2)在化学实验探究课上,化学老师交给某学习小组一包白色粉末,并提示该粉末由Na2SO4、NaNO2(亚硝酸钠)、NaCl 中的一种或几种组成。该小组同学们探究该白色粉末组成的实验过程如下:
[查阅资料]1亚硝酸盐能溶于水
2Na2SO4、NaNO2、NaCl的部分性质如表:
化学式 | 水溶液的酸碱性 | 与稀盐酸作用 | 毒性 |
NaNO2 | 碱性 | 产生棕红色气体 | 有 |
NaCl | 中性 | 不反应 | 无 |
Na2SO4 | 中性 | 不反应 | 无 |
[实验探究]
限用以下试剂:蒸馏水、酚酞试液、氯化钡溶液、硝酸钡溶液、硝酸银溶液、稀盐酸、稀硝酸
步骤 | 实验操作 | 实验现象 | 实验结论 |
步骤一 | 取少量白色粉末加入试管中,加蒸馏水溶解,滴加____________。 | 无现象 | 白色粉末中不含有NaNO2 |
步骤二 | 另取少量白色粉末加入试管中,加蒸馏水溶解,______________。 | _____________ | 白色粉末中含有Na2SO4和NaCl |
步骤三 | _______________ | _____________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】无水氯化钙在工业上有广泛的用途。以石灰石矿粉(含有SiO2、Fe2O3 、MgSO4等杂质)为原料,生产无水氯化钙的流程如图:
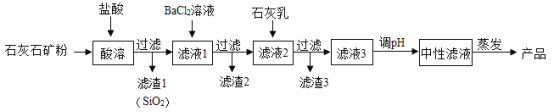
回答下列问题:
(1)从流程图中推知:SiO2具有的化学性质是________________。
(2)加入盐酸的主要作用是______________ ( 写化学方程式);
(3)滤渣3中除有Ca(OH)2外、还有_______________。(填化学式);
(4)产品中的杂质除极少量H2O外,最可能含的是______________ (填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】“见著知微,见微知著”是化学思维方法,观察下图,回答问题。
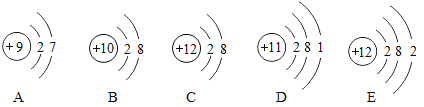
(1)微粒D次外层的电子数是__________________。
(2)属于同种元素的微粒是_______________ (填符号);
(3)微粒A、B、C、D、E中,对应单质化学性质最稳定的是______________(填编号);
(4)微粒C位于第______________周期。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com