
科目: 来源: 题型:
【题目】厉害了我的国!厉害了我的大广西!根据《广西铁路建设“十三五”规划》,2020年全区将基本实现“市市通高铁”,方便人们的出行。

(1)高铁列车利用碳滑板与接触网接触来获取电能。碳滑板通常用石墨制成,这利用了石墨的_______性。
(2)制造高铁列车的材料有:塑料、铝合金、不锈钢等。其中塑料属于_______(选填“金属材料”或“合成材料”);所需钢材通常以赤铁矿(主要成分Fe2O3)为原料炼制,请写出该炼铁原理:_______(用化学方程式表示)。
(3)高铁列车的餐车上为乘客准备的午餐为:大米饭、煎鸡蛋、炒牛肉、大白菜。这份午餐中大米饭提供的主要营养素是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求写出化学符号或符号中数字的意义。
(1)2个硫原子_______。
(2)3个氢分子_______。
(3)人体中含量最多的金属元素_______。
(4)五氧化二磷中磷元素的化合价_______。
(5)NH3中数字“3”表示_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】向装有过量锌粉的烧杯中加入一定质量AgNO3和Cu(NO3)2的混合溶液,烧杯中固体的质量随反应时间变化的情况如图所示。下列说法正确的是( )
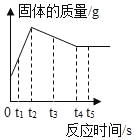
A. t<t2时,若向溶液中滴加NaCl溶液,无明显变化
B. t1时,溶液中金属离子有3种,固体中金属单质有2种
C. t3和t5时,溶液中的溶质种类不同,金属单质种类也不同
D. t1<t<t2时,若向溶液中插入铝丝,铝丝表面有红色固体析出
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在做二氧化锰催化氯酸钾分解的实验时,不小心将黑色的氧化铜当作二氧化锰与氯酸钾混合加热,用排水法收集,发现集气瓶中气泡的产生速率加快了。难道氧化铜对氯酸钾的分解也有催化作用?该同学展开如下探究:
(提出问题)氧化铜对氯酸钾的分解是否有催化作用?
(设计实验)
实验组 | 实验步骤 | 测量数据 |
① | 将 3.0 g 氯酸钾放在试管中加热,用排水法收集生成的气体 | |
② | 将 3.0 g 氯酸钾与 1.0 g 二氧化锰均匀混合加热,用排水法收集生成的气体 | |
③ | 将 x g 氯酸钾与 1.0 g 氧化铜均匀混合加热,用排水法收集生成的气体 |
(1)写出实验室加热氯酸钾和二氧化锰的混合物制氧气的化学方程式_____。
(2)实验③中 x 的数值为_____,测量数据为_____。
(实验结论)
(3)经验证,氧化铜可代替二氧化锰催化氯酸钾分解。将实验③完全反应后的固体加水溶解、过滤、_____,若称量得到 1.0 g 黑色粉末(假设氯酸钾完全反应),再将黑色粉末和氯酸钾混合加热,集气瓶中的现象与实验③_____(填“相同”或“不同”)。
(4)实验室还可以用过氧化氢溶液为原料制取氧气,与以氯酸钾为原料制取氧气相比,用过氧化氢溶液作原料的优点是_____(写一点即可)。某同学查阅资料发现氧化铜也能催化过氧化氢溶液分解。小组同学为了比较二氧化锰和氧化铜对过氧化氢溶液的催化效果,利用数字化仪器测得室温下质量相同的两种物质分别与 5 mL 5%的过氧化氢溶液在两个相同的密闭容器内混合时装置内压强的变化过程。
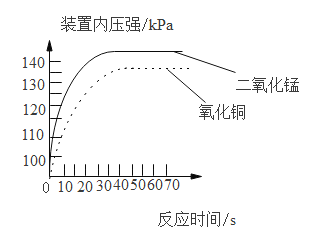
(5)由图像可知:常温下,_____对过氧化氢的分解催化效果更好。
(6)小明推测两条曲线最终将合并在一起,请你说出他的理由_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究小组同学对铝和稀盐酸的反应进行了探究。如图1所示实验,先检查装置气密性,再将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如图2所示的气体压强与时间的关系曲线图。
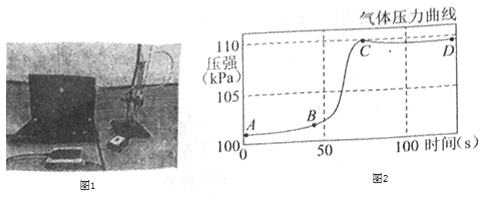
(1)铝与稀盐酸反应的化学方程式为__。
(2)AB段气体压力变化不明显的原因是__;CD段气体压力逐渐下降的原因是__。
(3)从BC段看反应的速率是先变快后变慢,导致变慢的因素有__(填序号)
a.铝片的表面积
b.盐酸的浓度
c.温度
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究小组对蜡烛(主要由碳、氢元素组成)燃烧进行了如下探究。
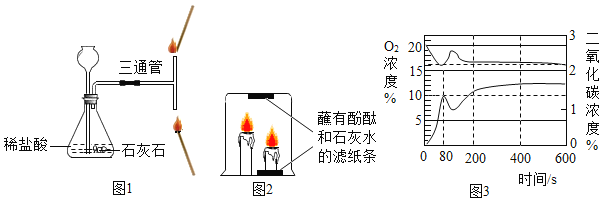
(1)设计图 1 所示实验,锥形瓶中发生反应的化学方程式为_____。请推测靠近三通管_____(填“上口”或“下 口”)的火柴火焰熄灭,理由是_____。
(2)某同学用大烧杯将高低 2 支燃烧的蜡烛罩住,观察到高的蜡烛先熄灭,低的蜡烛后熄灭。
(提出问题)导致高的蜡烛先熄灭的原因是什么?
(猜想与假设)
假设 1:可能是高蜡烛火焰附近的二氧化碳含量过大导致其先熄灭;
假设 2:可能是高蜡烛火焰附近的氧气浓度过低导致其先熄灭。
(设计实验)
甲同学按图 2 装置进行实验,点燃蜡烛,用大烧杯罩住。一段时间后,发现贴在烧杯内上部的滤纸条先褪色。说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的浓度_____(填“高”或“低”)。
(3)为进一步验证假设 1,乙同学收集 1 瓶含 20%氧气和 80%二氧化碳的气体,将点燃的蜡烛慢慢伸入瓶中并密闭,蜡烛点燃一段时间后慢慢熄灭,根据实验现象可知:假设 1_____(填“合理”或“不合理”)。
(4)丙同学使用传感器测得密闭装置内蜡烛从燃烧到熄灭后的过程中(80 s 时蜡烛熄灭),装置内氧气和二氧化碳含量的变化曲线如图 3 。 则可得蜡烛燃烧的条件是_____。
(5)结合已有知识和上述实验分析,乙同学实验中,蜡烛完全熄灭后瓶内含有的气体有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
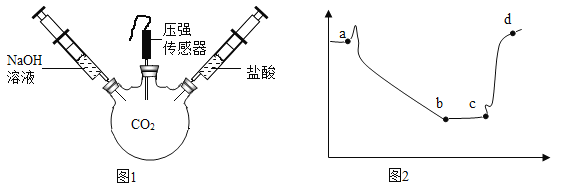
(1)先推入的溶液是____________________________________。
(2)bc段压强不变,原因是______________________________。
(3)cd段压强变大,用化学方程式解释:________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】气体压力传感器与数据采集器和数据处理软件相结合,可用于检测密闭体系内气压变化,并讲气压变化以数字、曲线等多种形式通过计算机实时显示出来,如图为空气中氧气含量测定实验的实验装置图图1及用气体压力传感器测的集气瓶中气压变化图图2.
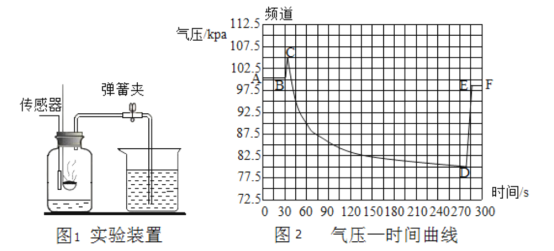
(1)红磷燃烧的化学方程式为________________;
(2)实验中红磷要足量的原因是______________;实验前在集气瓶中预先放入了20ml的水,此处水的作用是____________;若集气瓶的内部体积为200ml,则理论上倒流入集气瓶中的水的体积为__________;
(3)图2中BC段气压变化的原因是_________;CD段气压变化的原因是____________;导致DE段气压变化的实验操作是___________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们学习”二氧化碳实验室制取的研究”课题时,探究了二氧化碳的收集方法。
(查阅资料)
(1)通常状况下 1 体积水约溶解 1 体积二氧化碳,所得溶液的 pH 约为 5.6,pH 越小,二氧 化碳在水中溶解越多。
(2)石灰石中的杂质既不和盐酸反应,也不溶于水。
(提出问题)二氧化碳能不能用排水法收集?
(设计实验) 实验一:在通常状况下,测定二氧化碳溶于水所得溶液的 pH,判断二氧化碳 在水中溶解的体积,如下图:
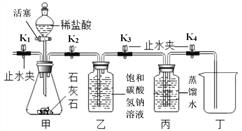
(1)甲装置中反应的化学方程式_____;
(2)检查甲装置气密性的方法是关闭活塞和止水夹 K1 ,打开 K2,K3,K4 双手握住锥形瓶, 观察到_____,说明装置气密性良好;
(3)实验时,需先将甲装置中的空气排尽。其操作是打开止水夹 K1,关闭止水夹 K2 ,打开 活塞,滴加稀盐酸至空气排尽。检验空气排尽的方法是 _____;
(4)关闭 K1 ,打开 K2 、K3 、K4 ,待丙装置中收集半瓶气体时,关闭 K2 、K3 、K4 ,充 分振荡丙装置,分别测得丙、丁瓶装置中溶液的 pH 为 5.5 和 6.5。分析可知,溶解的二氧化碳体积丙装置中_____(填“大于”或“等于”或“小于”)丁装置,乙装置的作用是 _____ ;
(5)实验结束后,装置甲反应后溶液中溶质除了氯化钙还有没有其他物质?请设计实验证明你的猜想(写出实验方法、现象和结论)______
(6)实验二:用二氧化碳数字传感器测得收集的气体中二氧化碳体积分数。如图是收集的 气体中二氧化碳体积分数随时间变化的关系图,从图中能得息:
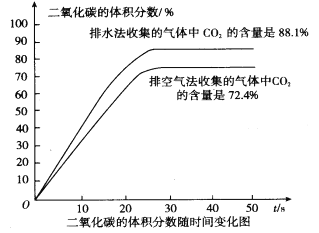
① ________________________________________
②___________________________________________________
(结论反思)由实验一、二分析,改进实验装置,二氧化碳能用排水法收集。能降低二氧 化碳在水中溶解性的措施③_____④_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组在老师指导下进行课外实验,利用下列装置来探究磷单质在空气中燃烧后氧气浓度的变化情况。
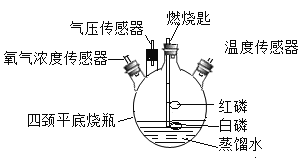
(提出问题)足量红磷在密闭的四颈平底烧瓶内燃烧熄灭后,容器中是否有氧气剩余?
(猜想假设)猜想①:有氧气剩余;
猜想②:无氧气剩余。
(实验验证)该小组同学按图组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)激光笔的作用是__________
(2)红磷燃烧产物与瓶底热水反应生成磷酸(H3PO4)的化学方程式为__________
(3)实验过程中,燃烧匙内的白磷先未燃着的原因是__________
(实验结论)根据上述实验现象,得出结论如下:
(4)结论1:猜想__________正确。
结论2:课本上用“燃烧红磷测定空气中氧气含量”的方法是__________(填“严谨”或“不严谨”)的,其理由是__________
(若回答下列小题,奖励4分,但化学总分不超过60分)
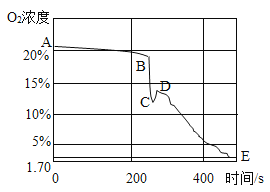
(拓展延伸)如图是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用氧气传感器测量容器内氧气浓度变化的曲线图。
(5)在图中__________(填“A、B、C、D、E”)点时红磷燃烧熄灭;请你解释曲线AB段、DE段氧气浓度变化的主要原因:①__________②__________
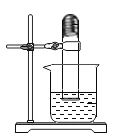
小组同学通过查阅资料可知,验证空气中氧气体积分数较好的药品是铁丝绒,利用铁与氧气、水等的缓慢氧化,可以将空气中氧气浓度消耗至0.2%。将足量细铁丝绒置于试管底部,并倒扣在装有水的烧杯中(如图),一段时间后你将看到的现象是__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com