
科目: 来源: 题型:
【题目】废干电池内的黑色固体含有MnO2、ZnCl2、NH4Cl、C(少量)等物质。化学小组欲通过以下流程,分离并回收部分物质。回答相关问题;
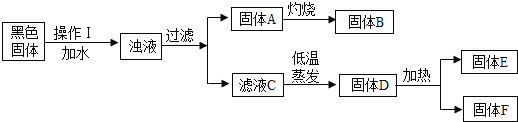
(1)玻璃棒在操作I中的作用:____________________。
(2)过滤后,滤液C仍然浑浊,则造成浑浊的原因可能是_______(填编号)。
A 滤纸破损
B 过滤过程中滤液的液面超过了滤纸的边缘
C 烧杯不干净
D 滤波C中的物质相互反应
(3)固体B常用作催化剂,则B是___(填化学式),写出在空气中灼烧A时发生反应的化学方程式:__。
(4)仅用硝酸银溶液___(填“能”或“不能”)区分E和F。某同学认为固体E是NH4Cl,则检验方法是:____。
(5)NH4Cl属于化学肥料中的_________肥。
查看答案和解析>>
科目: 来源: 题型:
【题目】锂电池是新型高能电池,手机、手提电脑中使用的电池多为锂电池(如图),锂电池具有质量轻、电量大等优点。则:

(1)锂电池内的某个反应可表示为Li+MnO2= LiMnO2。下列关于该反应的说法中正确的是(___)
A 反应中MnO2是催化剂 B 反应前后Mn元素的化合价不变
C 该反应为化合反应 D 生成物LiMnO2为氧化物
(2)现代社会生活中,各种电池用量大幅增加,废电池的回收处理问题已引起人们的关注。回收废电池主要是为了 (_____)
A 利用废电池外壳的金属材料
B 利用废电池中的石墨电极
C 防止废电池中的铅、镉、汞等重金属对土壤和水造成污染
D 防止废电池中渗漏的液体对其它物品造成腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】化学电池是一类重要的能源,按工作性质可分为:一次电池(例如干电池)和二次电池(可充电电池,例如铅酸蓄电池)。请你完成化学电池的利用与回收问题的探究:
(1)铅酸蓄电池放电时能量转变是______能转变成____能。
(2)电动自行车使用一种铅酸电池,而生产电池用的是28%的稀硫酸,将浓硫酸稀释配制成该稀硫酸时,一定将____沿器壁缓慢注入___中,并不断搅拌以防液体飞溅。
(3)使用铅酸蓄电池的电动车与使用汽油燃料的轻便摩托车相比,电动车不会产生________等有害气体,但电池对土壤和水体的污染是不容忽视的。
(4)废旧干电池中许多物质是可以回收利用的。某种型号干电池的剖面如图所示。现对干电池内的填充物(MnO2、C、可溶性糊状物和水)进行探究,请填空:
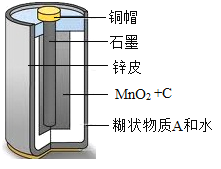
①取填充物溶于水,过滤、洗涤、干燥,得到黑色不溶物。再经过______处理,即可得到纯净的MnO2;
②取①中过滤得到的滤液,分为两份,一份加入烧碱溶液,加热产生一种刺激性气味的气体,该气体的水溶液pH>7,且常用作化肥,则该气体的化学式为______;另一份加入AgNO3溶液,产生白色沉淀,滴加稀HNO3沉淀不溶解,则可推知糊状物的化学式为_。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁金属镍(Ni)是一种应用广泛的金属材料,近似银白色、硬而有延展性并具有铁磁性,能高度磨光和抗腐蚀。则回答:
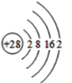
(1)镍原子的结构示意图如图所示,则镍原子的核电荷数数是____,在化学变化中易______(填“失去”或“得到”)电子。
(2)在一定条件下,镍在空气中会形成致密的氧化镍氧化膜(NiO),则反应的化学方程式为_________。
(3)铸造金属硬币用到的材料都是合金,不同材质的合金属于_____(填“纯净物”或“混合物”)。已知镍能发生的反应有:Fe+NiCl2=Ni+FeCl2,该反应属于基本反应类型中的_____反应,反应中Ni的化合价在反应前后______(填“不变”、“升高`“降低”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组同学用下图所示装置探究碳单质和化合物的性质。已知由一氧化碳发生装置得到的CO中混有少量CO2和H2O.
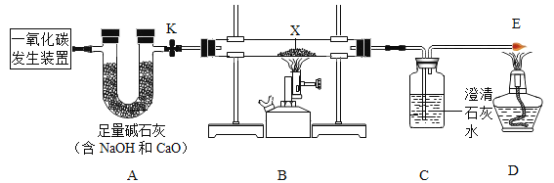
实验一:探究一氧化碳的还原性。按图23装置进行实验,X处放入氧化铜,打开活塞k,通入发生装置中的气体一会,点燃B、D处的酒精灯。
(1) A装置的作用是__________________。
(2) B中玻璃管内发生反应的化学方程式为___________________,证明一氧化碳有还原性的现象是_________。
(3)若通过该实验测铜的相对原子质量,实验中需要获得的数据是_________________。
实验二:探究碳和氧化铜的反应。
(查阅资料)
①碳还原氧化铜时,在一定条件下反应生成铜,或同时生成少量的氧化亚铜(Cu2O);
②Cu2O和Cu都为红色固体,且Cu2O能与稀硫酸反应,反应的化学方程式为![]() .
.
(实验探究)按上图装置进行实验(关闭活塞k)。
(1)取一定质量比的木炭粉和氧化铜的混合物放入X处进行实验,观察到黑色粉末变为红色,经检验红色固体为铜,则X处发生反应的化学方程式为____________________。
(2)另取一定质量比的木炭粉和氧化铜的混合物放入X处进行实验,观察到黑色粉末变为红色,为确定红色固体成份设计了如下实验。称量实验后的红色固体质量为mg,并置于烧杯中, 进行实验,请完成下表内容。
实验操作 | 实验现象 | 实验结论 | 结论解释 |
____________ | 溶液变蓝色有红色固体 | ____________ | ____________ |
(实验结论)一定条件下,碳能还原氧化铜且反应物比例不同,可能生成物不同。
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究CO2与NaOH溶液的反应,某同学进行了下列实验。请你参与。
(1)向NaOH溶液中通入CO2,发生反应的化学方程式为____________,若继续通入CO2,发生反应的方程式为![]() ______________(请填入生成物的化学式)。
______________(请填入生成物的化学式)。
(2)另取NaOH溶液并通入CO2,得到溶液M。向M中滴加稀盐酸,观察到__________现象,由此证明CO2与NaOH发生了反应。
(3)取上述溶液M,加入适量NaOH溶液,得到的溶液中溶质只有Na2CO3,则M中溶质可能是_________,相关反应的化学反应方程式为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据图1、2所示信息,回答相关问题。
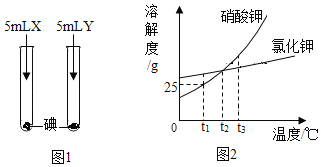
(1)图1所示实验,X、Y分别是水和汽油中的一种,实验中观察到:加入X后固体消失并得到棕色溶液,加入Y后固体未消失,则X是_______________,由实验可知,物质的溶解性与________________有关。
(2)图2为硝酸钾和氯化钾的溶解度曲线,则:
①t1°C时,硝酸钾的溶解度为_________________________。
②t1°C时,将20g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为__________________。
③t2°C时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是_________________________。
④将t3°C时硝酸钾、氧化钾的饱和溶液各100g 分别蒸发10g水,然后降温至t2°C,过滤,得到硝酸钾溶液a和氯化钾溶液b。对于溶液a和溶液b,下列说法正确的是__________________________。
A 都是饱和溶液
B 溶质质量a=b
C 溶质的质量分数a=b
D 溶液质量a<b
E 溶剂质量a<b
查看答案和解析>>
科目: 来源: 题型:
【题目】一年的化学学习,我们对化学反应有了一定的认识。
(1)调控化学反应的快慢。如实验室制取氧气,可以用二氧化锰作_____________,加快反应进行,其反应的化学方程式为_________________________。
(2)判断化学反应的发生。如实验室制取二氧化碳,可以通过________________现象判断反应的发生,其反应的化学方程式为_____________________________。
(3)认识化学反应的实质。如盐酸与氢氧化钠溶液的反应,反应的化学方程式为_________________________,其反应的实质是_________________________。
(4)化学反应往往伴随能量变化。如反应:______________________(用化学方程式表示), 就有热量放出。
(5)化学反应符合质量守恒定律。如4g氢气和16g氧气充分反应,生成水的质量为___ g。
查看答案和解析>>
科目: 来源: 题型:
【题目】建立“宏观一微观一符号”间的联系是化学学习的重要思想。
(1)如图所示是两瓶无色气体,若一瓶是氧气,一瓶是空气(只考虑空气中的氮气和氧气),请设计实验加以区别。完成下表内容,
实验操作 | 实验现象 | 实验结论 |
______________________ | ______________________ | ______________________ |
(2)请在如图的集气瓶中,用![]() 和●表示不同的原子,画出其微观示意图,这样我们还可以从微观视角对两瓶气体进行本质上的区别____。
和●表示不同的原子,画出其微观示意图,这样我们还可以从微观视角对两瓶气体进行本质上的区别____。
(3)我们可以通过原子结构示意图认识原子的结构,氧原子的结构示意图为___________,氧化物中氧元素一般呈-2价的原因是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学就在我们身边。
(1)我们周围有多样的物质。写出一种你熟悉物质的名称____,其化学式为_______________________。
(2)学校营养中餐的食谱为:米饭、红烧肉、麻婆豆腐、白菜粉丝汤,该食谱中含有的基本营养素有_______________________(至少写出两种)。
(3)化肥对提高农作物的产量具有重要作用。硝酸铵(化学式为NH4NO3)是种常用的化肥,从物质类别看硝酸铵属于____ (选填 “酸”,“碱”或“盐”)。往往用化肥中氮的质量分数衡量其肥效,则硝酸铵中氮元素的质量分数为_________________。
(4)硅是“天宫一号”动力源太阳能电池的主要构成材料。单质硅是由石英(SiO2) 与碳在高温条件下反应制得的,同时生成种可燃性气体, 该反应的化学方程式为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com