
科目: 来源: 题型:
【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表,回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.55 | 8.47 | 10.33 |
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是_________(填字母序号)。图中表示氧原子,表示氢原子)

(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式___________________。
(3)为研制一种安全、环保的除湿剂,可选择上表中的__________________(填溶质的化学式)。
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体,则该溶液是________(填“饱和”或“不饱和”)溶液。(已知该温度下氯化钠溶解度为36.1g)
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是_______________________。
②为验证甲同学的猜想是否正确,设计实验方案:_________________________。
(注意:若答对第(6)小题奖励4分,化学试卷总分不超过60分。)
(3)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,由此能否计算所得溶液中溶质组成?若能,请计算其组成;若不能,请补充完成实验方案设计,同时说明需要测定的数据(用a表示),并计算a的取值范围___________。(不要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对锡的绿色回收,设计如下工艺流程:
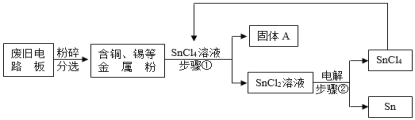
已知:Sn+SnCl4=2SnCl2
(1)塑料属于_____(填“有机物”或“无机物”)。
(2)SnCl2中锡元素的化合价是_____。
(3)铜的金属活动性比锡的_____(填“强”或“弱”);固体A中一定含有的金属元素是_____。
(4)写出步骤②发生反应的化学方程式_____。
(5)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是_____(回答一点)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙。已知:氢氧化镁受热易分解,反应的化学方程式为:Mg(OH)2![]() MgO + H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如下图所示。关于加热一段时间后剩余固体的判断,下列说法错误的是( )
MgO + H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如下图所示。关于加热一段时间后剩余固体的判断,下列说法错误的是( )
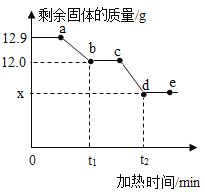
A. 图中a点剩余固体是由一种盐和一种碱组成
B. 若剩余固体中钙元素的质量分数为36.0%,则剩余固体的成分为CaCO3和MgO
C. 图中ab间任一点(不包括a、b两点)的剩余固体成分为CaCO3、MgO和Mg(OH)2
D. 若向c点的剩余固体中加入足量稀盐酸,充分反应生成CO2的质量为(12.0-x)g
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课外兴趣小组欲配制80g质量分数为12%的氢氧化钠溶液来制作“叶脉书签”。
(1)需要氢氧化钠固体的质量为__________g。
(2)称量时,氢氧化钠固体应放在__________(填“滤纸”或“烧杯”)中。
(3)下列说法或操作正确的是__________(填字母序号)。
A配制该溶液时所需的玻璃仪器中不包括玻璃棒
B用量程为100mL的量筒量取所需要的水
C将称量好的固体倒入装有水的量筒中溶解
(4)在量取水的体积时,若采用仰视的方法读数,则所配制的氢氧化钠溶液中溶质的质量分数将__________(填“偏大”或“偏小”)。
(5)某同学用蒸馏水润湿了的pH试纸来测定配制好的溶液的pH值时,他测得的结果会__________(填“偏大”、偏小”或“不变”)。
(6)该兴趣小组的同学提出还可以用配制好的氢氧化钠溶液和稀盐酸进行中和反应实验,具体操作如下图:
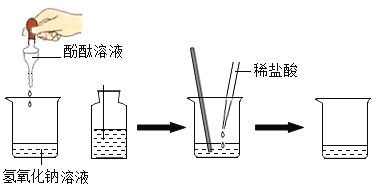
在烧杯中加入10mL的氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液呈__________色。接着加入一定量的稀盐酸,用玻璃棒搅拌后发现溶液为无色,此时__________(填“能”或“不能”)得出两者恰好中和的结论。以下操作及实验现象能证明加入的盐酸为过量的是__________(填字母序号)。
A加入少量铁粉,无明显现象
B滴加紫色石蕊溶液,搅拌后溶液变蓝
C加入碳酸钠溶液,产生气泡
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究铁制品锈蚀的条件,小明用普通铁钉、纯铁钉同时进行下面的四组实验,一段时间后只在实验I中观察到了红褐色的锈斑,其他均无明显变化。下列说法错误的是( )
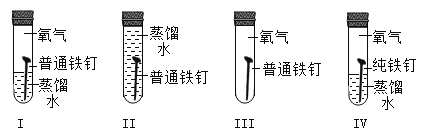
A. I和Ⅱ说明铁制品锈蚀需要O2
B. I和Ⅲ说明铁制品锈蚀需要H2O
C. I和Ⅳ说明H2O和O2同时存在,铁制品不一定发生锈蚀
D. Ⅲ和Ⅳ说明铁制品的锈蚀与铁制品内部结构有关
查看答案和解析>>
科目: 来源: 题型:
【题目】“生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的净化过程相似,如下图所示:(③中离子交换树脂的主要作用是去除重金属离子、软化水质)

(1)②中活性炭的作用是____(填字母。下同),④中超滤膜的作用是____。
A.去除有害菌和部分病毒 B.吸附杂质 C.除去较大的不溶性杂质
(2)若无生命吸管,取用河水时,要降低水的硬度和杀灭病原微生物,生活中常采取______方法。
(3)有的河水出现水华现象,经检测发现是河水中含有尿素、硫酸钾、磷酸二氢钾等而导致,上述三种物质属于复合肥的是___________。
(4)下列图标表示“国家节水标志”的是___________。

查看答案和解析>>
科目: 来源: 题型:
【题目】2019年“中国水周”活动的宣传主题为“坚持节水优先,强化水资源管理”。请回答下列问题:
(1)医疗上的0.9%生理盐水中的溶剂是_______(物质化学式)。
(2)积极推进居民水电阶梯式价格改革。下列做法有利于保护水资源的是______(填序号)
A 大量使用化肥农药 B 工业废水处理达标后排放
C 使用含磷洗衣粉 D 生活污水直接排放
(3)在水蒸发的过程中,下列说法正确的是______(填序号)
A 水分子不断运动 B 水分子之间间隔不变
C 水分子分解成氢原子和氧原子 D 水分子可以保持水的物理性质
(4)科学探究活动中,同学们玩起了以水为主题的“化学反应接龙”小游戏。游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,如图所示。仿照示例完成下列反应的化学方程式。
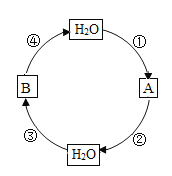
示例:①分解反应::2H2O2![]() H2↑+O2↑
H2↑+O2↑
②置换反应________
③化合反应________
④复分解反应_______
查看答案和解析>>
科目: 来源: 题型:
【题目】中科院大连化物所研究团队发现二氧化碳高效转化新途径,该项新技术为二氧化碳加氢制液体燃料的研究拓展了新思路。利用一种新型多功能复合催化剂,通过下图示意的I、II、III三个环节,将二氧化碳成功转化为汽油。
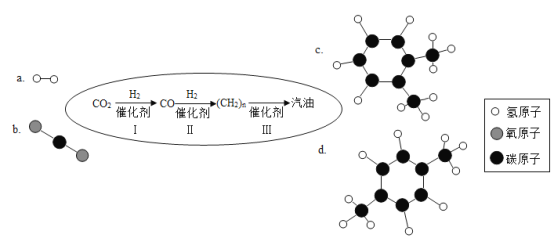
(注明:图中a、b是两种起始反应物的分子结构模型,c、d是最终制得的汽油中所含物质的分子结构模型)
请回答下列问题:
(1)在一定温度、一定压强和催化剂存在的条件下,环节I除生成CO外,还生成了一种化合物,则反应的化学方程式为_____。该反应中,二氧化碳中的部分氧元素被氢气夺去,二氧化碳发生了___(填“氧化”或“还原”)反应。
(2)观察c和d两种物质的分子结构模型,两种物质的化学式都可表示为C8H10,其中碳、氢元素的最简质量比为____,属于_____(填“无机”或“有机”)化合物。c和d的化学性质不同的原因是____。
(3)“二氧化碳变汽油”的研究成果,使我国成为此领域的世界领跑者。你认为该成果的现实意义是______,_______(答出两条即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国研究团队设计了一种高效稳定的Na-Fe3O4多功用复合催化剂,具有特殊的性质和功能,纳米四氧化三铁具有类似人工模拟酶的催化性能。
(1)在高温条件下用普通铁粉和水蒸气反应,得到粉末状的四氧化三铁和氢气。该反应的基本类型为___。
(2)四氧化三铁可近似地看作是氧化亚铁和氧化铁的化合物,它不溶于水,能与酸反应生成两种盐。请写出四氧化三铁与盐酸反应的化学方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国首架具有完全自主知识产权的大型喷气式客机C919(如图一)在上海浦东国际机场首飞成功,先进材料首次在国产民机大规模应用。回答下列问题:
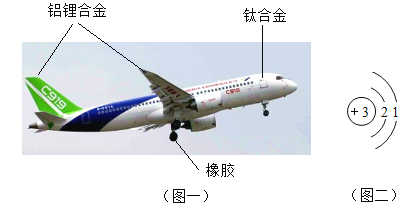
(1)第三代铝锂合金材料属于_____(填“纯净物”或“混合物”)。铝锂合金的硬度要_____(填“高于”或“低于”)铝和锂,其熔点要_____(填“高于”或“低于”)组成它的成分金属。这种材料具有较高的强度和适宜的延展性,都属于_____(填“物理”或“化学”)性质。
(2)铝锂合金中的铝(Al)元素和锂(Li)元素的本质区别是_____(填序号)
A 元素符号不同 B 原子质量不同
C 原子的质子数不同 D 原子的电子数不同
(3)锂元素的原子结构示意图如图二所示,该原子在化学反应中易_____(填“得到”或“失去”)最外层电子,所形成的离子符号为_____。
(4)钛合金中的一种钛原子核内有 22 个质子和26 个中子,钛原子的核外电子数为_____,相对原子质量为_____。
(5)新材料的应用是C919的亮点。飞机大量使用合金材料,分析其原因是_____。
(6)铝的金属活动性比铁的_____(填“强”或“弱”)。空气中,铝比铁具有更好的抗腐蚀性,用化学方程式解释原因为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com