
科目: 来源: 题型:
【题目】要用溶质质量分数为19.6%的稀硫酸与金属锌反应制取氡气,请回答下列问题
(1)用水和浓硫酸来配制500g溶质质量分数为19.6%的稀硫酸。需溶质质量分数为98%的浓硫酸的质量为__________g;
(2)配制溶液时,用玻璃棒不断搅拌,玻璃棒的作用是_______________;
(3)取配制后的溶液50g与足量的金属锌反应,生成氢气的质量为_________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表是学习和研宄化学的重要工具,试根据图示回答相应问题:
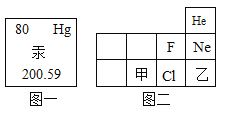
(1)图一是汞元素在元素周期表中的信息,则汞元素属于______________(填“金属”或“非金属”)元素,该元素的原子核外电子数为____________;
(2)图二为元素周期表的一部分,甲、乙代表两种不同元素,以下判断正确的是_________(填字母序号)。
A甲的原了序数大于乙
B甲和Cl在同一周期
C乙和He的最外层电子数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】轻质碳酸钙,又称沉淀碳酸钙,即高纯度的碳酸钙,它密度小、白度高、摩擦系数小,是制造牙膏的原料之一,常用在高档或浅色制品上。工业上通常以石灰石(主要成分为CaCO3)为原料,按下图所示工艺流程进行高纯度碳酸钙的制取与提纯:
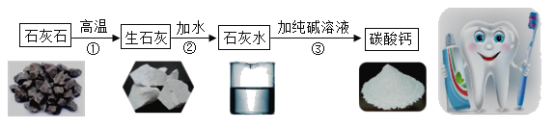
根据上述信息,试回答下列问题:
⑴石灰石的用途非常广泛,下列有关说法正确的是_____(单项选择)。
①可用于制取二氧化碳 ②可用于制取生石灰 ③可用于制造玻璃
④可用于治理酸性污水 ⑤可加入煤炭中做固硫剂 ⑥可用作高炉炼铁造渣剂
A ①③⑤⑥ B ②④⑤⑥ C ①②④⑤⑥ D 以上全部都是
⑵上述流程所涉及的物质中,可用作干燥剂的物质是_____。
⑶上述流程的步骤③中,还可以选择另外一种试剂采用沉淀法制备出高纯度的碳酸钙,其反应原理的化学方程式为_____。
⑷制备高纯度碳酸钙要经历“石灰石(CaCO3)→生石灰→石灰水→CaCO3”的转化过程,其目的是_____。
⑸小颖同学称取了25.0g某石灰石样品,按上图流程进行了模拟实验探究。她在步骤③中向石灰水里滴加了溶质质量分数为10%的Na2CO3溶液,该过程中产生沉淀的质量与加入Na2CO3溶液的质量关系如图所示。试计算:
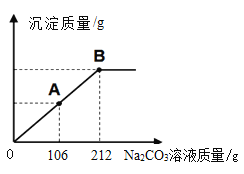
上述实验中,小颖最终制得轻质碳酸钙的质量?_____(结果精确到0.1g)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验室现有一包固体混合物A,它可能由Fe、Cu、CuO、Ca(OH)2、Na2CO3五种物质中的三种或多种组成。某化学兴趣小组的同学欲探究其成分组成,他们按下图所示进行了实验探究,出现的现象如图中所述。(设过程中所有可能发生的反应都恰好完全进行)
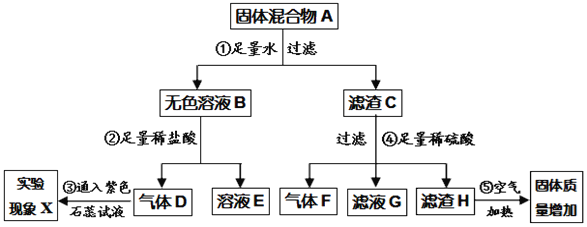
根据上述信息,试回答下列问题:
⑴现象X中,气体D使紫色石蕊试液变成了_____色;无色气体F是_____(写化学式)。
⑵溶液E中一定大量存在的金属阳离子为_____(写离子符号)。
⑶写出步骤②中发生反应的化学方程式:_____。
⑷写出步骤⑤中发生反应的化学方程式:_____。
⑸根据上述信息,可推知固体混合物A中一定存在的物质是(写化学式)_____。
⑹根据上述信息,固体混合物A中仍然不能确定的物质是(写化学式)_____,你的理由是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。
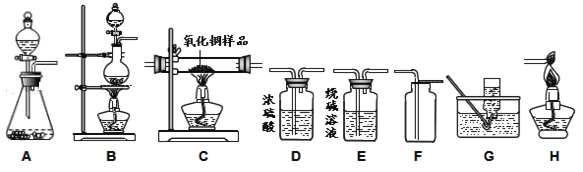
试根据题目要求,回答下列问题:
⑴请写出能用装置A制备的一种气体的化学反应方程式_____,该气体可选用装置_____来收集(填装置序号),其选择依据是_____。
⑵小颖同学欲用干燥、纯净的一氧化碳气体还原某氧化铜样品(杂质只有铜),并测定其纯度。
(查阅资料)
将草酸(H2C2O4)晶体与浓硫酸混合加热,会产生一氧化碳等气体,其反应原理为:H2C2O4 CO↑+CO2↑+H2O。
CO↑+CO2↑+H2O。
①若小颖同学选用草酸来制取CO,其发生装置她应选择_____(填装置序号)。
(定量实验)
②小颖同学先用电子秤称取了1.00g氧化铜样品,放入装置C中的玻璃管内并组装好所有相关仪器,再将草酸分解得到的气体产物按照以下仪器的连接顺序进行实验:混合气体→D→C→E→H,最后,通过测量反应前后装置E的质量变化进行计算。(已知:CO+CuO![]() Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是_____。
Cu+CO2)实验过程中,在装置C的大玻璃管内可观察到的现象是_____。
③请你分析上述实验方案存在的不足之处及对应的改进方法_____。
④实验改进后,小颖同学对实验所得的正确数据进行分析处理(设所发生的反应均完全进行):通过测定,当装置C中的氧化铜全部被还原后,装置E的质量增加了0.33g,则该样品中氧化铜的质量分数为_____(结果精确至0.1%)。
⑤小黄同学提出了异议,他认为若②中实验方案不加以改进,也能正确测算出该样品中氧化铜的纯度,他的计算依据或方法为:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学用语是化学学科的专用语言,也是学习化学的重要工具。
⑴请从氧气、二氧化碳、氯化钠、盐酸、硫酸、氢氧化钙中选择合适的物质,将其化学式填写在下列横线上。
①可供给呼吸的气体单质_____②参与光合作用的氧化物_____
③一种不易挥发的无机酸_____④常用于食品调味的盐_____
⑵铁缺乏被认为是全球三大“隐性饥饿”之首(微量营养元素缺乏),全球约有1/5的人患缺铁性贫血。食物铁强化是目前国际公认的最经济、有效和可持续的给人群补铁的方法。中国疾控中心研制的新型铁强化剂(EDTA钠铁)在人体内的铁吸收、利用率高于其他铁剂,是传统补铁剂硫酸亚铁的2倍至3倍。它在酱油中的溶解性较好,不影响食品口感,不改变酱油的原有口味。此外,EDTA钠铁在食品加工和储存过程中性质稳定,它在酱油中可稳定保持两年以上。研究表明,应用铁强化酱油补铁效果显著。EDTA钠铁的化学式为C10H12FeN2NaO8,它是一种淡土黄色结晶性粉末,易溶于水,性质稳定,不易被氧化,其水溶液pH在3.5~5.5之间。



根据上述信息,请回答下列问题:
①EDTA钠铁属于_____。(选填“混合物”、“有机物”、“无机物”或“氧化物”之一)
②EDTA钠铁中,碳、氧原子个数比为_____(填最简整数比)。
③EDTA钠铁中,元素质量分数最小的是_____元素。
④EDTA钠铁的化学性质有_____(至少答一条)。
⑤若经常使用铁锅炒菜做饭,也能有效预防缺铁性贫血,其反应原理的化学方程式为:(已知胃液中含有盐酸)_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钠非常活泼,常温下在空气中易被氧化,也易与水反应。现将5.4g部分氧化的金属钠样品放入150g 16%的硫酸铜溶液中,充分反应后过滤,得到9.8g蓝色滤渣。(已知样品成分仅为Na和Na2O,相关反应①![]() ②
②![]() ),下列计算错误的是( )
),下列计算错误的是( )
A.最终所得溶液中存在两种溶质
B.最终所得溶液的质量为145.5g
C.原混合物中钠元素质量为4.6g
D.原混合物中钠和氧化钠的质量比为46: 31
查看答案和解析>>
科目: 来源: 题型:
【题目】小黄同学进行了有关金属活动性顺序的实验探究,其实验过程及实验现象如图所示。则下列有关分析判断中,正确的是( )。
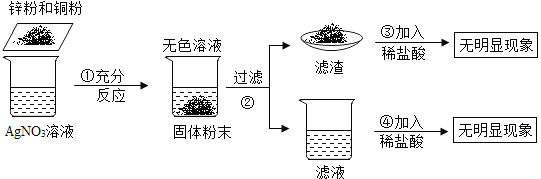
A.滤液中可能含有Ag+
B.滤渣中可能含有单质锌
C.滤液中只含有Zn2+
D.滤渣质量小于原混合粉末质量
查看答案和解析>>
科目: 来源: 题型:
【题目】用数轴表示某些化学知识,简洁明了且易记。下列数轴表示不正确的是( )
A. 金属始用的年代:![]()
B. 铁元素化合价:![]()
C. 碳元素质量分数:![]()
D. 物质的水溶性:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com