
科目: 来源: 题型:
【题目】某校化学兴趣小组进行了有关影响金属和酸反应的影响因素的实验探究。
小亮设计了如下实验(如图1):发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。
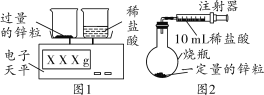
(提出问题)一定质量的某种金属和等体积盐酸反应速率快慢的影响因素有哪些?
下表为锌粒与等体积稀盐酸溶液反应的实验数据:
组别 | 稀盐酸溶 液的浓度 | 反应开始时酸溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
第一组 | 5% | 20℃ | 10 mL | 60 mL |
10% | 20℃ | 19 mL | 118 mL | |
15% | 20℃ | 28 mL | 175 mL | |
第二组 | 5% | 35℃ | 28 mL | 60 mL |
10% | ____ | 72 mL | 118 mL | |
15% | 35℃ | 103 mL | 175 mL |
(实验分析)
(1)分析实验数据得出:通过比较____可知盐酸溶液浓度是影响金属和酸反应快慢的因素;通过比较_______可知反应时溶液温度是影响金属和酸反应快慢的因素。
(2)可以通过比较______来确定金属和酸的反应速率。
(3)写出该反应的化学方程式________。
(反思评价)
(1)过量锌粒加入到稀盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因_____________。
(2)小丽设计了如图2所示实验装置用以测定一定量锌粒和稀盐酸反应产生气体的体积。请你分析图2与图1所示装置比较,其优点是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某班同学分别用向上排气法(瓶中加2mL水,标为甲)和排水法(瓶里留有2mL水,标为乙)各收集一瓶氧气,然后进行铁丝燃烧的实验,发现:铁丝在甲瓶中不能燃烧,在乙瓶中火星四射。
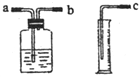
【提出问题】铁丝燃烧与___________________有关。
【查阅资料】氮气性质稳定,在加热条件下不与铁、碳、氧气等物质反应。
【讨论方案】如果选用如图16所示的仪器收集氧气,仪器接口的连接顺序是_________填“a”“b”或“c”)。
【进行实验】取5根相同的铁丝(直径0.6mm),卷成相同的螺旋状后,分别在体积分数不同的集气瓶中进行实验,如下图所示。实验记录如下:
实验次数 | 氧气的体积分数% | 实验现象 |
第一次 | 90% | 燃烧剧烈,火星四射,燃烧时间长,实验成功 |
第二次 | 80% | 燃烧现象与90%的相比没有明显差异,实验成功 |
第三次 | 70% | 燃烧比80%的弱,燃烧时间比80%的短,实验成功 |
第四次 | 60% | 燃烧比70%的弱,燃烧时间更短,实验成功 |
第五次 | 50% | 铁丝没有燃烧 |
(1)铁丝燃烧的化学方程式为_____________________________________。
(2)通过这组探究实验,可得出的结论是______________________________________。
(3)要研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是_______________
A.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C.在两瓶相同浓度的氧气中,分别进行粗、细铁丝的燃烧实验
【反思与评价】
(1)对氧气纯度要求较高的实验应采用______________方法收集氧气。
(2)在以上的实验中,某同学将集气瓶中装入一半的水,塞紧瓶塞,再通过排水法收集氧气,当把水排净时,收集到的氧气的体积分数约为(______)
A. 50% B.60% C.70% D.80%
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,向盛有铁钉的试管中注入稀盐酸,实验结束后铁钉连同废液一起倒入指定的带有纱网的烧杯中,实验中发现纱网上的铁钉很容易生锈,生锈应该是铁钉与________共同作用的结果。

(提出问题)为什么纱网上的铁钉更容易生锈呢?
(小明猜想)纱网上的铁钉表面可能有盐酸,是不是酸能促进铁钉生锈呢?
(实验验证)
(1)从纱网上取5枚干燥的铁钉放入试管中,加水没过铁钉,轻轻的摇动试管后,把液体转移入小烧杯,测定该液体的pH,测定方法是_______,结果pH=5。
(2)请你设计一个对比实验,直观地证明酸能促进铁钉生锈:___________。
(拓展延伸)生锈的铁钉要想重复使用需要除掉铁锈。小明把生锈铁钉泡在废弃的稀盐酸中,很快发现铁锈消失,溶液变成________色,反应的化学方程式是___________。小明继续观察,发现溶液中又产生了许多气泡,他猜想是产生了氢气,于是收集了一试管的该气体,他又做了实验:____。证明该气体就是氢气。
(反思交流)为保证铁钉重复利用,倒在纱网上的铁钉应该________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计了如下图所示的装置,用于实验室制取CO2并对它的部分性质进行探究,按要求答题。
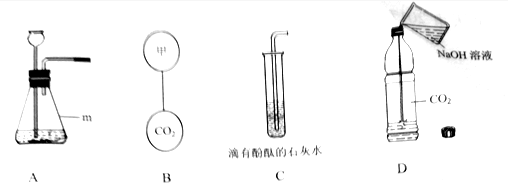
(1)仪器m的名称是_________,图A中发生反应的化学方程式为_________。
(2)若要图B中的两个气球悬浮在空气中,则气体甲可能是______(填序号)。
A.空气 b.氧气 c.氢气
(3)往图C中的试管通入CO2,当出现_________现象,表明石灰水的溶质刚好完全沉淀。
(4)向图D中的塑料软瓶中倒入一定量的NaOH溶液,迅速拧紧瓶盖,振荡,可观察到瓶子变瘪。若使塑料软瓶恢复原状,可用注射器向瓶中注入过量的_________(填试剂名称)充分反应即可,反应完成后瓶中溶液的溶质是_________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】为加深对一氧化碳还原性的理解,减少一氧化碳对环境的污染,某同学设计了如图所示的实验:
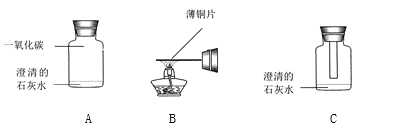
回答下列问题:
(1)图B中,薄铜片受热时发生反应的化学方程式为 。
(2)趁热将图B所示的薄铜片插入到图A所示的装置中(如图C所示),观察薄铜片的颜色变化,现象是 ;振荡集气瓶,观察到的现象是 。
(3)实验结束后用燃着的木条点燃瓶中的剩余气体,有明显的蓝色火焰出现,该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(2017石家庄新华区模拟)实验是进行科学探究的重要方式。某同学设计如图所示实验,制取二氧化碳并探究其性质,请回答有关问题。
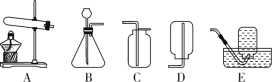
(1)实验室用稀盐酸与石灰石反应制取二氧化碳,应选用的装置是________(填编号);其中此发生装置也可以用来产生O2,该反应的化学方程式为____________。
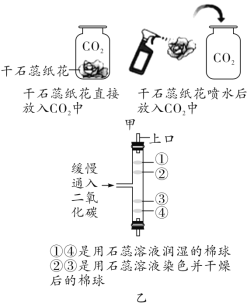
(2)实验甲用了科学探究中的控制变量法,该实验控制的变量是________。干石蕊纸花喷水后放入二氧化碳中,观察到纸花由紫变红,该反应的化学方程式是_____________。
(3)实验乙是在实验甲的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第________(填序号)号棉球先变色。
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们用下图所示装置进行实验,验证CO2与NaOH、Ca(OH)2都能发生反应。
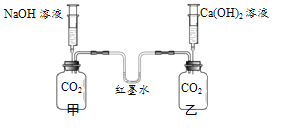
分别向甲、乙两个瓶中注入少量、等体积的两种溶液,观察实验现象。
(1)甲中反应的化学方程式是 。说明CO2能与Ca(OH)2反应的实验现象是 。
(2)下列实验现象中,一定能说明“CO2与NaOH发生了化学反应”的是 (填序号)。
a.U型管中红墨水左低右高
b.U型管中红墨水左高右低
c.U型管中红墨水液面没有发生改变
查看答案和解析>>
科目: 来源: 题型:
【题目】(2016河北中考说明题型拓展)将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示。下列说法正确的是( )
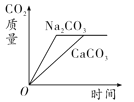
A.CaCO3一定没有剩余
B.消耗HCl与H2SO4的质量比为36.5∶98
C.消耗CaCO3与Na2CO3的质量比为1∶1
D.反应产生水的质量相等
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组称取4.0 g石灰石样品,把40 g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10 g | 3.0 g |
第二次加入10 g | 2.0 g |
第三次加入10 g | 1.0 g |
第四次加入10 g | 0.6 g |
请计算:
(1)4.0 g石灰石样品中碳酸钙的质量是_____g。
(2)求稀盐酸的溶质质量分数。
查看答案和解析>>
科目: 来源: 题型:
【题目】A-H是初中化学常见的物质,C是黑色固体,H是金属单质,煅烧石灰石得到E;可用F与D配制波尔多液作农药,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略,请回答下列问题:
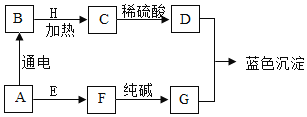
(1)E的俗称_____________。
(2)物质A属于__________(填“酸”“碱”“盐”或“氧化物”)。
(3)写出由F→G的化学方程式_________________;
(4)上述转化中没有涉及的基本反应类型是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com