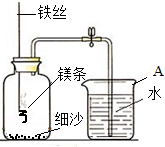
某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
(1)右图中A仪器的名称是
,燃烧、冷却后打开止水夹,水能进入集气瓶中的原因是:
.
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.
氮气是怎么减少的呢?
【假设一】氮气与镁条反应而减少.
【假设二】
.
镁条在氮气中燃烧,生成氮化镁(Mg
3N
2)固体,反应的方程式为:
反应类型为
,其中氮化镁中氮的化合价是
.镁条还可以在二氧化碳中燃烧生成碳和氧化镁,反应的方程式为
,该反应的类型是
.
(3)通过以上探究,你对燃烧的有关知识有了什么新的认识:
.(请写出两点).
(4)小芳为测定Vc药片中维生素C(化学式为C
6H
8O
6)的质量分数,进行了如下实验:
取Vc药片2g,共消耗I
2的质量为2.54g.请你帮助小芳计算该Vc药片中维生素C的质量分数.(反应原理:C
6H
8O
6+I
2=C
6H
6O
6+2HI ).

